Соли: определение, классификации, номенклатура. Способы получения.
Со́ли — класс химических соединений, состоящих из катионов и анионов
Номенклатура солей
Названия солей связанны с названиями соответствующих кислот:
Названия кислых солей имеют приставку гидро- (один атом водорода) или дигидро- (два атома водорода) к названию аниона
Названия основных солей имеют приставку гидроксо- или дигидроксо- к названию катиона
Названия оксосолей имеют приставку оксо- или диоксо- к названию катиона металла
Получение солей
Способы получения солей многочисленны
Соли образуются при взаимодействии.
1. Металлов с неметаллами
2. Основных оксидов с кислотами
3. Кислотных оксидов со щелочами
4. Амфотерных оксидов с кислотами
5. Амфотерных оксидов со щелочами
6. Основных оксидов с кислотными
7. Амфотерных оксидов с кислотными оксидами
8. Амфотерных оксидов с основными оксидами
9. Кислот со щелочами (реакция нейтрализации)
10. Оснований с кислотами
11. Амфотерных оснований со щелочами
12. Металлов с кислотами
13. Металлов с солями
14. Щелочей с солями
15. Кислот с солями
16. Солей с солями
Все соли разделяются на средние, кислые и основные. Средние соли содержат только атомы металла и кислотного остатка.
Кислые соли образуются многоосновными кислотами. Одноосновные кислоты кислых солей не образуют.
Кислые соли, помимо ионов металла и кислотного остатка, содержат ионы водорода.
Названия кислых солей содержат приставку "гидро" : 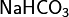
Основные соли образуются при неполной нейтрализации основания. Названия основных солей образуют с помощью приставки "гидроксо".
Основные соли, помимо ионов металла и кислотного остатка, содержат гидроксильные группы.
Основные соли образуются только из многокислотных оснований. Одноокислотные основания таких солей образовать не могут. : 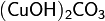
Предмет химической термодинамики.
Задачей химической термодинамики является применение законов общей
термодинамики к физическим и физико-химическим
явлениям (реакциям, фазовым превращениям). С помощью химической термодинамики можно решить много вопросов, возникающих у химиков-теоретиков
и технологов в процессе их практической деятельности, в частности такие, как:
. расчет тепловых эффектов процессов для различных условий;
. определение температур или теплот фазовых переходов;
. выбор оптимального технологического режима проведения процесса;
. определение условий подавления побочных (нежелательных) реакций и процессов;
. определение областей устойчивости вещества.
Химическая термодинамика изучает переходы энергии из одной формы в
другую, от одной системы к другой; энергетические эффекты, сопровождающие различные физические или химические процессы, зависимость их от условий; возможность протекания, направление и пределы самопроизвольного протекания самих процессов в рассматриваемых условиях. Термодинамика базируется на двух основных законах, называемых первым и вторым началами термодинамики, которые были установлены на основании опыта человечества.
Основные понятия химической термодинамики. Первый закон термодинамики.
Основные определения
Система – это тело или группа тел, которые находятся во взаимодействии
и условно обособлены от окружающей среды, в качестве которой рассматривается остальная часть вселенной.
Обмен энергией между системой и внешней средой может происходить
в виде теплоты и в виде работы. Работа может быть механической и немеханической (например, химической).
Системы подразделяют на гомогенные и гетерогенные.
Гомогенной называют систему, имеющую в каждом элементе объема одинаковые плотность и состав (например, раствор сахара в воде).
При наличии уравнений связи независимые составные части становятся взаимно зависимыми. Их называют компонентами. Число компонентов равно числу составных частей минус число уравнений связи.
Совокупность свойств системы называется ее состоянием.
Свойства, которые однозначно определяют состояние системы, называются термодинамическими параметрами. В свою очередь параметры делятся
на две группы. Параметры, зависящие от количества вещества, составляющего
систему, которые подчиняются закону аддитивности, называются экстенсивными. Параметры, которые не зависят от количества вещества и имеют одинаковые значения во всех точках системы, если она находится в равновесии называются интенсивным.
Процесс – это изменение состояния системы. Процесс может протекать в
равновесных условиях, когда при бесконечно малых воздействиях со стороны
внешней среды происходят бесконечно малые изменения параметров. Разновидностью равновесного процесса является обратимый процесс, совершив который, система возвращается в исходное состояние, не оставив изменений ни в системе, ни в окружающей среде.
Неравновесный (необратимый) процесс – это процесс, при котором изменения в системе происходят и при этом система не возвращается в исходное со-
стояние.
Первый закон термодинамики - Изменение внутренней энергии системы при ее переходе из одного состояния в другое равно сумме количества теплоты, подведенного к системе извне, и работы внешних сил, действующих на нее:
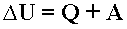
Первый закон термодинамики - количество теплоты, подведенное к системе, идет на изменение ее внутренней энергии и на совершение системой работы над внешними телами: