Тема 3. Реакционная способность углеводородов, спиртов, фенолов, тиолов и аминов
3-01 Стабильность свободных радикалов уменьшается в ряду:
1) CH3CH21) 2>3>1>4
2) (CH3)2CCH2CH3 2) 2>4>1>3
3) CH3CHCH3 3) 2>1>4>3
4) CH3 4) 3>1>2>4
5)4>3>1>2
3-02 Гомолитический разрыв связи С-Н в пентене-2 приводит к образованию радикалов аллильного типа
1) У атома C-1
2) у атома C-2
3) у атома C-3
4) у атома С-4
5) у атома C-5
3-03 Радикалы аллильного типа, которые образуются в процессе пероксидного окисления олеиновой кислоты
1) CH3(CH2)6CHCH=CH(CH2)7COOH
2) CH3(CH2)7CH=CH(CH2)6CHCOOH
3) CH3(CH2)5CHCH2CH=CH(CH2)7COOH
4) CH3(CH2)7CH=CHCH(CH2)6COOH
5) CH2(CH2)7CH=CH(CH2)7COOH
3-04 Основания Бренстеда
1) C2H5NH2
2) C2H5OC2H5
3) CH3CH=O
4) (C2H5)2NH
5) CH3CH2CH3
3-05 Стабильность карбокатионов уменьшается в ряду
1) (CH3)2CCH2CH3 1) 2>3>1>4
2) CH2=CHCHCH3 2) 2>4>1>3
3) CH3CH2 3) 2>1>4>3
4) CH3CH2CHCH3 4) 3>1>2>4
5)4>3>1>2
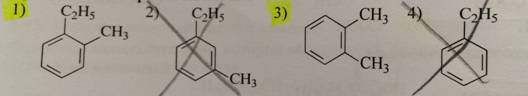
3-06 Продукт окисления 1,3-диэтилбензола
3-07
Кислота Бренстеда - Формула
1) NH-кислота - CH3CONH2
2) SH-кислота - C2H5SH
3-08 Взаимодействуют при комнатной температуре
Реагент - Соединение
1) Раствор гидроксида натрия -C6H5OH
2) Хлороводородная кислота - (C2H5)2NH
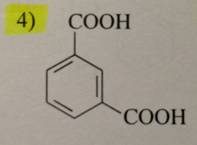
3-09 Соединения, которые образуют изофталевую (бензол-1,3-дикарбоновую) кислоту при окислении хромовой смесью

3-10 Соединения, которые образуют фталевую (бензол-1,2-дикарбоновую) кислоту при окислении хромовой смесью
3-11 Соединение, способное реагировать с раствором гидроксида натрия
1) CH3CH2CH2OH
2) C2H5SH
3) CH3CH=CH2
3-12 Соединение, образующее относительно прочные межмолекулярные водородные связи
1) C6H13OH
2) CH3CH2CH=O
3) CH3CH2COOH
4) C6H5SH
5) CH3CH2OCH3
3-13 Наиболее сильные кислотные свойства проявляет
1) CH3CH2COOH
2) CH3CH2CH2SH
3) (CH3)2NH
4) (CH3)2CHCH2OH
3-14 Наиболее сильные основные свойства проявляет
1) CH3CH2CH2CH2NH2
2) C2H5OH
3) –
4) –
3-15 Наиболее сильные основные свойства проявляет
1) –
2) CH3CH2CH2CH2SCH3
3) (CH3CH2CH2)2NCH3
4) (CH3)2CHCH2OCH3
3-16 Продукт реакции мягкого окисления пропантиола-1
1) CH3CH2CH2-S-OH
2) CH3CH2CH2-S-S-CH2CH2CH3
3) CH3CH2CH2-SH=O
4) CH3CH2CH2-S(O)2-OH
5) CH3CH2CH2-S(O)2-CH2CH2CH3
3-17 Соединение, обладающее амфотерными свойствами
1) CH3CH2COOH
2) H2NCH2CH2NH2
3) –
4) Н2N-( бензольноекольцо)-ОН
3-18 Соединение, способное реагировать с хлороводородной кислотой
1) C6H5OH
2) CH3SH
3) (CH3)3N
4) CH3CH2CH2CH2COOH
3-19 Кислотные свойства соединений в растворе увеличиваются в ряду
1) CH2CH5OH 1) 3<2<1<4
2) C2H5SH 2) 3<4<1<2
3) C2H5NH2 3) 2<1<4<3
4) CH3COOH 4) 3<1<2<4
3-20
Схема реакции - Механизм реакции
1) CH3CH=CH2+H2O….. - электрофильное присоединение
2) CH3CH(OH)CH3……. - элиминирование
3-21 Синее окрашивание с гидроксидом меди 2 дает соединение
1) C6H5OH
2) HOCH2CH(OH)CH2OH
3) CH3COOH
4) H3CC(CH3)(OH)CH3
5) –
3-22 Соединения, проявляющие амфотерные свойства
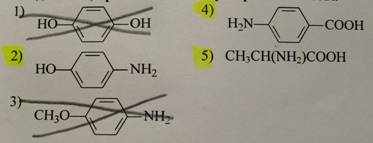
3-23 Нуклеофильные реагенты
1) H-
2) H2O
3) C2H5S-
4) C2H5OH2
5) (C2H5)2NH2
3-24 Схема реакции внутримолекулярной дегидратации спирта
1) CH3CH2CH2OH+HBr—CH3CH2CH2BR+H2O
2) CH3CH2CH2OH—CH3CH2CH2OCH2CH2CH3+H2O
3) CH3CH2CH2OH+Na—CH3CH2CH2ONa+H2
4) CH3CH2CH2OH—CH3CH=CH2+H2O
5) CH3CH2CH2OH+H2SO4—CH3CH2CH2OSO3H+H2O
3-25 Соединение, проявляющее амфотерные свойства
1) H2NCH2COOH
2) CH3CH2CH2CH3
3) –
4) –
