Водородный показатель среды растворов – pH.
Водородный показатель – рН – это мера активности (в случае разбавленных растворов отражает концентрацию) ионов водорода в растворе, количественно выражающая его кислотность, вычисляется как отрицательный (взятый с обратным знаком) десятичный логарифм активности водородных ионов, выраженной в молях на литр.
pН = – lg[H+]
Это понятие было введено в 1909 году датским химиком Сёренсеном. Показатель называется pH, по первым буквам латинских слов potentia hydrogeni – сила водорода, или pondus hydrogenii – вес водорода.
Несколько меньшее распространение получила обратная pH величина – показатель основности раствора, pOH, равная отрицательному десятичному логарифму концентрации в растворе ионов OH:
рОН = – lg[OH–]
В чистой воде при 25°C концентрации ионов водорода ([H+]) и гидроксид-ионов ([OH-]) одинаковы и составляют 10-7моль/л, это напрямую следует из константы автопротолиза воды Кw , которую иначе называют ионным произведением воды:
Кw = [H+] · [OH–] =10–14 [моль2/л2] (при 25°C)
рН + рОН = 14
Когда концентрации обоих видов ионов в растворе одинаковы, говорят, что раствор имеет нейтральную реакцию. При добавлении к воде кислоты концентрация ионов водорода увеличивается, а концентрация гидроксид-ионов соответственно уменьшается, при добавлении основания – наоборот, повышается содержание гидроксид-ионов, а концентрация ионов водорода падает. Когда [H+] > [OH–] говорят, что раствор является кислым, а при [OH–] > [H+] – щелочным.
Определение рН
Для определения значения pH растворов широко используют несколько способов.
1) Водородный показатель можно приблизительно оценивать с помощью индикаторов, точно измерять pH-метром или определять аналитически путём, проведением кислотно-основного титрования.
Для грубой оценки концентрации водородных ионов широко используются кислотно-основные индикаторы – органические вещества-красители, цвет которых зависит от pH среды. К наиболее известным индикаторам принадлежат лакмус, фенолфталеин, метиловый оранжевый (метилоранж) и другие. Индикаторы способны существовать в двух по-разному окрашенных формах – либо в кислотной, либо в основной. Изменение цвета каждого индикатора происходит в своём интервале кислотности, обычно составляющем 1-2 единицы (см. Таблица 1, занятие 2).
Для расширения рабочего интервала измерения pH используют так называемый универсальный индикатор, представляющий собой смесь из нескольких индикаторов. Универсальный индикатор последовательно меняет цвет с красного через жёлтый, зелёный, синий до фиолетового при переходе из кислой области в щелочную. Определения pH индикаторным методом затруднено для мутных или окрашенных растворов.
2) Аналитический объёмный метод – кислотно-основное титрование – также даёт точные результаты определения общей кислотности растворов. Раствор известной концентрации (титрант) по каплям добавляется к исследуемому раствору. При их смешивании протекает химическая реакции. Точка эквивалентности – момент, когда титранта точно хватает, чтобы полностью завершить реакцию, – фиксируется с помощью индикатора. Далее, зная концентрацию и объём добавленного раствора титранта, вычисляется общая кислотность раствора.
Кислотность среды имеет важное значение для множества химических процессов, и возможность протекания или результат той или иной реакции часто зависит от pH среды. Для поддержания определённого значения pH в реакционной системе при проведении лабораторных исследований или на производстве применяют буферные растворы, которые позволяют сохранять практически постоянное значение pH при разбавлении или при добавлении в раствор небольших количеств кислоты или щёлочи.
Водородный показатель pH широко используется для характеристики кислотно-основных свойств различных биологических сред (Табл. 2).
Кислотность реакционной среды особое значение имеет для биохимических реакций, протекающих в живых системах. Концентрация в растворе ионов водорода часто оказывает влияние на физико-химические свойства и биологическую активность белков и нуклеиновых кислот, поэтому для нормального функционирования организма поддержание кислотно-основного гомеостаза является задачей исключительной важности. Динамическое поддержание оптимального pH биологических жидкостей достигается благодаря действию буферных систем.
3) Использование специального прибора – pH-метра – позволяет измерять pH в более широком диапазоне и более точно (до 0,01 единицы pH), чем с помощью индикаторов, отличается удобством и высокой точностью, позволяет измерять pH непрозрачных и цветных растворов и потому широко используется.
С помощью рН-метра измеряют концентрацию ионов водорода (pH) в растворах, питьевой воде, пищевой продукции и сырье, объектах окружающей среды и производственных систем непрерывного контроля технологических процессов, в т. ч. в агрессивных средах.
рН-метр незаменим для аппаратного мониторинга pH растворов разделения урана и плутония, когда требования к корректности показаний аппаратуры без её калибровки чрезвычайно высоки.
Прибор может использоваться в лабораториях стационарных и передвижных, в том числе полевых, а также клинико-диагностических, судебно-медицинских, научно-исследовательских, производственных, в том числе мясо-молочной и хлебопекарной промышленности.
Последнее время pH-метры также широко используются в аквариумных хозяйствах, контроля качества воды в бытовых условиях, земледелия (особенно в гидропонике), а также – для контроля диагностики состояния здоровья.
Таблица 2. Значения рН для некоторых биологических систем и других растворов
| Система (раствор) | рН |
| Двенадцатиперстная кишка | 7,0 – 7,8 |
| Желудочный сок | 1,6 – 1,8 |
| Кровь человека | 7,35 – 7,45 |
| Ликвор | 7,5 |
| Моча | 4,8 – 7,5 |
| Мышечная ткань | 6,7 – 6,8 |
| Панкреатический сок | 8,3 |
| Пот | 4,0 – 8,0 |
| Почки | 6,6 – 6,9 |
| Протоплазма клеток | 6,4 – 7,0 |
| Связки | 7,2 |
| Слёзы | 7,4 |
| Слюна | 6,35 – 6,85 |
| Тонкая кишка | 6,2 – 7,3 |
| Молоко | 6,6 – 6,9 |
| Морская вода | 8,0 |
| Белок куриного яйца | 8,0 |
| Апельсиновый сок | 2,6 – 4,4 |
| Томатный сок | 4,3 |
| Кофе | 5,0 |
| Чай | 5,5 |
Контрольные вопросы
1. Уравнение ионного произведения воды, его анализ.
2. Водородный и гидроксильный показатели среды.
3. Характеристика кислотности сред по величине pH.
4. Биологическое значение водородного показателя.
Типовые задачи
Задача 1. Рассчитать рН раствора соляной кислоты с молярной концентрацией вещества в растворе С(НСl) = 0,001 моль·дм-3.
Дано: Решение:
 С(HCl) = 0,001 моль·дм-3 HCl « H+ + Cl-, т.к. a = 1, то
С(HCl) = 0,001 моль·дм-3 HCl « H+ + Cl-, т.к. a = 1, то
 [H+] = [HCl] = 10-3 моль·дм-3
[H+] = [HCl] = 10-3 моль·дм-3
рН - ? pH = -lg [H+]
pH = -lg10-3 = 3
Ответ: pH = 3.
Задача 2. Рассчитать pH раствора гидроксида калия с молярной концентрацией вещества в растворе C(KOH) = 1,5·10-2 моль·дм-3.
Дано: Решение:
 С(KOH) = 1,5·10-2 моль·дм-3 KOH « K+ + OH-, т.к. a = 1, то
С(KOH) = 1,5·10-2 моль·дм-3 KOH « K+ + OH-, т.к. a = 1, то
 [OH-] = [KOH] = 1,5·10-2 моль·дм-3
[OH-] = [KOH] = 1,5·10-2 моль·дм-3
рН -? pOH = –lg[OH-]
pOH = –lg1,5·10-2 = 1,82
pH + pOH = 14 Þ pH = 14 – pOH
pH = 14 – 1,82 = 12,18.
Ответ:pH = 12,18.
Задача 3. pH желудочного сока равен 1,65. Определить концентрации ионов [H+] и [OH-] в желудочном соке.
Дано: Решение:
 pH = 1,65 pH = –lg [H+]
pH = 1,65 pH = –lg [H+]
 lg [H+] = –pH Þ [H+] = 10–pH
lg [H+] = –pH Þ [H+] = 10–pH
[H+] - ? [H+] = 10–1,65 = 0,0224 моль·дм–3 = 2,24·10–2 моль·дм–3
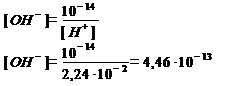 |
[OH-] - ? [H+] · [OH-] = 10–14
Ответ: [H+] = 2,24·10–2 мольˑдм–3; [OH–] = 4,46·10–13 мольˑдм–3 .
Тестовые задания для самоконтроля
Выберите правильный вариант ответа
01. КОНЦЕНТРАЦИЯ ИОНОВ ОН— (МОЛЬ/ДМ3) В РАСТВОРЕ ПРИ рН = 2,00 РАВНА ________МОЛЬ/ДМ3
1) 10–10
2) 10–2
3) 10–12
4) 10–4
02. ЗНАЧЕНИЯ С(ОН—) И С(Н+ ) В РАСТВОРЕ ПРИ рН = 5,0 СОСТАВЛЯЮТ______ МОЛЬ/ДМ3
1) 10–5 и 10 –9
2) 10–4 и 10 –10
3) 10–10 и 10 –4
4) 10–9 и 10 –5
03. ЗНАЧЕНИЯ С(ОН—) И С(Н+ ) В РАСТВОРЕ ПРИ рОН = 6,0 СОСТАВЛЯЮТ ______ МОЛЬ/ДМ3
1) 10–8 и 10–6
2) 10–4 и 10–10
3) 10–6 и 10–8
4) 10–7 и 10–7
04. УКАЖИТЕ рН СОЛЯНОЙ КИСЛОТЫ С КОНЦЕНТРАЦИЕЙ 0,1 МОЛЬ/Л И ВОДНОГО РАСТВОРА ГИДРОКСИДА КАЛИЯ С КОНЦЕНТРАЦИЕЙ 1,0 МОЛЬ/Л, СЧИТАЯ, ЧТО УКАЗАННЫЕ ВЕЩЕСТВА ДИССОЦИИРУЮТ ПОЛНОСТЬЮ
1) 1 и 14
2) 7 и 7
3) 14 и 0
4) 2 и 12
05. В РАСТВОРЕ АЗОТНОЙ КИСЛОТЫ С рН = 2 КОНЦЕНТРАЦИЯ ВЕЩЕСТВА ПРИ α = 100% РАВНА _____ МОЛЬ/ДМ3
1) 0,05
2) 0,1
3) 0,01
4) 0,001
06. рН РАСТВОРА ГИДРОКСИДА БАРИЯ РАВЕН 13, КОНЦЕНТРАЦИЯ ОСНОВАНИЯ В НЕМ ПРИ α =100% РАВНА ______ МОЛЬ/ ДМ3
1) 0,005
2) 0,1
3) 0,05
4) 0,001
07. РАСТВОР, В 500 МЛ КОТОРОГО РАСТВОРЕНО 1,825 г HCl, ИМЕЕТ рН, РАВНЫЙ
1) 2
2) 4
3) 5
4) 1
08. УКАЖИТЕ рН 0,003 МОЛЯРНОГО РАСТВОРА СОЛЯНОЙ КИСЛОТЫ
1) 11,5
2) 3
3) 7
4) 2,5
Контрольные задания
09. Рассчитать рН и рОН слюны, если концентрация ионов водорода в ней составляет
1,78·10–7 моль·дм-3.
10. Физиологическое значение рН крови 7,36. Определить концентрацию ионов [H+] и [OH-] в крови.
11. Рассчитать рН раствора соляной кислоты с концентрацией 0,03 моль/дм3 и водного раствора гидроксида калия с концентрацией 0,12 моль/дм3, считая, что указанные вещества диссоциируют полностью.
12. Определите рН кишечного сока, если концентрация гидроксид- анионов ОН- в составе кишечного сока составляет 2,3·10-6 моль·дм-3.
Литература
1. Общая химия. Биофизическая химия. Химия биогенных элементов: Учеб. для вузов / Ю. А. Ершов, В.А. Попков, А.С. Берлянд и др.; Под ред. Ю.А. Ершова. – 5-е изд., стер. – М.: Высш.шк., 2005. – С. 66 – 76, 101 – 107.
2. Практикум по общей химии. Биофизическая химия. Химия биогенных элементов: Учеб. пособие для студентов медицинских спец. вузов / Ю.А. Ершов, А.М. Кононов, С.А. Пузаков и др.; Под ред. Ю.А. Ершова, В.А. Попкова. – М. : Высш. шк., 2008. – С.45-50.
1.8. Буферные системы
Свойством всех живых организмов является постоянство рН биологических жидкостей, тканей и органов. Это постоянство поддерживается их буферными системами и необходимо для обеспечения нормальной деятельности ферментов, регулирования осмотического давления и других показателей.
Знания по теме «Буферные «системы» необходимы для понимания механизма их действия, количественной оценки способности буферных систем связывать посторонние кислоты и щелочи, понимания их взаимосвязи и роли в поддержании кислотно-основного гомеостаза.
Кроме того, важно уметь готовить буферные растворы для последующего использования их в различных медико-биологических, химических и клинических исследованиях.
Буферными называют системы, состоящие из двух сопряженных компонентов, способных до определенного предела противодействовать изменению рН среды при добавлении к ним небольших количеств кислоты и щелочи, а также при разбавлении раствора или концентрировании.
Способность буферных систем сохранять постоянство pH называется буферным действием.
По составу, с точки зрения протонной теории, буферные системы делят на кислые и основные.
Кислые буферные системы состоят из слабой кислоты и сопряженного с ней избытка сильного основания, создаваемого солью этой кислоты.
Например: Ацетатная буферная система – кислая буферная система, состоит из:
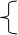 СН3СООН – слабая кислота;
СН3СООН – слабая кислота;
СН3СООNa – растворимая соль (содержит сопряженное сильное основание СН3СОО- ).
Аммиачная буферная система – основная буферная система, состоит из:
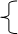 NН4ОН – слабое основание;
NН4ОН – слабое основание;
NН4Сl –растворимая соль (содержит сопряженную сильную кислоту NН4+).
Буферные системы в растворенном состоянии образуют буферные растворы.
Буферные растворы, в отличие от буферных систем, могут быть многокомпонентными.
Кровь относят к буферным растворам.
Водородный показатель среды буферного раствора рассчитывают по уравнению Гендерсона-Гассельбаха:
pH = pKa + lg[соль]/[кислота]
pH - водородный показатель среды буферного раствора,
pKa – показатель константы кислотности слабой кислоты,
[соль]/[кислота]– количества соли и кислоты в момент равновесия; буферное соотношение.
В рабочем виде: 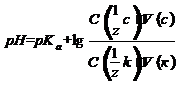
- C (1/z с), C (1/z к) – исходные молярные концентрации эквивалентов соли и кислоты, моль·дм-3;
- V (с), V (к) – объемы растворов соли и кислоты соответственно, см3.
Величину, характеризующую способность буферной системы противодействовать смещению реакции среды при добавлении кислот и щелочей, называют буферной емкостью (B). Буферную ёмкость можно определить по кислоте или по основанию.
Буферная ёмкость показывает сколько моль-эквивалентов сильной кислоты или щелочи следует добавить к 1 дм3 буферного раствора, чтобы изменить его рН на единицу.
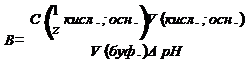 |
B – буферная ёмкость, моль дм-3;
C(1/z кисл.; осн.) – молярная концентрация эквивалента добавляемой кислоты или основания;
V(кисл.; осн.) – объем раствора добавляемой кислоты или основания, см3;
∆pH – изменение pH;
V (буф.)- объем буферного раствора, см3.
Для сохранения оптимальных условий обменных процессов необходимо постоянство pH внутренних сред организма. Постоянство кислотности сред, наряду с физиологическими механизмами поддерживается буферными системами организма.
Контрольные вопросы
1. Буферные системы, их состав, свойства, классификация. Механизм буферного действия. Буферные растворы
2. Уравнение кислых буферных систем Гендерсона-Гассельбаха, его вывод и анализ. Зона буферного действия.
3. Буферная емкость. Факторы, влияющие на величину буферной емкости.
4. Биологическая роль буферных систем. Буферные системы крови: гемоглобиновая, оксигемоглобиновая, белковая, водородкарбонатная, фосфатная, эфиры глюкозы и фосфорной кислоты различной степени замещенности.
5. Роль водородкарбонатной буферной системы в поддержании постоянства рН крови. Ацидоз. Алкалоз. Щелочной резерв крови.
Типовые задачи
Задача 1. Рассчитайте рН ацетатного буферного раствора, приготовленного из 80 мл 0,1 н раствора СН3СООН и 20 мл 0,1 н раствора СН3СООNa. КД (СН3СООН) = 1,74 · 10– 5.
| Дано: | Решение: |
| С (СН3СООН) = 0,1 н | 1. Находим рКкислоты: рКкислоты = – lgКД = – lg 1,74 · 10– 5 = 4,76 |
| Vр (СН3СООН) = 80 мл = 0,08 л | |
| С (СН3СООNa) = 0,1 н | 2. Находим рН ацетатного буферного раствора: |
| Vр (СН3СООNa) = 20 мл | |
| КД (СН3СООН) = 1,74 · 10– 5 | CC · VC 0,02 · 0,1 рН = рКкислоты + lg ----------- = 4,76 + lg -------------- = 4,16 CК · VК 0,08 · 0,1 |
| -------------------------------------- | |
| рН = ? | |
| Ответ: рН = 4,16 |
Задача 2. Рассчитать рН оксалатной буферной системы, состоящей из100 см3 раствора щавелевой кислоты с концентрацией С(1/2 Н2С2О4)=0,5 моль·дм -3 и 150 см3 растворы оксалата натрия с концентрацией С(1/2 Na2C2O4)=0,25 моль·дм-3,если КД (Н2С2О4)=5,6·10-2.
 Дано: Решение:
Дано: Решение:
V (H2C2O4) = 100см3 рН=рКД+lgC(1/2H2C2O4)·V(Na2C2O4)/C(1/2H2C2O4)·V(H2C2O4)
С(Na2C2O4) = 0,5 моль·дм– 3 pКд = – lgКд
V(Na2C2O4) = 150 см3 pКд = – lg 5,6·10-2 = 1,25
С(1/2Na2C2O4) = 0,25 моль·дм– 3 рН = 1,25 + lg(0,25·150)/(0,5·100 )= 1,125.
КД (H2C2O4) = 5,6·10– 2
рН-? Ответ: рН = 1,125.
Задача 2. Рассчитайте объемы (см3) 0,1М СН3СООН и 0,1 М СН3СООNa, необходимые для приготовления 100 см3 буферного раствора с рН = 4,0. рК (СН3СООН) = 4,76
| Дано: | Решение: |
| C(СН3СООН) = 0,1моль/дм3 | 1. По уравнению Гендерсона-Гассельбаха : |
| C(СН3СООNa) = 0,1моль/дм3 | рН = рК + lg (Cс·Vс)/(Cк·Vк) |
| Vбуф. = 100 см3 | lg(Cс·Vс)/(Cк·Vк) = pH – pK |
| рН = 4,0 | 2. Подставим данные: |
| рК (СН3СООН) = 4,76 | lg(0,1·Vс)/(0,1·Vк) = 4 – 4,76 = –0,76 |
| V(СН3СООН) = ? V(СН3СООNa) = ? | 3. Vс + Vк = 100 см3 lg Vс/(100 –Vc) = –0,76 |
| Vс/(100 –Vc) = 10 -0,76 = 0,174 Vc = 14,84 см3 Vк = 100 – 14,84 = 85,16 см3 | |
| Ответ: V(СН3СООН) = 85,16 см3; V(СН3СООNa) = 14,84 см3 |
Задача 3. Рассчитайте рН фосфатного буфера, состоящего из 100 см3 0,01 моль/дм3 NaH2PO4 и 20 см3 0,1 моль/дм3 Na2HPO4. Как изменится рН при добавлении к этой смеси 30 мл раствора NaOH с молярной концентрацией С(NaОН) = 0,02 моль/дм3?
КД (Н2РО-4)=1,6·10– 7.
| Дано: | Решение: |
| C(NaH2PO4) = 0,01моль/дм3 | 1. По уравнению Гендерсона-Гассельбаха : |
| C(Na2HPO4) = 0,1моль/дм3 | рН = рК(H2PO4–) + lg (Cс·Vс)/(Cк·Vк) |
| V(NaH2PO4) = 100 см3 | pK (H2PO4–) = – lg1,6·10– 7 = 6,8 |
| V(Na2HPO4) = 20 см3 | 2. Подставим данные: |
| V(NaOН) = 30 см3 | pH = 6,8 + lg(0,1·20)/(0,01·100) = 6,8 + lg2 = 7,1 |
| C(NaОН) = 0,02моль/дм3 | 3. Роль соли (основания) в буфере выполняет Na2HPO4, а роль кислоты – NaH2PO4 H2PO4– + OH– ↔ HPO42– + H2O; HPO42– + Н+ ↔ H2PO4– кислота основание |
| КД (Н2РО-4)=1,6·10-7 рН = ? | |
| При добавлении NaOH в буфере уменьшится количество кислоты NaH2PO4 и увеличится количество соли Na2HPO4. Расчет ведем в миллимолях(ммоль) n(NaOH) = 30 мл · 0,02 = 0,6ммоль | |
| рН = 6,8 + lg(2+0,6)/(1-0,6) = 6,8 + lg(2,6/0,4) = 7,615 | |
| Ответ: рН = 7,615 |
Задача 4. Рассчитайте буферную емкость по кислоте, если при добавлении к 100 см3 гидрокарбонатного буфера с рН = 6,5 10 см3 раствора НСl с молярной концентрацией эквивалента С(НСl) = 0,1 моль/дм3 изменился до 6,3.
| Дано: | Решение: |
| C(НСl) = 0,1 моль/дм3 | 1. По уравнению: |
| V(НСl) = 10 см3 | Bк = V(HCI)·С(НСl) /Vбуф. ·ΔpH |
| Vбуф. = 100 см3 | Bк = 10 · 0,1 / 100 · (6,5 – 6,3) = 0,05 моль/дм3 |
| рН1 = 6,5 | |
| рН2 = 6,3 | |
| Вк = ? | |
| Ответ: Bк = 0,05 моль/дм3 |
Тестовые задания для самоконтроля
Выберите правильный вариант ответа
01. ВЫБЕРИТЕ БУФЕРНУЮ СИСТЕМУ
1) KH2PO4/Na2HPO4
2) HCl / NaCl
3) H2SO4/ Na2SO4
4) NaHSO4/ Na2SO4
02. УКАЖИТЕ КАК НАЗЫВАЕТСЯ СДВИГ РЕАКЦИИ СРЕДЫ ОРГАНИЗМА В ЩЕЛОЧНУЮ СТОРОНУ
1) ацидоз
2) алкалоз
3) алкалемия
4) изогидрия
Дополните высказывание
03. СПОСОБНОСТЬ БУФЕРНЫХ СИСТЕМ СОХРАНЯТЬ ПОСТОЯНСТВО ВОДОРОДНОГО ПОКАЗАТЕЛЯ СРЕДЫ НАЗЫВАЕТСЯ ___________________.
04. СИСТЕМА, СОСТОЯЩАЯ ИЗ СЛАБОГО ОСНОВАНИЯ И СОПРЯЖЕННОГО С НИМ ИЗБЫТКА КИСЛОТЫ, СОЗДАВАЕМОГО СОЛЬЮ ЭТОГО ОСНОВАНИЯ. НАЗЫВАЕТСЯ____________.
05. ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ СРЕДЫ БУФЕРНОГО РАСТВОРА ЗАВИСИТ ОТ ПРИРОДЫ КОМПОНЕНТОВ БУФЕРА, ТЕМПЕРАТУРЫ И ВЕЛИЧИНЫ____________.
06. ИНТЕРВАЛ ЗНАЧЕНИЙ ВОДОРОДНОГО ПОКАЗАТЕЛЯ СРЕДЫ, В ПРЕДЕЛАХ КОТОРОГО БУФЕРНАЯ СИСТЕМА СОХРАНЯЕТ СВОИ СВОЙСТВА, ЯВЛЯЕТСЯ _____________________
Контрольные задания
07.Рассчитать рН для пяти буферных систем, состоящих из уксусной кислоты и ацетата натрия, учитывая, что С (СН3СООН) = С (СН3СООNa) = 0,1 моль/дм3, а соотношение объемов буферных компонентов [соль]/[кислота] составляет: 1/9; 3/7; 5/5; 7/3; 9/1.
КД (СН3СООН) = 1,74 · 10– 5.
08. Рассчитать рН буферного раствора, состоящего из 80 см3 раствора NaH2PO4 с концентрацией равной 0,12 моль/дм3 и 30 см3 раствора Na2HPO4 с концентрацией 0,14 моль/дм3. КД (Н2РО4– ) = 6,2 · 10– 8.
09. К 10 см3 сыворотки крови с рН = 7,34 прибавили 1 см3 раствора хлороводородной кислоты с С(НСl) = 0,05 моль/дм3, что привело к снижению рН до 7,29. Определить буферную емкость крови по кислоте.
Литература
- Общая химия. Биофизическая химия. Химия биогенных элементов: Учеб. для вузов / Ю. А. Ершов, В.А. Попков, А.С. Берлянд и др.; Под ред. Ю.А. Ершова. – 5-е изд., стер. – М.: Высш.шк., 2005. – С. 108 – 119.
2. Практикум по общей химии. Биофизическая химия. Химия биогенных элементов: Учеб. пособие для студентов медицинских спец. вузов / Ю.А. Ершов, А.М. Кононов, С.А. Пузаков и др.; Под ред. Ю.А. Ершова, В.А. Попкова. – М. : Высш. шк., 2008. – С.42-45.
