Водородный показатель для различных сред растворов
План
1. Электролиты и неэлектролиты.
2. Теория электролитической диссоциации (ТЭД) С.А.Аррениуса.
3. Механизм электролитической диссоциации электролитов с ионной и ковалентной полярной связью.
4. Степень диссоциации.
5. Кислоты, основания, амфотерные гидроксиды, соли с точки зрения ТЭД.
6. Значение электролитов для живых организмов.
7. Диссоциация воды. Ионное произведение воды. Водородный показатель. Среды водных растворов электролитов. Индикаторы.
8. Реакции ионного обмена и условия их протекания.
По способности проводить электрический ток в водном растворе или расплаве все вещества можно разделить на электролиты и неэлектролиты.
Электролиты – это вещества, растворы или расплавы которых проводят электрический ток; в электролитах (кислоты, соли, щелочи) имеются ионные или полярные ковалентные связи.
Неэлектролиты – это вещества, растворы или расплавы которых не проводят электрический ток; в молекулах неэлектролитов (органические вещества, газы, вода) связи ковалентные неполярные или малополярные.
Для объяснения электропроводности растворов и расплавов электролитов Аррениус в 1887 г. создалтеорию электролитической диссоциации, основные положения которой звучат следующим образом.
1. Молекулы электролитов в растворе или расплаве подвергаются диссоциации (распадаются на ионы). Процесс распада молекул электролитов на ионы в растворе или расплаве называется электролитической диссоциацией. Ионы – это частицы, имеющие заряд. Положительно заряженные ионы – катионы, отрицательно заряженные – анионы. Свойства ионов отличаются от свойств соответствующих нейтральных атомов, что объясняется разным электронным строением этих частиц.
2. В растворе или расплаве ионы движутся хаотически. Однако при пропускании через раствор или расплав электрического тока движение ионов становится упорядоченным: катионы движутся к катоду (отрицательно заряженному электроду), а анионы – к аноду (положительно заряженному электроду).
3. Диссоциация – обратимый процесс. Одновременно с диссоциацией идет ассоциация – процесс образования молекул из ионов.
4. Общая сумма зарядов катионов в растворе или расплаве равна общей сумме зарядов анионов и противоположна по знаку; раствор в целом электронейтрален.
Главной причиной диссоциации в растворах с полярным растворителем является сольватация ионов (в случае водных растворов – гидратация). Диссоциация ионных соединений в водном растворе протекает полностью (KCl, LiNO3, Ba(OH)2 и др.). Электролиты с полярной ковалентной связью могут диссоциировать частично или полностью в зависимости от величины полярности связи (H2SO4, HNO3, HI и др.). В водном растворе образуются гидратированные ионы, но для простоты записи в уравнениях изображаются ионы без молекул воды:
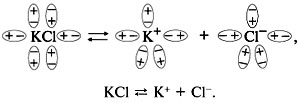
Одни электролиты диссоциируют полностью, другие – частично. Для характеристики диссоциации вводится понятие степень электролитической диссоциации α. Величина α показывает отношение числа диссоциировавших молекул n к числу растворенных молекул N электролита в растворе:
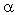 = n/N.
= n/N.
Степень диссоциации увеличивается при разбавлении раствора и при повышении температуры раствора. В зависимости от степени диссоциации электролиты делятся на сильные, средней силы и слабые. Сильные электролиты практически полностью диссоциируют в растворе, их степень диссоциации больше 30% и стремится к 100%. К средним электролитам относятся электролиты, степень диссоциации которых колеблется в пределах от 3% до 30%. Степень диссоциации слабых электролитов меньше 3%. К сильным электролитам относятся соли, сильные кислоты, щелочи. К слабым – слабые кислоты, нерастворимые основания, гидроксид аммония, вода.
С точки зрения теории электролитической диссоциации можно дать определения веществам разных классов.
Кислоты – это электролиты, образующие при диссоциации катионы водорода и анионы кислотного остатка. Число ступеней диссоциации зависит от основности кислоты, например:
HCl 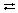 H+ + Cl–,
H+ + Cl–,
H2CO3 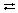 H+ + HCO3–
H+ + HCO3– 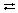 2H+ + CO32–.
2H+ + CO32–.
Основания – это электролиты, диссоциирующие на катионы металла и анионы гидроксигрупп. Число ступеней диссоциации зависит от кислотности основания, например:
NaOH 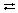 Na+ + 2OH–,
Na+ + 2OH–,
Ca(OH)2 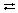 CaOH+ + OH–
CaOH+ + OH– 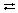 Ca2+ + 2OH–.
Ca2+ + 2OH–.
Амфотерные гидроксиды – это слабые электролиты, которые при диссоциации образуют как катионы водорода, так и анионы гидроксигруппы, например:
Zn(OH)2 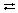 ZnOH+ + OH–
ZnOH+ + OH– 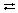 Zn2+ + 2OH–,
Zn2+ + 2OH–,
H2ZnO2 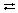 H+ + HZnO2–
H+ + HZnO2– 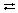 2H+ + ZnO22–.
2H+ + ZnO22–.
Средние соли – это электролиты, диссоциирующие на катионы металла и анионы кислотного остатка, например:
Na2SO4 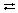 2Na+ + SO42–.
2Na+ + SO42–.
Кислые соли – это электролиты, диссоциирующие на катионы металла и сложные анионы, в состав которых входят атомы водорода и кислотный остаток, например:
NaНСO3 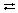 Na+ + НСO3–.
Na+ + НСO3–.
Основные соли – это электролиты, диссоциирующие на анионы кислотного остатка и сложные катионы, состоящие из атомов металла и гидроксигрупп, например:
Сu(OН)Сl 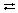 CuОН+ + Сl–.
CuОН+ + Сl–.
Комплексные соли – это электролиты, образующие при диссоциации сложные комплексные ионы, которые довольно устойчивы в водных растворах, например:
K3[Fe(CN)6] 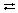 3K+ + [Fe(CN)6]3–.
3K+ + [Fe(CN)6]3–.
Электролиты являются составной частью жидкостей и тканей живых организмов. Для нормального протекания физиологических и биохимических процессов необходимы катионы натрия, калия, кальция, магния, водорода, анионы хлора, сульфат-ионы, гидрокарбонат-ионы, гидроксид-ионы и др. Концентрации этих ионов в организме человека различны. Так, например, концентрации ионов натрия и хлора весьма значительны и ежедневно пополняются. Концентрации ионов водорода и гидроксид-ионов очень малы, но играют большую роль в жизненных процессах, способствуя нормальному функционированию ферментов, обмену веществ, перевариванию пищи и т.д.
Диссоциация воды.
Водородный показатель
Вода является слабым амфотерным электролитом. Уравнение диссоциации воды имеет вид:
Н2O 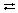 Н+ + ОН–
Н+ + ОН–
или
2Н2O 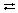 Н3О+ + ОН–.
Н3О+ + ОН–.
Концентрация протонов и гидроксид-ионов в воде одинакова и составляет 10–7 моль/л при 25 °С.
Произведение концентраций ионов водорода и гидроксид-ионов называется ионным произведением воды и при 25 °С составляет 10–14.
Среду любого водного раствора можно охарактеризовать концентрацией ионов Н+ или ОН–. Различают нейтральную, кислую и щелочную среды растворов.
В нейтральной среде раствора:
[H+] = [OH–] = 10–7 моль/л,
в кислой среде раствора:
[H+] > [OH–], т.е. [H+] > 10–7 моль/л,
в щелочной среде раствора:
[OH–] > [H+], т.е. [OH–] > 10–7 моль/л.
Для характеристики среды раствора удобно пользоваться водородным показателем рН (табл. 1). Водородный показатель – это отрицательный десятичный логарифм концентрации ионов водорода:
рН = –lg[H+].
Таблица 1
Водородный показатель для различных сред растворов
| Характеристика раствора | Среда раствора | ||
| кислая | нейтральная | щелочная | |
| Kонцентрация ионов Н+ (моль/л) | [H+] > 10–7 | [H+] = [OH–] = 10–7 | [H+] < 10–7 |
| Водородный показатель (рН) | pH < 7 | pH = 7 | pH > 7 |
В кислой среде раствора рН < 7, в нейтральной среде рН = 7, в щелочной рН > 7. Чем меньше рН, тем больше кислотность раствора. При значениях рН > 7 говорят о щелочности раствора.
Существуют различные методы определения рН раствора. Качественно характер среды раствора определяют с помощью индикаторов. Индикаторы – вещества, которые обратимо изменяют свой цвет в зависимости от среды раствора. На практике чаще всего применяют лакмус, метиловый оранжевый, фенолфталеин и универсальный индикатор (табл. 2).
Таблица 2
