Составить ионно-молекулярное и молекулярное уравнения гидролиза карбоната калия. Вычислить константу, степень и рН гидролиза соли в 0,01 М растворе.
Дано: 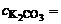 0,01M 0,01M | Решение K2CO3 диссоциирует в растворе: K2CO3 → 2К+ + СО32- K2CO3 KOH + H2CO3 cильн. cлаб. |
| Kг – ? pH- ? h – ? |
Сокращенное ионно-молекулярное уравнение гидролиза
| |||
| |||


 СО32- + НОН <=> – + , рН > 7, среда щелочная.
СО32- + НОН <=> – + , рН > 7, среда щелочная.
Молекулярное уравнение гидролиза:
K2CO3 + H2O = KHCO3 + KOH
Kг = 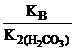 ,
,
 (таблица)
(таблица)
Kг = 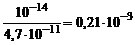 .
.
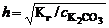 ;
; 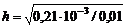 = 0,14;
= 0,14;
pH + рОН = 14.
Так как среда щелочная, определяем 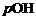 ;
;
pОН= –1/2∙lgKг – 1/2 ∙ lg 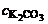 =
=
= 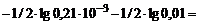 (–1/2lg0,21) + (–1/2lg10-3) +
(–1/2lg0,21) + (–1/2lg10-3) +
+ (–1/2lg10-2) = 0,34 + 1,5 + 1 = 2,84.
рН = 14 – рОН; рН = 14 – 2,84 = 11,16.
Ответ: 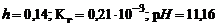
2. Рассчитать при температуре 300 К константу, степень и рН гидролиза NH4NO3 в 1 М растворе, используя значения термодинамических характеристик реакции гидролиза соли. Написать ионно-молекулярное и молекулярное уравнение гидролиза этой соли.
∆гНо(298 К) = 51,135 кДж;
∆гSo(298 K) = -4,67 Дж/К.
Дано: ∆гНо(298 К) = 51,135 кДж ∆гSo(298 K) = –4,67 Дж/К 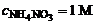 T = 300 K T = 300 K | Решение NH4 NO3 – диссоциирует в растворе: NH4 NO3 → NH4+ + NO3-. NH4NO3 NH4OH + HNO3 слаб. сильн. Сокращенное ионно-молекулярное уравнение гидролиза |
| Kг – ? h – ? pH – ? |
|

 NH4+ + HOH<=>NH4OH + , , pH < 7, среда кислая.
NH4+ + HOH<=>NH4OH + , , pH < 7, среда кислая.
 |
Молекулярное уравнение гидролиза
NH4 NO3 + H2O <=> NH4OH + HNO3.
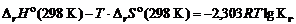 ;
;
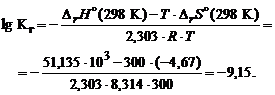
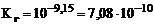 .
.
Так как среда кислая, то определяем рН:
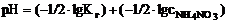 ;
;
рН = –1/2 ∙ (–9,15) – 1/2 ∙ lg1 = 4,57;
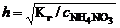 =7,08·10–10/1 22,66·10–5.
=7,08·10–10/1 22,66·10–5.
Ответ: 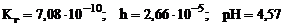 .
.
3. Какая из двух солей, ZnCl2 или СuCl2, при равных концентрациях в большей степени подвергается гидролизу? Ответ мотивировать расчетом отношения степеней гидролиза обеих солей. Составить ионно-молекулярные и молекулярные уравнения гидролиза этих солей.
Дано: 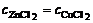 | Решение 1. ZnCl2 диссоциирует в растворе: ZnCl2 → Zn2+ + 2Cl- |
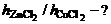 |
ZnCl2
Zn(OH)2 + HCl
слаб. сильн.
Сокращенное ионно-молекулярное уравнение гидролиза
|
|
Zn2+ + HOH < = > + , рН < 7 – среда кислая.
 |
Молекулярное уравнение гидролиза
ZnCl2 + H2O < = > ZnOHCl + HCl.
2. СuCl2 диссоциирует в растворе:
CuCl2 → Cu2+ + 2Cl-
CuCl2
Cu(OH)2 + HCl
слаб. сильн.
Сокращенное ионно-молекулярное уравнение гидролиза
|
|
 Cu2+ + HOH < = > + , рН < 7 – среда кислая.
Cu2+ + HOH < = > + , рН < 7 – среда кислая.
Молекулярное уравнение гидролиза:
CuCl2 + H2O < = > CuOHCl + HCl.
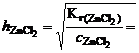
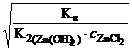 ;
;
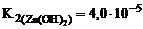 .
.
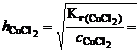
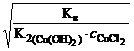 ;
;
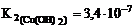 .
.
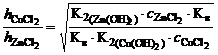 =
= 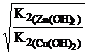 =
=
= 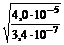 = 10,85.
= 10,85.
Ответ: степень гидролиза CuCl2 в 10,85 раз больше степени гидролиза ZnCl2.
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ
РЕАКЦИИ
УРОВЕНЬ А
1. Расположить перечисленные вещества в порядке уменьшения степени окисления хрома:
Cr2O3 – CrCl2 – K2Cr2O7.
Ответ: алгебраическая сумма степеней окисления отдельных атомов, образующих молекулу, с учетом стехиометрических индексов равна нулю.
Cr Х Сl 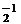 Сr
Сr 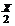 O
O 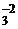
Х + (–1) ∙ 2 = 0 Х ∙ 2 + (–2) ∙ 3 = 0
Х = +2 Х = +3
K 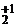 Cr
Cr 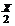 O
O 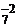
(+1) ∙ 2 + Х ∙ 2 + (–2) · 7 = 0
Х = +6
K2Cr 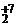 O7 – Cr
O7 – Cr 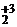 O3 – Cr+2Cl2.
O3 – Cr+2Cl2.
2. Составить уравнения для следующих процессов и назвать их:
а) Ni0 → Ni+2
б) 2I- → I2
в) Cu+2 → Cu0
Ответ:
а) Ni0 – 2е = Ni+2 – процесс окисления;
б) 2I 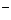 – 2е = I20 – процесс окисления;
– 2е = I20 – процесс окисления;
в) Cu+2 + 2е = Cu0 – процесс восстановления.
3. Какие свойства (окислительные или восстановительные) проявляют PbO2 ; H2S; KMnO4 ?
Ответ: окислители – атомы, молекулы или ионы, присоединяющие электроны, а восстановители – отдающие электроны. Поэтому чем выше степень степень окисления иона, тем сильнее он проявляет окислительные свойства, а чем ниже степень окисления иона – тем сильнее его восстановительные свойства.
Pb+4O2 – окислитель H2S-2 – восстановитель
KMn+7 O4 – окислитель
УРОВЕНЬ В
Закончить уравнения реакций и уравнять их используя метод электронного баланса. Указать окислитель и восстановитель:
а) Pb + HNO3 конц →
б) S + HNO3 конц →
в) P + H2SO4 конц →
г) Mg + H2SO4 конц →
а) Металл + НNО3(конц) → соль + оксид азота + Н2О.
Формула оксида азота зависит от активности металла: N2O выделится, если в реакцию вступает активный металл (стоящий в ряду стандартных электродных потенциалов в интервале Li...Al);
NО выделится, если в реакцию вступает металл средней активности (Mn–Рb);
NO2 выделится, если в реакцию вступает малоактивный металл (стоящий в ряду стандартных электродных потенциалов после водорода).
| Дано: а) Pb + HNO3 конц → S + HNO3 конц → б) P + H2SO4 конц → Mg + H2SO4 конц → | Решение а) Pb0 + HN+5O3 конц = восст. окисл. = Pb+2(NO3)2 + N+2O + H2O   НОК ДМ восстановитель Pb0 – 2ē = Pb+2 3 окислитель N+5 + 3ē = N+2 2 НОК ДМ восстановитель Pb0 – 2ē = Pb+2 3 окислитель N+5 + 3ē = N+2 2  3Pb0 + 2N+5 = 3Pb+2 + 2N+2 3Pb0 + 2N+5 = 3Pb+2 + 2N+2 |
| Уравнять реакции и указать окислитель и восстановитель |
Переносим полученные коэффициенты в молекулярное урав-нение:



 3Pb0 + 2HN+5O3(конц) = 3Pb+2(N+5O3)2 + N+2O + H2O.
3Pb0 + 2HN+5O3(конц) = 3Pb+2(N+5O3)2 + N+2O + H2O.
 |
Поскольку азотная кислота расходуется не только на получение 2 моль NO, но и на получение 3 моль Pb(NO3)2, в которых содержится 6NO 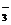 со степенью окисления N+5, то для протекания этого процесса необходимо дополнительно 6 моль HNO3:
со степенью окисления N+5, то для протекания этого процесса необходимо дополнительно 6 моль HNO3:
 |


 6HNO3 (конц) + 3Pb0 + 2HNO3(конц) = 3Pb(NO3)2 + 2NO + H2O
6HNO3 (конц) + 3Pb0 + 2HNO3(конц) = 3Pb(NO3)2 + 2NO + H2O
 |
Суммируем число моль HNO3 и уравниваем количество водорода и кислорода (4Н2О):
3Рb + 8HNO3(конц) = 3Pb(NO3)2 + 2NO + 4Н2О.
б) Неметалл + HNO3(конц) → кислота, в которой неметалл проявляет высшую степень окисления + NO2 + (Н2О):
B → H3B+3O3; P → H3P+5O4; S → H2S+6O4; Se → H2Se+6O4;
Si → H2Si+4O3; C → H2C+4O3; As → H3As+5O4.
Решение
So + HN+5O3(конц) = Н2S+6O4 + N+4O2 + H2O
восст. окисл.

 НОК ДМ
НОК ДМ
восст-ль Sº – 6ē = S+6 1
окисл-ль N+5 + ē = N+4 6
 |
Sº + 6N+5 = S+6 + 6N+4
S + 6HNO3(конц) = Н2SO4 + 6NO2 + 2H2O.
в) Неметалл + H2SO4(конц) → кислота, в которой неметалл проявляет высшую степень окисления + SO2 +(Н2O); см. пример б).
Решение
P0 + H2S+6O4(конц) = Н3Р+5О4 + S+4O2 + H2O
восст. окисл.

 НОК ДМ
НОК ДМ
восст-ль P0 – 5ē = P+5 2
окисл-ль S+6 + 2ē = S+4 5
 |
2Р0 + 5S+6 = 2P+5 + 5S+4
2P + 5H2SO4(конц) = 2Н3РО4 + 5SO2 + 2H2O.
г) Металл + H2SO4(конц) → соль + (H2S, S, SO2)
(в зависимости от активности металла) + Н2О.
H2S выделится, если в реакцию вступает активный металл
(Li–Al),
S выделится, если в реакцию вступает металл средней активности (Mn–Рb),
SO2выделится, если в реакцию вступает малоактивный металл (стоящий в ряду стандартных электродных потенциалов после водорода).
Решение
Mg0 + H2S+6O4(конц) = Mg+2SO4 + H2S-2 + H2O.
восст. oкисл.
НОК ДМ

 восст-ль Mg0 – 2ē = Mg+2 4
восст-ль Mg0 – 2ē = Mg+2 4
окисл-ль S+6 + 8ē = S-2 1
 |
4Mg0 + S+6 = 4Mg+2 + S-2
Аналогично примеру (а) уравниваем реакцию:
 |
4H2SO4(конц) + 4Mg + H2SO4(конц) = 4MgSО4 + H2S + 4H2O

4Mg + 5H2SO4(конц) = 4MgSО4 + H2S + 4H2O.
УРОВЕНЬ С
