Двухосновные карбоновые кислоты
ПолучениеАлифатические двухосновные карбоновые кислоты синтези-руют методами, используемыми для синтеза одноосновных алифатических кислот, но с использованием соответствующих бифункциональных соединений.
Гидролиз дицианопроизводных или цианкислот:
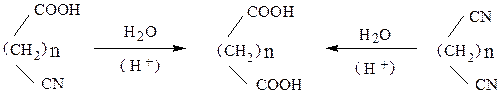
Окисление диолов, гидроксиальдегидов, гидроксикислот, диальдегидов, альдегидокислот:
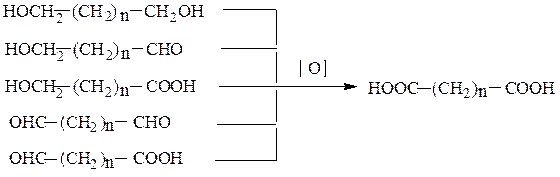
Широко распространенную в природе щавелевую кислоту в промышлен-ности получают пиролизом формиата натрия:
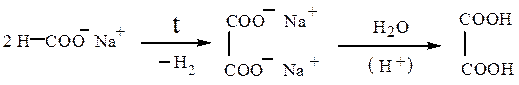
Химические свойства
Дикарбоновые кислоты проявляют все свойства монокарбоновых кислот, образуя соли, галогенангидриды, ангидриды, сложные эфиры, амиды. Отличия химических свойств дикарбоновых кислот от свойств одноосновных кислот заключаются в следующем:
Двухступенчатая диссоциация кислот в отличие от одной ступени:
первая ступень: 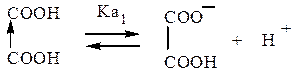
вторая ступень: 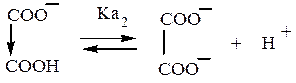
Поскольку группа –СООН имеет –I-эффект, а группа –СОО– – +I-эффект, то константа диссоциации по первой ступени выше, а по второй – ниже, чем у соответствующей одноосновной кислоты. Для щавелевой кислоты:
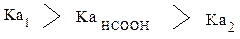
Образование моно- или дизамещенных производных с получением двух или трех видов сложных эфиров:
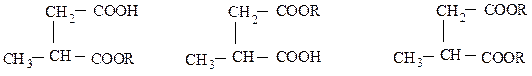
Образование смешанных производных:
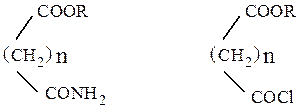
Превращение дикарбоновых кислот типа 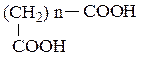 при
при
нагревании в зависимости от величины n приводит к следующим продуктам реакций:
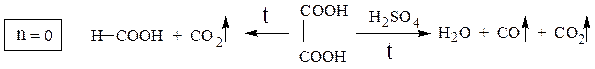
щавелевая кислота
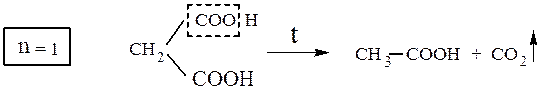
малоновая кислота
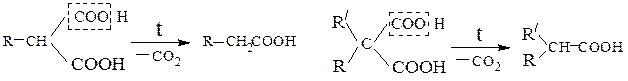
алкилмалоновая кислота диалкилмалоновая кислота
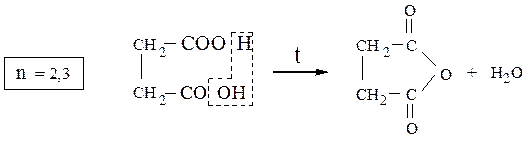
янтарная кислота янтарный ангидрид
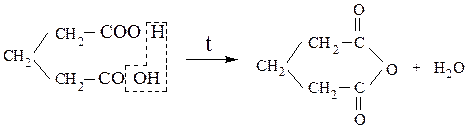
глутаровая кислота глутаровый ангидрид
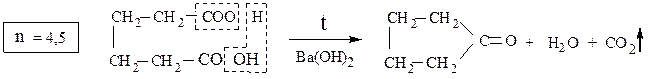 адипиновая кислота циклопентанон
адипиновая кислота циклопентанон
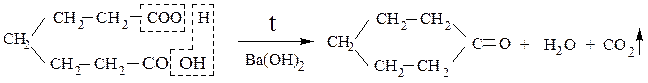 себациновая кислота циклогексанон
себациновая кислота циклогексанон
Важнейшим соединением является малоновый эфир, который используется в синтезах витаминов В1, В6, аминокислот, гетероциклических соединений и различных карбоновых кислот.
Синтезы на основе малонового эфира основаны на легкой способности протона отщепляться от атомов водорода метиленовой группы под действием щелочных реагентов. При действии на малоновый эфир металлического натрия или этилата натрия получается натриймалоновый эфир, который далее взаимодействует с галогенсодержащими соединениями. Образующийся анион стабилизируется за счет делокализации заряда:
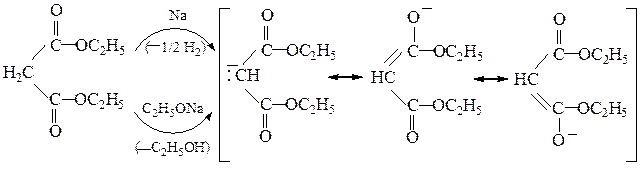
Натриймалоновый эфир вступает в реакцию С-алкилирования при действии галогеналканов:
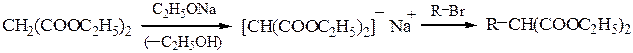
Алкилмалоновый эфир также способен металлироваться и алкилироваться:
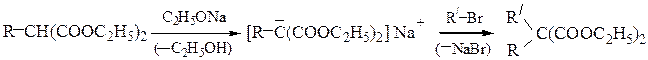
При омылении (взаимодействие с водой) моно- или диалкилмалонового эфира образуются свободные кислоты, которые при нагревании легко декарбоксилируются:
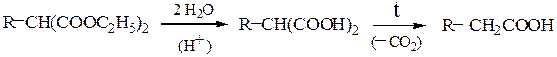
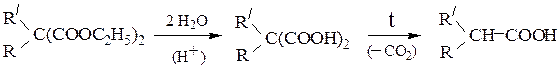
Таким образом, с использованием малонового эфира можно синтезировать моно- и диалкилуксусные кислоты. Важным является подбор галоген-содержащих соединений в зависимости от конечного продукта. При планировании синтеза кислоты, необходимо выделить основу 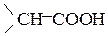 , остающуюся от малонового эфира и представить, сколько раз (1 или 2) необходимо алкилировать малоновый эфир и какими галогенопроизводными.
, остающуюся от малонового эфира и представить, сколько раз (1 или 2) необходимо алкилировать малоновый эфир и какими галогенопроизводными.
Получение дикарбоновых кислот:
· Янтарную кислоту получают обработкой натриймалонового эфира иодом:
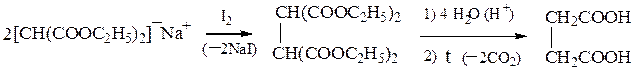
· Синтез кислоты любого строения с использованием для эфиров галоген-
замещенных кислот:
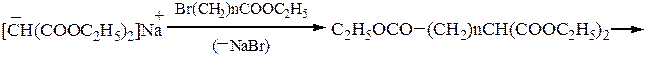
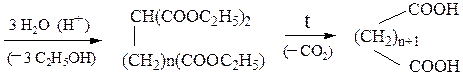
· Получение a,b-непредельных карбоновых кислот конденсацией
альдегидов с малоновой кислотой или ее эфиром в условиях щелочного катализа:
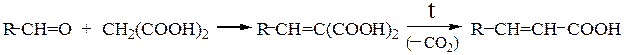
· Синтез производных барбитуровой кислоты, используемых в медицине
(снотворные средства) из замещенных малоновых кислот и мочевины по схеме:
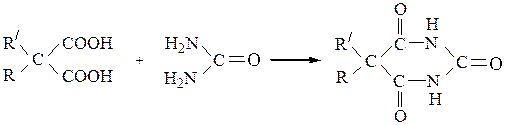
ВЫСШИЕ КАРБОНОВЫЕ КИСЛОТЫ
Таблица 16.Высшие карбоновые кислоты
| Структурная формула ВЖК | Название |
| Предельные ВЖК : | |
| СН3–(СН2)10–СООН | Лауриновая кислота, додекановая кислота |
| СН3–(СН2)12–СООН | Миристиновая кислота, тетрадекановая кислота |
| СН3–(СН2)14–СООН | Пальмитиновая, кислота гексадекановая кислота |
| СН3–(СН2)16–СООН | Стеариновая кислота, октадекановая кислота |
| Непредельные ВЖК : | |
CH3(CH2)7CH=CH(CH2)7COOH или 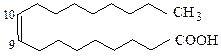 | Олеиновая кислота, цис-9-октадеценовая кислота |
СH3(CH2)4CH=CHCH2CH=CH(CH2)7COOH или 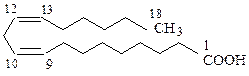 | Линолевая кислота, 9-цис-,12-цис-октадекадиеновая кислота |
СH3CH2CH=CHCH2CH=CHCH2CH=CH(CH2)7COOH или 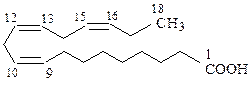 | Линоленовая кислота, 9-цис-,12-цис-,15-цис- октадекатриеновая кислота |
СH3(CH2)4CH=CHCH2CH=CHCH2CH=CHCH2CH=CH(CH2)3CO2H или 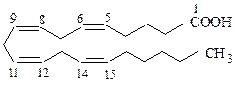 | Арахидоновая кислота, 5-цис-,8-цис-,12-цис-15-цис-эйкозатетраеновая кислота |
Содержатся в жирах. Они по своему строению одноосновны, имеют неразветвленную цепь углеродных атомов и содержат в молекулах четное число атомов углерода (С12 – С18). Ненасыщенные карбоновые кислоты, входящие в состав жиров, имеют цис-конфигурацию молекулы по отношению к двойным связям (см. табл. 13). Химические свойства высших карбоновых кислот напоминают свойства низших карбоновых кислот. С участием карбоксильной группы они вступают в реакции образования солей (мыла) галогенангидридов, ангидридов, амидов, сложных эфиров, нитрилов. Непредельные жирные кислоты также вступают в реакции по двойным связям (гидрирование, галогенирование, окисление).
Высшие кислоты находятся в природе, прежде всего, в составе жиров – полных сложных эфиров глицерина – причем жиры являются глицеридами не только одинаковых (простые ацилглицерины), но в основном разных кислот (смешанные ацилглицерины). Соотношение остатков карбоновых кислот меняется при переходе от одного жира к другому: каждый жир имеет свой характерный состав, мало изменяющийся от образца к образцу. Животные жиры, содержащие, главным образом, ацилглицерины предельных кислот, – твердые вещества. Растительные жиры, обычно называемые маслами, содержат глицериды непредельных кислот. Они являются преимущественно жидкостями, например подсолнечное, оливковое, конопляное и льняное масло.
В химическом отношении жиры – типичные сложные эфиры. Им характерны реакции гидролиза и присоединения по двойным связям ненасыщенных радикалов:
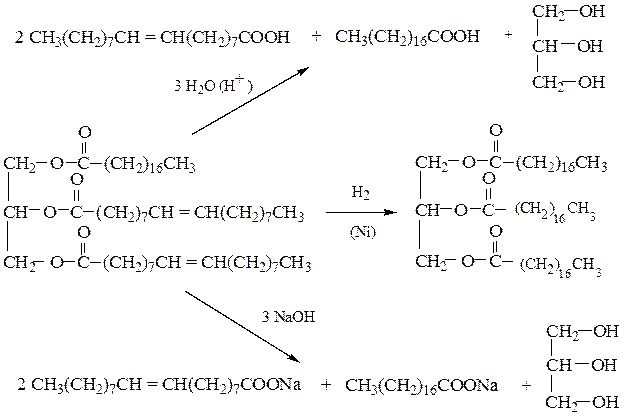
Жиры имеют большое значение в жизнедеятельности человека. Они выполняют функцию энергетического запаса, отлагаясь в тканях организма. По теплотворной способности жиры занимают первое место среди питательных веществ: 1 г жира при сгорании дает 9300 кал. Непредельные кислоты с системой связи –CH=CHCH2CH=CН– организм человека не синтезирует, но они должны входить в состав рациона для полноценного питания. Данные кислоты образуют липиды клеточных стенок и играют большую роль в придании им полупроницаемости при задерживании одних веществ и пропускании других.
Жиры служат исходным материалом в производстве глицерина и мыла. Высшие карбоновые кислоты, содержащие 24–32 атома углерода и спирты с числом атомов углерода от 16 до 30, входят в состав восков.
Фосфатиды (фосфолипиды) – диацилглицерины жирных кислот, в которых глицерин частично этерифицирован фосфорной кислотой, а кислота вторым своим гидроксилом этерифицирует аминоспирты –
холин HO–CH2CH2–N+(CH3)3 или этаноламин HO–CH2CH2–NH2.
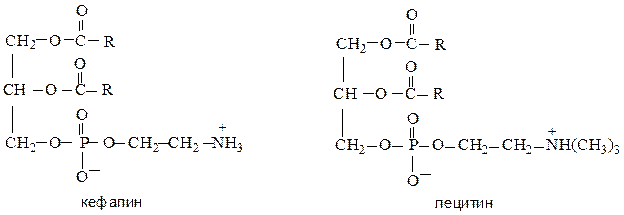
Фосфатиды входят в состав клеток и тканей животных (мозговая и нервная ткань, куриный желток) и раститетельных организмов, в куриный желток и играют важную роль в биологических процессах: при передаче нервного возбуждения, для регулирования проницаемости оболочек клеток и т.д.
Контрольные вопросы к главе 12 «Карбоновые кислоты»
№ 1Чем объясняются кислотные свойства карбоновых кислот и чем определяется их сила? Что такое рКа кислоты? Почему в карбоновой кислоте связи С-О различные по длине, а в карбоксилат-анионе одинаковые? Почему относительную силу кислот можно оценивать по стабильности их анионов?
Расположите соединения в ряд по возрастанию их кислотных свойств:
(а) a-бромпропионовая кислота, a,a-дибромпропионовая кислота, b-бромпропионовая кислота, a,b-дибромпропионовая кислота, пропионовая кислота; (б) бензойная кислота, 4-хлорбензойная кислота, 2,4,6-трихлор-бензойная кислота, 2,4-дихлорбензойная кислота; (в)триметилуксусная кислота, трифторуксусная кислота, уксусная кислота, пропионовая кислота, трихлоруксусная кислота; (г)муравьиная кислота, уксусная кислота, изомасляная кислота, щавелевая кислота; (д) иодуксусная кислота, бромуксусная кислота, уксусная кислота, хлоруксусная кислота, трифторуксусная кислота.
№ 2.Какие существуют способы повышения выхода сложного эфира при проведении реакции этерификации кислоты спиртом? Покажите механизм этерификации валериановой кислоты метанолом в прис. H2SO4. Что такое переэтерификация? Приведите механизм этой реакции на примере синтеза октилового эфира пропионовой кислоты.
№ 3. Приведите механизмы кислотного и щелочного гидролиза метилового эфира бензойной кислоты. Объясните, почему щелочи катализируют только гидролиз сложных эфиров, но не их образование. Если гидролиз метилбензоата проводить водой, меченной изотопом 18О, то в составе какого продукта гидролиза обнаружится 18О ?
№ 4.Какие функциональные производные карбоновых кислот вам известны? Укажите методы их получения, свойства и взаимосвязь.
№ 5.Что такое реакции ацилирования? Приведите примеры. Расположите в ряд по уменьшению ацилирующих свойств производные карбоновых кислот: бромангидрид уксусной кислоты, уксусный ангидрид, хлорангидрид уксусной кислоты, ангидрид масляной кислоты.
№ 6. Как различить: (а) муравьиную и уксусную кислоты; (б) щавелевую и уксусную кислоты; (в) щавелевую и янтарную кислоты; (г) малеиновую и фумаровую кислоты; (д) олеиновую и лауриновую кислоты.
№ 7. Главные глицериды хлопкового масла – пальмитоолеолинолеин пальмитодиолеин,трилинолеин. Напишите структурные формулы этих веществ.
№ 8.Напишите уравнения реакций и назовите образующиеся продукты:(а)муравьиной кислоты с пентанолом-1;(б)бензойной кислоты с хлористым тионилом; (в) щелочного гидролиза этилового эфира янтарной кислоты; (г) дегидратации ангидрида масляной кислоты с P2O5; (д) уксусного ангидрида с диметиламином; (е) расшифруйте схему превращений:
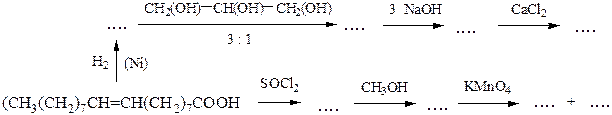
№ 9. Напишите схемы синтеза следующих соединений: (а) изомасляной кислоты из пропанола-1; (б) a-хлорфенилуксусной кислоты из толуола; (в)бензамида из толуола; (г) α-метилянтарной (2-метилбутандиовой-1,4) кислоты из пропилена; (д)циклопентанкарбоновую кислоту из циклопентана.
№10. Напишите схемы синтеза следующих кислот, используя малоновый эфир и необходимые алкилгалогениды: (а) b-фенилпропионовой кислоты; (б) пентен-4-овой кислоты; (в) 2-этил-3-фенилпропановой кислоты; (г)диэтил-уксусной кислоты; (д) α-метилянтарной (2-метилбутандиовой-1,4) кислоты.
№ 11.Установите строение соединений: (а) С3Н4О4, обладает кислыми свойствами, с этанолом дает вещество С7Н12О4; при нагревании исходного вещества выделяется СО2 и образуется вещество С2Н4О2, водный раствор которого также имеет рН<7; (б) С4Н8О2, реагирует с раствором Na2CO3 с выделением газа, при сплавлении с щелочью образуется пропан, с Са(ОН)2 дает соединение С8Н14О4Са, при пиролизе которого получается дипропилкетон; (в) С4Н8О2, нерастворяяется в воде, не реагирует с карбонатом натрия, а при кислотном гидролизе образует хорошо растворимые в воде вещества С2Н6О и С2Н4О2, последнее вещество способно реагировать с эквимолярным количеством NaOH; (г) С4Н6О2, при озонолизе образует формальдегид и пировиноградную кислоту СН3-СО-СООН.
ГИДРОКСИКИСЛОТЫ
Определение. Гидроксикислоты – соединения, в молекулах которых содержатся гидроксильная и карбоксильная группы.
Классификация
1) Функциональные группы гидроксикислот могут быть присоединены к
алифатической цепи молекулы (спиртокислоты) или к ароматическому кольцу (фенолокислоты):

п-гидроксибензойная кислота миндальная кислота (α-оксифенилуксусная кислота)
(фенолокислота) (спиртокислота)
2) По взаимному расположению функциональных групп гидроксикислоты
делятся на α-, β-, γ- и др. замещенные. Буквы греческого алфавита указывают положение гидроксильной группы относительно карбоксильной, причем отсчет ведется от ближайшего к карбоксильной группе атома углерода (от атома С-2).
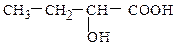
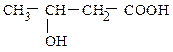
α-гидроксимасляная кислота β-гидроксимасляная кислота
3) По количеству карбоксильных групп различают одноосновные, двухосновные, многоосновные гидроксикислоты:
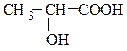
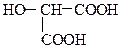
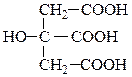
молочная кислота тартроновая кислота лимонная кислота
(одноосновная) (двухосновная) (трехосновная)
4) По количеству гидроксильных групп гидроксикислоты делят на одноатомные, двухатомные и т.д.:
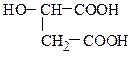
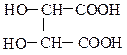
яблочная кислота (одноатомная) винная кислота (двухатомная)
Систематические названия гидроксикислот строятся по общим принципам заместительной номенклатуры, однако для многих широко распространенных представителей предпочтительными являются тривиальные названия.
Получение. a-Гидроксикислоты удобно получать гидролизом a-галоген-замещенных карбоновых кислот и оксинитрильным методом из карбонильных соединений.
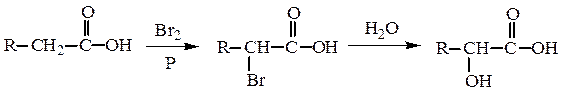
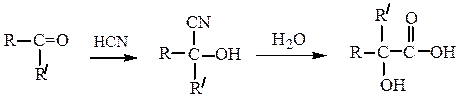
ного синтеза подвергаются бензоиновой конденсации. В этих случаях циангидрин получают из соответствующего гидросульфитного производного действием NaCN:
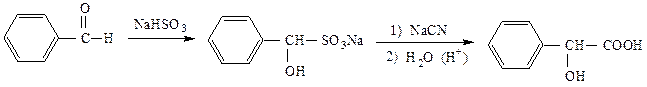
К другим методам синтеза относятся: реакции a-аминокислот с азотистой кислотой, мягкое окисление гликолей R-СH(OH)-CH2OH и восстановление эфиров кетонокислот.
R–CH–COOH HNO2 R–CH–COOH + N2 ↑ + H2O
│ ¾¾¾¾¾® │
NH2 OH
R-СH-CH2OH [Ag(NH3)2] OH R–CH–COONH4 + Ag ↓ + NH3 + H2O
│ ¾¾¾¾¾¾¾¾¾® │
OH OH
H2 H2 O
R–C–COOСH3 ¾¾® R–CH–COOCH3 ¾¾® R–CH–COOH
║ ( Ni) │ (H+) │
O OH OH
b-Гидроксикислоты обычно получают, используя реакции мягкого окисления альдолей (аммиакат серебра, бромная вода), гидратации a,b-непредельных карбоновых кислот или методом Реформатского, который заключается во взаимодействии карбонильных соединений с цинковой пылью и эфирами a-галогензамещенных карбоновых кислот:
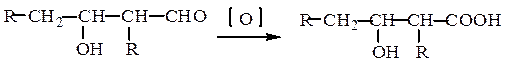
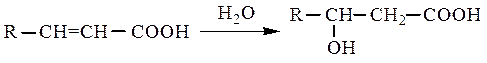
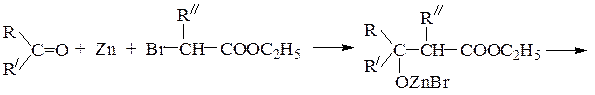
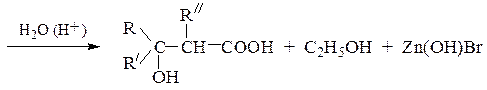
β-Гидроксикислоты можно также получать, иcпользуя общие методы: например, заменой галогена и восстановлением карбонильной группы, если они находятся в β-положении по отношению к карбоксильной группе:
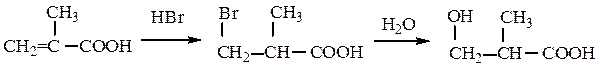
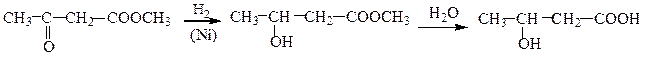
Фенолкарбоновые кислоты синтезируют по реакции Кольбе – Шмидтапри нагревании фенолятовщелочных металлов с оксидом углерода (IV). Использование фенолята натрия приводит к о-оксибензойной кислоте:
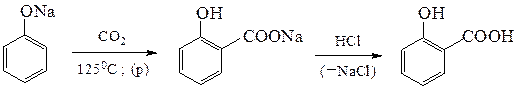
Использование фенолята калия по аналогичной схеме дает к ее п-изомер.
Химические реакции
В реакциях, характерных для карбоксильной и гидроксильной групп, могут затрагиваться как та, так и другая или обе одновременно. В последнем случае для проведения реакции по одной из групп используют методы защиты другой.
Таблица 17. Реакции функциональных групп гидроксикислот с реагентами
| Реагент Функц. группа | Na | NaOH или Na2CO3 | NH3 | HBr | CH3OH (HCl) | PCl5 | (CH3CO)2O |
| -COOH | + | + | + | - | + | + | - |
| -OH | + | - | - | + | - | + | + |
Схема 16. Химические реакции молочной кислоты
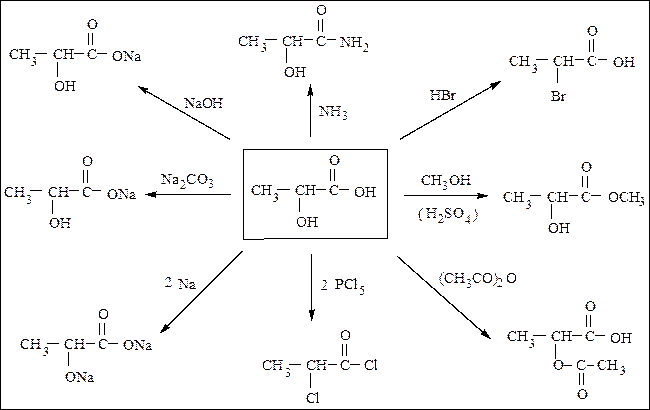
Фенолокислоты в отличие от спиртокислот при взаимодействии с гидроксидом натрия реагируют обеими функциональными группами, а в случае обработки бромоводородом фенольный гидроксил проявит инертность.
В результате ацилирования салициловой кислоты уксусным ангидридом получают лекарственный препарат – аспирин (ацетилсалициловую кислоту):
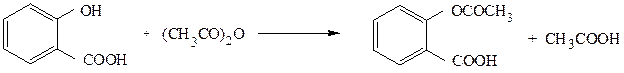 салициловая кислота аспирин
салициловая кислота аспирин
Фенолокислотыэтерифицируются по карбоксильной группе спиртами в присутствии минеральной кислоты, однако низкая нуклеофильность фенолов не позволяет таким способом получить фенилацетат. Поэтому салициловую кислоту предварительно превращают в более активный ацилирующий агент – ее хлорангидрид, которым затем ацилируют фенол:
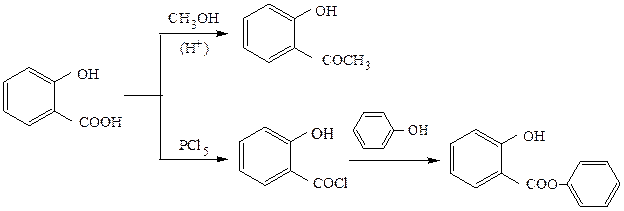
Специфической реакцией гидроксикислот является дегидратация при нагревании, причем в зависимости от их типа реакции идут по разным схемам, приводящим к различным продуктам:
а) a-гидроксикислоты обычно образуют продукты межмолекулярной реакции - лактиды:
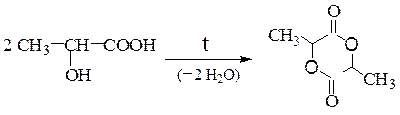
б) b-гидроксикислоты превращаются в a,b-непредельные кислоты:
t
CН3–СН2–СН–СН2–СООН ¾¾¾® CН3–СН2–СН=СН–СООН
│ (- Н2О)
ОН
в) g- и d-гидроксикислоты дают циклические эфиры (лактоны):
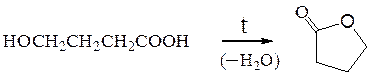
γ-гидроксимасляная кислота γ-бутиролактон
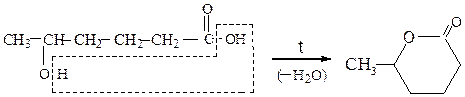
δ-гидроксикапроновая кислота δ-капролактон
Внутримолекулярную этерификацию g-гидроксикарбоновой кислоты до g-лактона в кислой среде можно представить следующей схемой:
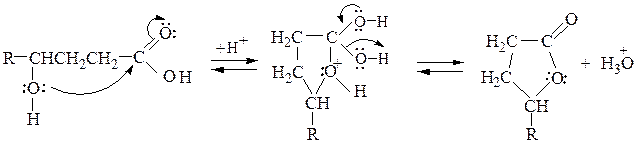
г)при нагревании лимонная кислота (как b-гидроксикислота) превращается в аконитовую кислоту, которая распадается далее на смесь итаконового и цитраконового ангидридов. В присутствии H2SO4 лимонная кислота (как a-гидроксикислота) отщепляет муравьиную кислоту и образует ацетондикарбоновую кислоту
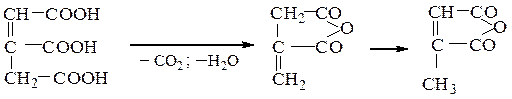
аконитовая кислота итаконовый ангидрид цитраконовый ангидрид
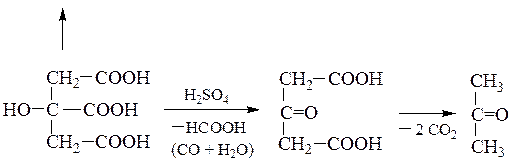
лимонная кислота ацетондикарбоновая кислота ацетон
д) винная кислота при нагревании теряет воду и декарбоксилируется, превращаясь в пировиноградную кислоту:
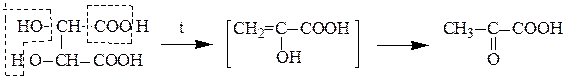
Оптическая изомерия.Растворы некоторых органических веществ способны отклонять плоскость плоскополяризованного света на определенный угол. Такие соединения называются оптически активными и существуют в виде двух оптических изомеров: один из этих изомеров вращает плоскость поляризации влево, другой (в одинаковых условиях) на такой же угол вправо. Для обозначения этого явления пользуются знаками (+) и (─), которые ставят перед названием оптического изомера. Такие изомеры называют энантиомерами. Смесь, состоящую из равных количеств левовращающего и правовращающего изомеров, называют рацематом и обозначают символом (+). Рацемат оптически неактивен из-за взаимной компенсации оптической активности входящих в него оптических изомеров. Одной из причин появления оптической активности у некоторых органических веществ является наличие в молекуле асимметрического атома углерода, у которого все четыре валентности соединены с различными заместителями. Любое органическое вещество, содержащее асимметрический атом, можно представить в виде двух пространственных форм, которые отличаются друг от друга как предмет от зеркального отображения. При наложении этих пространственных форм нельзя добиться их совмещения. Такая изомерия получила название «зеркальной». Молекулы, несовместимые в пространстве и относящиеся друг к другу как зеркальные отображения, являются хиральными; у них отсутствуют плоскости и центры симметрии. При наличии в молекуле нескольких (n) асимметрических атомов углерода, общее число стереоизомеров (N) (сюда входят зеркальные изомеры – энантиомеры и диастереомеры – незеркальные изомеры) определяют по формуле: N = 2n.
При изображении оптически активных изомеров используют проекционные формулы Фишера. Для этого главную цепь молекулы гидроксикислоты располагается вертикально с первым атомом углерода вверху (карбоксильная группа). Тетраэдр асимметрического атома углерода, содержащий четыре раз-
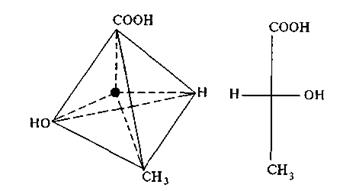 Рис. 8. D-молочная кислота Рис. 8. D-молочная кислота | личных заместителя, поворачивают так, чтобы начало и продолжение цепи находились за плоскостью проекции, а боковые заместители были направлены к наблюдателю. Все атомы, кроме асимметричес-кого, и группы атомов проекти-руются на плоскость, асимметрии-ческий атом С предполагается в точке пересечения линий его связей со всеми заместителями. |
Если при таком построении функциональная группа ОН оказывается справа, то соединение относится к D-ряду, если слева, то к L-ряду.
При изменении положения проекционной формулы на плоскости, во избежание искажения стереохимического смысла, преобразования проводят с соблюдением следующих правил:
1. Проекционные формулы Фишера нельзя выводить из плоскости бумаги, ее нельзя поворачивать на 90° (допустим поворот на 180°):
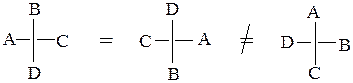
Допустимо фиксирование одной группы и вращение трех остальных по часовой стрелки или против часовой стрелки:
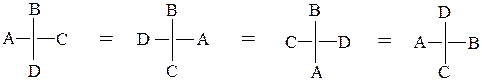
2. В проекциях Фишера однократная взаимная перестановка любых двух групп приводит к превращению энантиомера в его зеркальное изображение, а
при перестановке местами заместителей у одного асимметрического центра четное число раз стереохимическая конфигурация соединения сохраняется.
3. Проекционные формулы Фишера нельзя применять к молекулам, хиральность которых обусловлена не наличием асимметрического атома, а другими причинами.
Для обозначения конфигурации асимметиричесих атомов в хиральных (оптически активные) молекулах в настоящее время используют D,L- (см. выше) и R,S- системы обозначений. В основу R,S-системы обозначения конфигурации положен принцип старшинства заместителей, окружающих центр хиральности. Для этого проекционную формулу Фишера преобразуют так, чтобы младший заместитель разместился внизу, на вертикальной связи. Если после преобразования проекции падение старшинства заместителей остальных трех группировок проходит против часовой стрелки, то асимметрическому атому приписывают S-конфигурацию. Падение старшинства по часовой стрелке соответствует R-конфигурации. Старшинство заместителей определяется следующими правилами:
1. Если с хиральным центром (асимметрический атом углерода) связаны четыре различных атома, то старшим является атом с большим атомным номером (I > Вг > Cl > S > Р > F >N > ОН).
2. Если старшинство групп нельзя определить с помощью правила 1, то необходимо провести аналогичное сравнение следующих атомов в группе:
а) -СН2С1 > -СН2ОН > -СН2СН3 ;
б) -С(СН3)3 > -СН(СН3)2 > -СН2СН3 > -СН3 ;
в) СН3-О-СН-СН2СН3 > Н-О-СН-СН2СН3 .
½ ½
3. Если группа содержит двойную (тройную) связь, то ее атомы следует удвоить (утроить). Так, -СН=СН2 эквивалентна -CH-CH2-
½ ½
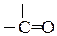 эквивалентна
эквивалентна 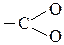 ; -CºN эквивалентна
; -CºN эквивалентна 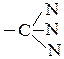
а) СН3-СН-СН2СН3 > -СН=СН2 > -СН3 ;
½
б) -СООСН3 > -СООН > -CONH2 > -СНО ;
в) -CºN > -С6Н5 > -СºСН > -СН=СН2 .
4. Старшинство изотопов убывает с уменьшением их массы (Т> D > Н). При обозначении конфигурации по R,S-системе рассматривается модель хиральной молекулы, которую располагают так, чтобы младший заместитель (атом водорода) был удален от глаза наблюдателя. Если падение старшинства остальных заместителей происходит по ходу часовой стрелки, то соединению приписывают R-конфигурацию, если против - S-конфигурацию.
Отдельные представители
Молочная кислота.Образуется в квашеных продуктах (моченые яблоки, капуста, огурцы) при молочнокислом брожении сахаров бактерииями родов Lactobacillus и Streptococcus: С6H12O6 (D–глюкоза) ¾® 2 CH3CH(OH)COOH. Существует в двух оптически активных (D и L и неактивной рацемической формы. Рацемическая форма представляет молочную кислоту брожения. L-(+)-молочная кислота образуется в мышцах как продукт превращения гликогена. D-(–)-молочная кислота может быть получена под действием микроорганизмов. Соли и сложные эфиры молочной кислоты называются лактатами.
Яблочная кислота содержится в незрелых яблоках, рябине, барбарисе. Существует в виде двух энантиомеров и рацемата.

D-(+)-яблочная кислота L-(-)-яблочная кислота
2-(R)-гидроксибутандиовая кислота 2-(S)-гидроксибутандиовая кислота
Винная кислота. Содержит два асимметрических атома углерода. Согласно формуле N= 2n, должна бы существовать в виде 4 конфигурационных стереоизомеров, однако вследствие наличия плоскости симметрии два из них одинаковые и оптически неактивные (табл. ). D-винная кислота содержится в виноградном соке; в процессе приготовления вина она накапливается в виде малорастворимого гидротартрата калия и часто образует осадок – «винный камень». Двойная соль – калийнатрийтартрат (сегнетова соль), подобно вицинальным диолам, способна образовывать с голубым осадком Cu(OH)2 растворимое в воде комплексное соединение темно-синего цвета. Оно используется для идентификации альдегидов и называется жидкостью Фелинга (см. с. 142).
Контрольные вопросы к главе 13 «Гидроксикислоты»
№ 1.Какие нужно взять исходные вещества, чтобы синтезировать по методу Реформатского: (а) 3-гидрокси-3-метилбутановую кислоту; (б) 3-гидрокси-3-метилпентановую кислоту; (в) b-гидрокси-b-фенилмасляную кислоту; (г) b-гидрокси-b-фенил-a-метилпропионовую кислоту?
Таблица 18. Стереоизомеры винной кислоты
D-(+)- или 2R,3R-винная кислота 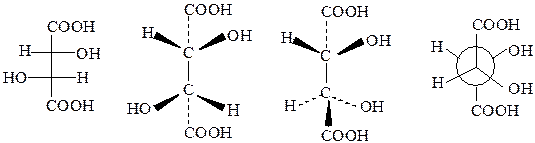 т.пл. 170 °С ; [ α ]D (25 °C, 20%-ный р-р) = + 12°; растворимость при 20 °С – 139 г в 100 г воды; К1 = 1,17·10─3 , К2 = 5,9·10─-5 т.пл. 170 °С ; [ α ]D (25 °C, 20%-ный р-р) = + 12°; растворимость при 20 °С – 139 г в 100 г воды; К1 = 1,17·10─3 , К2 = 5,9·10─-5 |
L-(─)- или 2S,3S-винная кислота 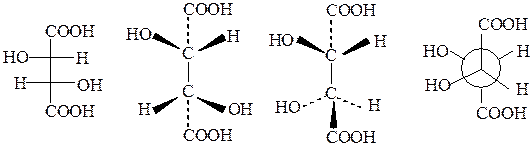 т.пл. 170 °С ; [ α ]D (25°C, 20%-ный р-р) = ─ 12°; растворимость при 20 °С– 139 г в 100 г воды; К1 = 1,17·10─3 , К2 = 5,9·10─5 т.пл. 170 °С ; [ α ]D (25°C, 20%-ный р-р) = ─ 12°; растворимость при 20 °С– 139 г в 100 г воды; К1 = 1,17·10─3 , К2 = 5,9·10─5 |
| виноградная кислота [рацемическая смесь – DL-( + )-винная кислота]: т.пл. 206 °С ; [α]D (25C, 20%-ный р-р) = 0 0 (оптически неактивна); растворимость при 200С– 20,5 г в 100 г воды; К1 = 1.1·10─3 , К2 = 5.8·10─5 |
2R,3S-винная кислота (мезовинная кислота) 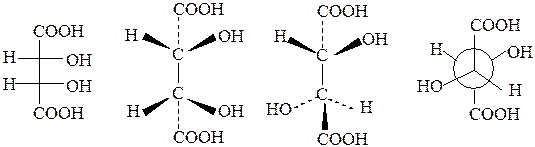 т.пл. 140 0С ; [α]D (250C, 20%-ный р-р) = 0 0 (оптически неактивна); растворимость при 200С– 125 г в 100 г воды; К1 = 0.77·10─3 , К2 = 1.6·10─5 т.пл. 140 0С ; [α]D (250C, 20%-ный р-р) = 0 0 (оптически неактивна); растворимость при 200С– 125 г в 100 г воды; К1 = 0.77·10─3 , К2 = 1.6·10─5 |
№ 2.Напишите уравнения реакций салициловой кислотыс реагентами, взятыми в избытке: (а) пропионовым ангидридом, (б) гидроксидом натрия, (в) этанолом, (г) хлористым тионилом, (д) аммиаком, (е) натрием.
№ 3.Дайте определения понятиям: «оптически активное соединение», «хиральный центр», «диастереомеры», «энантиомеры», «рацемат», «мезо-соединение». Изобразите проекционные формулы Фишера (где возможно) для D- и L-изомеров: (а) диметилового эфира яблочной кислоты; (б) диэтилового эфира винной кислоты; (в) изобутилового эфира α-гидрокси-изомасляной кислоты.
№ 4.Какие гидроксикислоты при нагревании образуют следующие соединения:
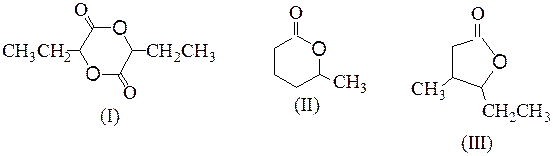
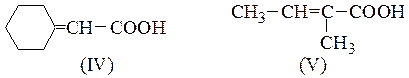
№ 5.Как с помощью химических проб различить изомерные вещества: (а) миндальную и салициловую кислоты; (б) метиловый эфир гликолевой кислоты и метоксиуксусную кислоту?
№ 6.Определите строение веществ по молекулярной формуле и продуктам реакций: (а)С8Н8О3, растворяется в воде и водной щелочи, образует сложные эфиры с кислотами и спиртами, не дает реакции с FеС13, реагирует с РС15, образуя вещество С8Н6ОС1. Имеет два оптических изомера;(б)С6Н12О3, оптически деятельно, с основаниями образует соль, при нагревании дает соединение C6H10O2, которое, окисляясь KMnO4 при нагревании, превращается в смесь изомасляной и щавелевой кислот; (в)C9H10O3 (троповая кислота), получают из алкалоида атропина, находящегося в Atropa belladonne, при окислении KMnO4 в кислом растворе дает бензойную кислоту, реагирует с одним эквивалентом NaOH и двумя Na;(г)С4Н8О3, водный раствор имеет рН < 7, обладает оптической активностью, при действии НС1 образует С4Н7О2С1, а при обработке РС15 - С4Н6ОС12, может быть получено циангидридным синтезом из карбонильного соединения
№ 7.Cинтезируйте: (а) молочную кислоту из этанола; (б) a-гидрокси-изомасляную кислоту из пропилена; (в) винную кислоту из бензола; (г) метилсалицилат (метиловый эфир о-гидроксибензойной кислоты) из о-крезола (2-метилфенола); (д) лимонную кислоту из хлоруксусной кислоты.
ОКСОКИСЛОТЫ
Определение. Оксокислотами называются соединения, содержащие наряду с карбоксильной группой оксогруппу, т.е. это альдегидо- или кетонокислоты.
Классификация.Оксокислоты могут содержать одну, две и более карбонильных или карбоксильных групп. По взаимному расположению функциональных групп различают α-, β-,γ- и др. оксокислоты.
Номенклатура.В названиях альдегидо- и кетонокислот наличие карбонильной группы обозначают приставкой «оксо-». Для некоторых оксокислот используются тривиальные названия (пировиноградная, левулиновая), а для оксокислот, участвующих в биохимических циклах в живых организмах, используются традиционно сложившиеся в биохимической литературе названия – ацетоуксусная, щавелевоуксусная, кетоглутаровая и др.
Способы получения. К общим методам синтеза оксокислот относятся гидролиз гем-дигалогензамещенных кислот и окисление гидроксикислот:
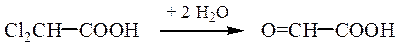
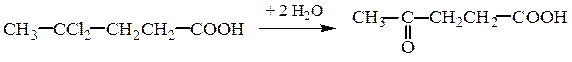
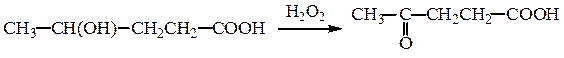
α-Оксокислоты образуются при гидролизе α-оксонитрилов, которые могут быть получены из хлорангидридов карбоновых кислот и солей синильной кислоты, например при использовании цианида меди (I):
R–C=O Cu2(CN)2 R–C=O H2O R–C=O
│ ¾¾¾¾¾¾® │ ¾¾¾¾¾® │
Cl CN OH
Пировиноградную кислоту можно получить из винной кислоты, которая при нагревании теряет воду и декарбоксилируется,а ацетондикарбоновую кислоту – из лимонной кислоты при действии олеума в результате дегидрата-ции и декарбонилирования. β-Оксокислоты разлагаются при попытке выделить их в свободном состоянии.(ацетоуксусная кислота легко декарбоксилируется, чему способствует образование внутримолекулярной водородной связи):
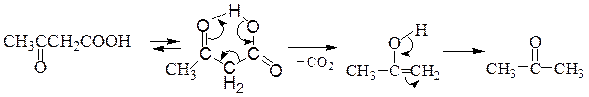
В связи с этим β-оксокислоты обычно получают в виде стабильных сложных эфиров с помощью сложноэфирной конденсации по Кляйзену, которая протекает протекает по схеме:
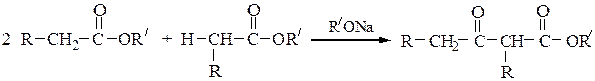
Механизм конденсации Кляйзена следующий:
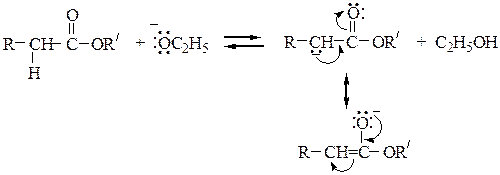
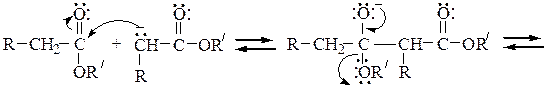
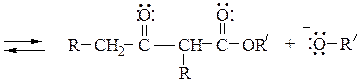
Перекрестной сложноэфирной конденсацией по Кляйзену между этилокса-латом (карбонильная компонента) и этилацетатом (метиленовая компонента) синтезируют эфир щавелевоуксусной кислоты (этилоксалоацетат):
&n
