Линейная димеризация и тримеризация ацетилена.
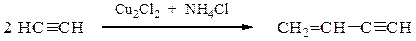
бутен-1-ин-3 (винилацетилен)
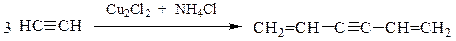
гексадиен-1,5-ин-3 (дивинилацетилен)
10. Циклотримеризация.
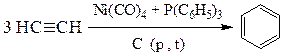
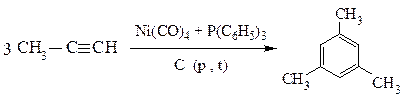
Циклотетрамеризация ацетилена на Cu2(CN)2 дает циклооктатетраен.
11. Кислотные свойства. Получение ацетиленидов (алкинидов).
Кислотными свойствами обладают только ацетилен и алкины-1 (R-СºС-H), имеющие атом водорода у sp-гибридизованного С-атома. Это обусловлено смещением электронной плотности к центру связи СºС, приводящему к «обнажению» ядра sp-гибридизованного атома углерода. Появление на нем эффективного положительного заряда разрыхляет связь С-Н, и возникает СН-кислотность. Сила протонных кислот обусловлена прочностью связи С-Н и стабильностью образующегося аниона. В молекулах метана, этилена и ацетилена [ рКа (СН4) = 45, рКа (СН2=СН2) = 36, рКа (СНºСН) = 25, рКа (С2Н5ОН) = 16, рКа (СН3СООН) = 4,5 ] атомы водорода, как и неподеленная пара электронов в соответствующих им карбанионах, связаны с sp3-, sp2- и sp-гибридизованными С-атомами. S-Электроны связаны с ядром прочнее, чем р-электроны, и менее подвижны. Следовательно, с увеличением s-характера орбитали, на которой расположена неподеленная пара электронов, будет увеличиваться и устойчивость карбаниона: H3C- < CH2=CH- < HCºC-, и сила соответствующих СН-кислот: СН4 < СH2=CH2 < HCºCH . В этом ряду увеличивается и энергия разрыва связи С-Н : 410, 440 и 500 кДж / моль соответственно.
При взаимодействии со щелочными металлами или сильными основаниями (например, амид натрия) образуются ацетилениды (алкиниды):
HC≡CH + NaNH2 ¾¾ ¾¾® HC≡C–Na + NH3
NH3 (жидк.)
(СН3)3С–С≡СН + Na ¾¾ ¾¾® (СН3)3С–С≡С–Na + ½ H2 ↑
NH3 (жидк.)
С аммиакатами серебра и меди (I) ацетилен и алкины-1 образуют осадки:
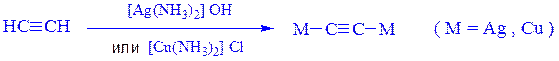
Моно- и дизамещенные ацетилены можно синтезировать через натриевые производные или комплекс Йоцича (BrMg–C≡C–MgBr) алкилированием соответствующими галогенопроизводными углеводородов по схеме:
NaNH2 R–X 1) NaNH2
HC≡CH ¾¾ ¾¾® HC≡C–Na ¾¾® HC≡C–R ¾ ¾¾® R/–C≡C–R
NH3 (жидк.) (–NaX) 2) R/–X
(–NaX)
Данная схема, однако, исключает возможность введения третичных радикалов, поскольку в присутствии сильных оснований практически полностью происходит дегидрогалогенирование третичных алкилгалогенидов. Также с невысокими выходами удается выделить продукты дизамещения ацетилена. Причиной этого является побочно протекающие перегруппировки Фаворского, приводящие к перемещению тройной связи.
12. Реакции с карбонильными соединениями.
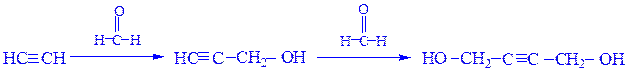 пропин-2-ол-1 бутин-2-диол-1,4
пропин-2-ол-1 бутин-2-диол-1,4
(пропаргиловый спирт)
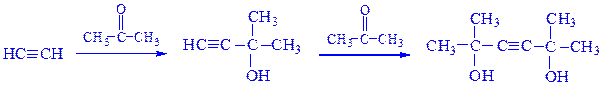
2-метилбутин-3-ол-2 2,5-диметилгексин-3-диол-2,5
2-Метилбутин-3-ол-2 является полупродуктом в синтезе изопрена из ацетилена по методу Фаворского.
13. Окисление.
Горение. С воздухом ацетилен образует взрывоопасные смеси.
2 HC≡CH + 5 О2 ¾® 4 СО2 + 2 Н2О СnH2n-2 + (3n- ½) O2 ¾® n СО2 + (n-1) Н2О
Мягкое окисление осуществляется перманганатом калия в нейтральной среде или диоксидом селена; в результате образуются дикетоны:
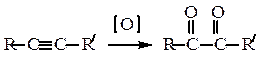
Жесткое окисление проводят действием перманганата калия в кислой или щелочной среде (качественная реакция на тройную связь – обесцвечивание фиолетового раствора) или дихроматом калия в кислой среде. Происходит расщепление тройной связи и образуются смеси карбоновых кислот:
[O] COOH [O]
HC≡CH ¾¾® │ R–C≡C– R/ ¾¾® R–COOH + R/–COOH
COOH
щавелевая кислота
1) О3
Озонолиз ацетилена приводит к глиоксалю: HC≡CH ¾ ¾¾® О=НC–CН=О
2) 2 Н2О
Схема 5. Реакции и пути промышленного использовании яацетилена
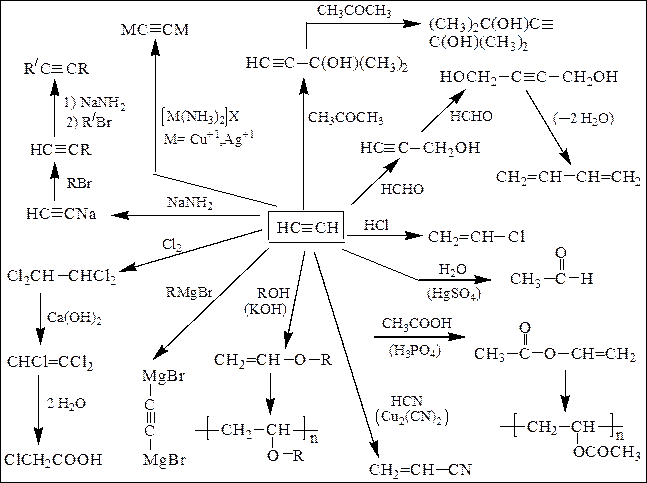
Применение алкинов. Ацетилен применяется в качестве горючего при газовой сварке и резке металлов (температура пламени достигает 3000 0С). Ацетилен и его производные используются в синтезах уксусного альдегида, уксусной кислоты, этилена, хлоруксусной кислоты и трихлоруксусной кислоты, хлористого винила и полихлорвинила, винилацетилена и хлоропренового каучука, винилацетата, акрилонитрила, бальзама Шостаковского и др.:
Контрольные вопросы к главе 4 «Алкины»
№ 1. Напишите уравнения реакций:(а)бромирования изопропилацетилена; (б) метилацетилена с формальдегидом; (в) гидратации гептина-1 в присутствии HgSO4 (pеакция Кучерова); (г) циклотримеризации бутина-2, (д) бензил-ацетилена с аммиакатом серебра; (е) ацетилена с пропанолом-2 (в присутствии КОН); (ж) гидрохлорирования третбутилацетилена; (з) бутина-1 с HCN.
№ 2.Объясните наличие слабых кислотных свойств у ацетилена и алкинов-1
№ 3. Напишите схемы синтеза следующих соединений, используя неорганические реагенты: (а) бутанона-2 из 1-бромбутана; (б) акрилонитрила из 1,2-дибромэтана; (в) мезитилена (1,3,5-триметилбензола) из пропанола-1; (г) 1,1,2,2,3,4-гексабромбутана из ацетилена; (д) поливинилацетата из ацетилена.
№ 4.Установите строение соединений: :(а) С7Н12, при гидрировании образуется 3-метилгексан, а при обработке аммиакатом серебра — C7H11Ag;(б) С7Н12, с аммиакатом серебра образуется C7H11Ag, а при гидратации по Кучерову — 5-метилгексанон-2;(в) С6Н10, имеет симметричное строение молекулы, не реагирует с амидом натрия в жидком аммиаке, при гидратации в присутствии сульфата ртути (II) образует несимметричное карбонильное соединение;(г) С6Н10, в результате обработки эквимолярными количествами амида натрия в жидком аммиаке и бромистого изопропила образуется 2,6-диметилгептин-3;(д) С4Н4, при последовательной обработке эквимолярными количествами амида натрия в жидком аммиаке и иодистого аллила обра- зуется гептадиен-1,6-ин-3;
№ 5.Как с помощью химических реакций можно различить: (а) октина-1 от октана; (б) гексина-1 от гексина-2; (в) бутина-2 от бутадиена-1,3; (г) пентадиена-1,4 от пентина-1; (д) ацетилена от пропина.
