Получение и свойства оксидов
Оксиды
Названия и формулы оксидов
Оксидами называются вещества, состоящие из двух элементов, один из которых кислород в степени окисления – 2. В оксидах атомы кислорода соединяются только с атомами других элементов и не связаны между собой.
Номенклатура. Названия оксидов элементов, имеющих постоянную степень окисления, составляются из двух слов
оксид + нaзвaние элемента в родительном падеже:
MgO — оксид магния, Na2O - оксид натрия, СаО - оксид кальция.
Если элемент образует несколько оксидов, то после названия элемента указывается его степень окисления римской цифрой в скобках: МnО — оксид марганца (II), Мn2О3 — оксид марганца (III).
Название оксидов можно также образовывать добавлением к слову «оксид» греческих числительных. Например, СО2 -диоксид углерода, SО2 — диоксид серы, SO3 — триоксид серы,OsO4 — тетраоксид осмия.
Классификация. По химическим свойствам оксиды делятся на солеобразующие и несолеобразующие. Оксиды, которые при химических реакциях образуют соли, называются солеобразующими:
CO2 + Са(ОН)2 = СaСО3¯ + H2O
оксид гидроксид карбонат
углерода кальция кальция
(IV)
MgO + 2HCl = MgCl2 + Н2О
оксид хлорово хлорид
магния дородная магния
кислота
СО2 и MgO — солеобразующие оксиды.
Оксиды, которые не образуют солей, называются несолеобразующими: NO — оксид азота (II), N2O — оксид азота (I), SiO — оксид кремния (II) — это несолеобразующие оксиды. Несолеобразующих оксидов мало.
Кислоты
Названия и формулы кислот
Кислотами называются соединения, в состав которых входят атомы водорода, способные замещаться атомами металла. При этом образуются соли.
Например,
2НС1 + Mg ® MgС12 + Н2↑
С позиций теории электролитической диссоциации, кислотами называются электролиты, при диссоциации которых в качестве катионов образуются только ионы водороды, способные замещаться на атомы металла.
Классификация. Кислоты различают:
1) по наличию или отсутствию кислорода в составе кислоты
а) бескислородные (это водные растворы водородных соединений неметаллов VI и VII групп периодической системы элементов Н2S, H2Se, H2Te, HF, HC1, HBr, HI, a также HSCN и HCN);
б) кислородсодержащие (это гидраты оксидов неметаллов, а также некоторых металлов в высших степенях окисления (+5, +6, +7) - Н2СО3, H2SO4, H2СrО4 и т.д.).
2) по основности (т.е. по числу атомов водорода в молекуле кислоты, способных замещаться атомами металлов с образованием соли)
а) одноосновные (HCl, HNO3, HCN, CH3COOH),
б) двухосновные (H2S, H2SO4, H2СО3),
в) трехосновные (H3РО4, Н3AsO4) и т.д.
Номенклатура.
а) Названия бескислородных кислот составляют из
названия элемента + О + слово «водородная»:
НCl – хлороводородная кислота, H2S – сероводородная кислота, HCN – циановодородная кислота, HI – йодоводородная кислота.
б) Названия кислородсодержащих кислот образуют от
русского названия элемента + «кислота».
При этом название кислоты, в которой элемент имеет высшую степень окисления, оканчивается на –наяили-овая(H2SO4 – серная кислота, HClO4- хлорная кислота, H3AsO4 – мышьяковая кислота). С понижением степени окисления элемента окончания изменяются так: - оватая (HСlO3 – хлорноватая кислота), -истая (HСlO2 – хлористая кислота), -оватистая(HOCl – хлорноватистая кислота). Если элемент образует кислоты, находясь только в двух степенях окисления, то название кислоты, отвечающей низшей степени окисления, получает окончание –истая (HNO3 – азотная кислота, HNO2 – азотистая кислота)
Кислотные остатки. Отрицательно заряженные группы атомов и одиночные атомы (отрицательные ионы), которые остаются после отрываот молекулы кислоты одного или нескольких атомов водорода, называются кислотными остатками.
Величина отрицательного заряда кислотного остатка определяется числом атомов водорода, замещенных металлом (табл.15).
Таблица 15. Названия и формулы некоторых кислотных остатков.
| Формула кислоты | Название кислоты | Кислотный остаток | Название кислотного остатка | |
| HCl | Хлороводородная (соляная) | Cl- | Хлорид-ион | |
| HBr | Бромоводородная | Br- | Бромид-ион | |
| HI | Йодоводородная | I- | Йодид-ион | |
| H2S | Сероводородная | HS- | Гидросульфид-ион | |
| S2- | Сульфид-ион | |||
| HClO | Хлорноватистая | ClO- | Гипохлорит-ион | |
| HClO2 | Хлористая | ClO 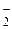 | Хлорит-ион | |
| HClO3 | Хлорноватая | ClO 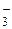 | Хлорат-ион | |
| HClO4 | Хлорная | ClO 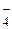 | Перхлорат-ион | |
| H2SO3 | Сернистая | HSO 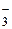 | Гидросульфит-ион | |
SO 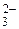 | Сульфит-ион | |||
| H2SO4 | Серная | HSO 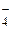 | Гидросульфат-ион | |
SO 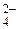 | Сульфат-ион | |||
| HNO2 | Азотистая | NO 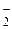 | Нитрит-ион | |
| HNO3 | Азотная | 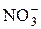 | Нитрат-ион | |
| H3PO4 | Ортофосфорная | 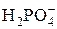 | Дигидрофосфат-ион | |
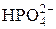 | Гидрофосфат-ион | |||
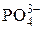 | Ортофосфат-ион | |||
| H2CO3 | Угольная | 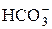 | Гидрокарбонат-ион | |
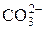 | Карбонат-ион | |||
| H2SiO3 | Кремниевая | 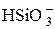 | Гидросиликат-ион | |
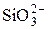 | Силикат-ион | |||
| HMnO4 | Марганцовая | 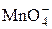 | Перманганат-ион | |
| H3BO3 | Борная (ортоборная) | 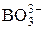 | Борат-ион | |
| H2CrO4 | Хромовая | 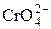 | Хромат-ион | |
| H2Cr2O7 | Дихромовая | 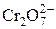 | Дихромат-ион | |
| HCN | Циановодородная (синильная) | 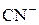 | Цианид-ион |
Получение и свойства кислот
Получение. 1. Кислородсодержащие кислоты можно получить при взаимодействии кислотных оксидов с водой
P2O5 + 3H2O = 2H3PO4 SO2 + H2O = H2SO3
оксид ортофосфорная оксид сернистая
фосфора (V) кислота серы (IV) кислота
2. Бескислородные кислоты получаются при растворении в воде продуктов соединения неметаллов с водородом:
H2 + Cl2 = 2HCl, раствор НС1 в воде — хлороводородная кислота
хлоро -
водород
Н2 + I2 = 2НI, раствор HI в воде — йодоводородная кислота
йодо –
водород
3. И бескислородные и кислородсодержащие кислоты получаются при действии на их соли других кислот (более сильных или менее летучих). Например,
2CH3COONa + H2SO4(к) = 2СН3СООН + Na2SO4
ацетат натрия серная уксусная сульфат
кислота кислота натрия
концентри
рованная
FeS + 2HC1 = FеС12 + H2S
сульфид хлорово - хлорид сероводород
железа (II) дородная железа (II)
кислота
NаС1 + Н2SO4(к) = NaHSO4 + HCl
хлорид серная гидросуль хлороводород
натрия кислота фат
концентри натрия
рованная
Физические свойства. Кислоты могут быть твердыми (борная Н3ВО3,) или жидкими (серная H2SO4, азотная НNО3) веществами. Большинство из них хорошо растворяется в воде. Кислотами являются также растворы газов НС1, НВr, H2S и других в воде. В молекулах кислот атомы водорода связаны с кислотными остатками ковалентной полярной связью.
Химические свойства.
1. Кислоты изменяют окраску многих индикаторов. В табл. 16 показано изменение цвета индикаторов в разных средах.
Таблица 16. Цвет некоторых индикаторов в нейтральной, кислой и щелочной среде.
| Индикатор | Среда | ||
| нейтральная | щелочная | кислая | |
| Метиловый оранжевый Фенолфталеин Лакмус | Оранжевый Бесцветный Фиолетовый | Желтый Малиновый Синий | Красный Бесцветный Красный |
2. Кислоты взаимодействуют с основаниями. При этом образуются соль и вода:
2NaOH + H2SO4 = Na2SO4 + 2Н2О
гидроксид серная сульфат
натрия кислота натрия
разбавленная
NaOH + H2SO4 = NaHSO4 + H2O
NaHSO4 + NaOH = Na2SO4 + Н2О
3. Кислоты взаимодействуют с основными оксидами. В результате реакции образуются соль и вода:
СаО + 2НNО3 = Са(NO3)2 + Н2О
оксид азотная нитрат
кальция кислота кальция
разбав –
ленная
NH3 + HCl = NH4Cl
4. Кислоты реагируют с металлами. В результате реакции образуется соль и выделяется газ, например, водород:
Mg + HCl = MgCl2 + H2↑
Zn + H2SO4(разб) = ZnSO4 + H2
Металлы, которые в ряду напряжений расположены слева от водорода, вытесняют его из кислот. Металлы, которые в ряду напряжений расположены справа от водорода (Сu, Hg, Ag, Au, Pt), не вытесняют его из кислот.
При реакции металлов с концентрированными азотной и серной кислотами обрадуются соли, но водород не выделяется. В этом случае понижают степень окисления азот N+5 и сера S+6 .
Например,
Zn + 2H2SO4(конц) = ZnSO4 +SO2 + 2H2O
Сu + 4HNO3(конц) = Сu(NO3)2 + 2NО2+ 2Н2О
3Сu + 8HNO3(разб) = 3Сu(NO3)2 + 2NО+ 4Н2О
5. Кислоты взаимодействуют с солями. При этом могут образоваться
а) новая кислота и средняя соль
BaCl2 + H2SO4 = BaSO4↓ + 2HCl
соль серная соль хлороводо -
хлорид кислота сульфат родная
бария разбав - бария кислота
ленная
б) новая кислота и кислая соль
NaCl + H2SO4(кон) = NaHSO4 + HCl
хлорид серная гидросуль - хлороводо -
натрия кислота фат родная
натрия кислота
в) только кислая соль
СаСО3 + Н2СО3 = Са (HСО3)2
карбонат угольная гидрокарбонат
кальция кислота кальция
6. Некоторые кислородсодержащие кислоты разлагаются на воду и кислотный оксид:
H2SO3 = H2O + SO2
Основания
Амфотерные гидроксиды
Гидроксиды, которые взаимодействуют с кислотами и щелочами с образованием солей, называются амфотерными.
C позиций теории электролитической диссоциации, амфотерными называются гидроксиды, которые при диссоциации образуют и катионы водорода и гидроксид-ионы.
К амфотерным гидроксидам относятся гидроксиды некоторых металлов главных подгрупп (бериллия, алюминия), а также некоторых металлов побочных подгрупп периодической системы элементов в промежуточных степенях окисления. Например,Ве(ОН)2,Al(ОН)3, Zn(OH)2, Ge(OH)2, Sn(ОН)4, Fе(ОН)3, Сr(ОН)3 — амфотерные гидроксиды.
Получение. Амфотерные гидроксиды нерастворимы в воде. Получают их, как и другие нерастворимые в воде основания, при взаимодействии солей со щелочами (чтобы получившийся гидроксид не растворился в избытке щелочи, берут эквивалентное количество щелочи). Например,
Cr2(SO4)3 + 6NaOH = 2Cr(OH)3¯ + 3Na2SO4
Химические свойства. В зависимости от условий амфотерные гидроксиды могут проявлять основные или кислотные свойства.
Al3+ + 3OH- « Al(OH)3 º Al(OH)3 + 3H2O « [Al(OH)4(H2O)2]- + H+
1. При взаимодействии с кислотами амфотерные гидроксиды проявляют основные свойства:
А1(ОН)3 + 3НС1 = А1С13 + 3Н2О
2. При взаимодействии со щелочами амфотерные гидроксиды проявляют кислотные свойства:
3А1(ОН)3 + 3NaOH = 3Na[Al(OH)4]
кислота основание тетрагидроксоалюминат натрия
Соли
Названия и формулы солей
Соли — это продукты замещения водорода кислоты металлом или гидроксогрупп оснований кислотными остатками.
Например,
H2SO4 + Zn = ZnSO4 + Н2
NaOH + НС1 = NaCl + H2O
С позиций теории электролитической диссоциации, соли – это электролиты, при диссоциации которых образуются катионы,отличные от катионов водорода, и анионы, отличные от анионов ОН- .
Классификация. Соли бывают средние, кислые, основные, двойные, комплексные.
Средняя соль — это продукт полного замещения водорода кислоты металлом или гидроксогруппы основания кислотным остатком. Например, Na2SO4, Ca(NO3)2 — средние соли.
Кислая соль — продукт неполного замещения водорода многоосновной кислоты металлом. Например, NaHSO4, Са(НСО3)2 — кислые соли.
Основная соль — продукт неполного замещения гидроксогрупп многокислотного основания кислотными остатками. Например, Mg(OН)С1, Bi(OH)Cl2 — основные соли
Если атомы водорода в кислоте замещаются атомами разных металлов или гидроксогруппы оснований замещаются различными кислотными остатками, то образуются двойные соли. Например, KAl(SO4)2, Са(ОС1)С1. Двойные соли существуют только в твердом состоянии.
Комплексные соли — это соли, в состав которых входят комплексные ионы. Например, соль K4[Fe(CN)6] — комплексная, так как в ее состав входит комплексный ион [Fe(CN)6]4-.
Составление формул солей. Можно сказать, что соли состоят из остатков оснований и остатков кислот. При составлении формул солей нужно помнить правило: абсолютная величина произведения заряда остатка основания на число остатков основания равна абсолютной величине произведения заряда кислотного остатка на число кислотных остатков. Для 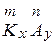 тх = пу, где K — остаток основания, A — кислотный остаток, т — заряд остатка основания, n — заряд кислотного остатка, х — число остатков основания, у — число кислотных остатков. Например,
тх = пу, где K — остаток основания, A — кислотный остаток, т — заряд остатка основания, n — заряд кислотного остатка, х — число остатков основания, у — число кислотных остатков. Например,
| Формулы: | 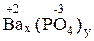 | 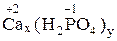 | 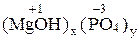 |
| 2x = 3y x = 3, y = 2 Ba3(PO4)2 | 2x = 1y x = 1, y = 2 Ca(H2PO4)2 | 1x = 3y x = 3; y = 1 (MgOH)3PO4 |
Номенклатура солей. Названия солей составляют из
названия аниона (кислотного остатка (табл.. 15)) в именительном падеже и названия катиона (остатка основания (табл. 17 )) в родительном падеже (без слова «ион»).
Для названия катиона используют русское название соответствующего металла или группы атомов (в скобках римскими цифрами указывают степень окисления металла, если это необходимо).
Анионы бескислородных кислот называют, используя окончание –ид (NH4F – фторид аммония, SnS – сульфид олова (II), NaCN – цианид натрия). Окончания названий анионов кислородсодержащих кислот зависят от степени окисления кислотообразующего элемента:
| Окончание названия кислоты | Название аниона |
| -ная, -овая | -ат |
| -истая | -ит |
| -оватистая | Гипо- + -ит |
Названия кислых и основных солей образуются по тем же общим правилам, что и названия средних солей. При этом название аниона кислой соли снабжают приставкой гидро-, указывающей на наличие незамещенных атомов водорода (число атомов водорода указывают греческими числительными приставками). Катион основной соли получает приставку гидроксо-, указывающую на наличие незамещенных гидроксогрупп.
Например,
MgС12 – хлорид магния
Ba3(РО4)2 – ортофосфат бария
Na2S – сульфид натрия
CaHPO4 – гидрофосфат кальция
K2SO3 – сульфит калия
Ca(H2PO4)2 – дигидрофосфат кальция
А12(SO4)3 – сульфат алюминия
Mg(OH)Cl – хлорид гидроксомагния
КА1(SO4)2 – сульфат калия-алюминия
(MgOH)2SO4 – сульфат гидроксомагния
KNaHPO4 – гидрофосфат калия-натрия
MnCl2 – хлорид марганца (II)
Са(OCI)C1 – хлорид-гипохлорит кальция
MnSO4 – сульфат марганца (II)
К2S – cульфид калия
NaHCO3 – гидрокарбонат натрия
К2SO4 – сульфат калия
Получение и свойства солей
Получение. Соли получают:
1. При взаимодействии металла с неметаллом:
Fe + S = FeS
2. При взаимодействии металла с кислотами:
Zn + 2НС1 = ZnCl2 + Н2
3. При взаимодействии металла с солями:
Сu + Hg(NО3)2 = Hg¯ + Сu(NO3)2
4. При взаимодействии металлов, оксиды которых амфотерны, со щелочами:
Zn + 2NaOH = Na2ZnO2 + Н2
5. При взаимодействии основных оксидов с кислотами:
СаО + 2НС1 = CaCl2 + H2О
6. При взаимодействии основныхоксидов с кислотными оксидами:
MgO + СO2 = MgСO3
7. При взаимодействии оснований с кислотами:
2КОH + H2SO4 = K2SO4 + 2H2O
КОН + H2SO4 = KHSO4 + Н2О
Bi(ОН)3 + HC1 = Bi(ОН)2С1 + Н2О
8. При взаимодействии оснований с кислотными оксидами:
NaОН + СO2 = NаНСО3
3NaОН + СО2 = Na2CO3 + H2O
9. При взаимодействии щелочей с солями:
CuCl2 + NaOH = СuОНСl + NaCl
CuCl2 + 2NaOH = Сu(ОН)2 + 2NaCl
10. При взаимодействии щелочей с неметаллами:
2NaOH + Cl2 = NaCl + NaClO + H2O
11. При взаимодействии солей с кислотами:
ВaС12 + Н2SO4 = ВaSO4¯ + 2НС1
12.При взаимодействии солей с кислотными оксидами:
Na2CO3 + SiO2 = Na2SiO3 ¯+ СО2
CaCO3 + CO2 + H2O = Ca(HCO3)2
13.При взаимодействии солей между собой:
Ва(NО3)2 + Na2SO4 = BaSO4 ¯ + 2NaNO3
14. При взаимодействии солей с неметаллами:
2KI + Сl2 = 2КСl + I2
Физические свойства. Соли — твердые кристаллические вещества. Остатки оснований и кислот в солях связаны между собой, как правило, ионной связью. Соли имеют разный цвет и характеризуется различной растворимостью в воде.
Химические свойства.
1. Соли реагируют со щелочами. При этом образуются новая соль и новое основание или основная соль:
MgCl2 + 2NaOH = Mg(OH)2 + 2NaCl
MgCl2 + NaOH = MgOHCl + NaCl
2. Соли взаимодействуют с кислотами. При этом образуются
а) новая кислота и новая средняя соль:
Ва(NO3)2 + H2SO4 = BaSO4¯+ 2HNO3
б) кислая и средняя соли
Са3(РO4)2 + 2Н2SO4 = Са(Н2РO4)2 + 2CaSO4
в) только кислая соль
Na2S + H2S = 2NaHS
3. Соли могут взаимодействовать между собой. При этом образуются новые соли. Реакции обмена между растворами солей идут до конца, если в результате реакции образуется нерастворимая соль:
CaCl2 + Nа2СО3 = СаСО3 ¯ + 2NaCl
4. Соли могут взаимодействовать с металлами.
CuSO4 + Fe = FeSO4 + Cu¯
Каждый металл может вытеснить из растворов солей все металлы, стоящие в ряду напряжений после него, и не может вытеснить металлы, стоящие перед ним:
FeSO4 + Сu ® реакция не идет
5. Некоторые соли разлагаются при нагревании:
СаСО3 = СаО + СО2
УПРАЖНЕНИЯ
1. Какие способы получения солей вызнаете?
2. Составьте уравнения реакций между следующими веществами:а) железоми хлороводородной кислотой; б) серной кислотой и гидроксидом натрия; в) хлоридом алюминия и гидроксидом калия; г) нитратомбарияи сульфатом натрия; д) хлоридом магния и нитратом серебра.
3. Напишите уравнения реакций, при помощи которыхможноосуществить следующиепревращения:
1) Сu ® СuО ® CuSO4 ® Сu(ОН)2 ® CuCl2 ® Сu
2) Zn ® ZnO ® ZnSO4 ® Zn(ОH)2 ® Na2 ZnO2
3) Р ® Р2О5®Н3РО4 ®Na3PO4 ®Са3(PO4)2
4) Mg ® МgО ® Mg(OH)2 ® MgCl2 ® Mg(NO3)2
Оксиды
Названия и формулы оксидов
Оксидами называются вещества, состоящие из двух элементов, один из которых кислород в степени окисления – 2. В оксидах атомы кислорода соединяются только с атомами других элементов и не связаны между собой.
Номенклатура. Названия оксидов элементов, имеющих постоянную степень окисления, составляются из двух слов
оксид + нaзвaние элемента в родительном падеже:
MgO — оксид магния, Na2O - оксид натрия, СаО - оксид кальция.
Если элемент образует несколько оксидов, то после названия элемента указывается его степень окисления римской цифрой в скобках: МnО — оксид марганца (II), Мn2О3 — оксид марганца (III).
Название оксидов можно также образовывать добавлением к слову «оксид» греческих числительных. Например, СО2 -диоксид углерода, SО2 — диоксид серы, SO3 — триоксид серы,OsO4 — тетраоксид осмия.
Классификация. По химическим свойствам оксиды делятся на солеобразующие и несолеобразующие. Оксиды, которые при химических реакциях образуют соли, называются солеобразующими:
CO2 + Са(ОН)2 = СaСО3¯ + H2O
оксид гидроксид карбонат
углерода кальция кальция
(IV)
MgO + 2HCl = MgCl2 + Н2О
оксид хлорово хлорид
магния дородная магния
кислота
СО2 и MgO — солеобразующие оксиды.
Оксиды, которые не образуют солей, называются несолеобразующими: NO — оксид азота (II), N2O — оксид азота (I), SiO — оксид кремния (II) — это несолеобразующие оксиды. Несолеобразующих оксидов мало.
Получение и свойства оксидов
Получение. Оксиды получаются:
а) при взаимодействии простых веществ с кислородом:
4А1 + 3O2 = 2А12О3
4Р + 5O2 = 2Р2O5
Исключениями благородные металлы (Au, Pt) и щелочные металлы (кроме Li)
2Na + O2 = Na2O2
2Na + H2O2 = Na2O + H2O
б) при взаимодействии сложных веществ с кислородом:
СН4 + 2O2 = СO2 + 2Н2О
2Н2S +3O2 = 2Н2О + 2SO2
в) при разложении сложных веществ:
-оснований
Fe(OH)2↓ 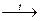 FeO + H2O
FeO + H2O
-кислот
H2SO3 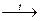 SO2 + H2O
SO2 + H2O
-солей
СaCO3↓ 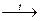 CaO + CO2
CaO + CO2
г) при некоторых других реакциях:
3P + 5HNO3 + 2H2O = 3H3PO4 + 5NO
Солеобразующие оксиды делятся на основные, кислотные и амфотерные.
Химические свойства основных оксидов. К основным оксидам относятся только оксиды металлов: щелочных (Li, Na, К, Rb, Cs, Fr), щелочноземельных (Mg, Ca, Sr, Ba, Ra), лантана, а также всех остальных металлов в их низших степенях окисления. Например, Na2O, CaO, Cu2O, CrO, MnO, BaO, La2O3 — основные оксиды.
1. Оксиды щелочных и щелочноземельных металлов взаимодействуют с водой. При этом образуются их гидраты — растворимые в воде основания (щелочи). Например,
Na2O + H2O = 2NaOH
оксид гидроксид
натрия натрия
СаО + Н2O = Са(ОН)2
оксид гидроксид
кальция кальция
CuO + 2HCl = CuCl2 + H2O
CuCl2 + 2KOH = Cu(OH)2 + 2KCl
Основные оксиды многих других металлов с водой не взаимодействуют. Их гидраты получают косвенным путем. Гидраты всех основных оксидов являются основаниями:
Na2О ® NaOH CaO ® Ca(OH)2
оксид основание оксид основание
натрия гидроксид кальция гидроксид
натрия кальция
2. Основные оксиды взаимодействуют с кислотами. При этом образуются соль и вода:
CaO + 2НС1 = СаС12 + Н2О
оксид хлорово– соль
кальция- дородная хлорид
кислота кальция
BaO + 2HNO3 = Ba(NO3)2 + H2O
оксид азотная соль нитрат
бария кислота бария
Химические свойства кислотных оксидов. К кислотным оксидам относятся оксиды неметаллов, а также металлов в высших степенях окисления. Например, SO2, SО3, СО2, СrО3, Mn2O7 — кислотные оксиды.
1. Большинство кислотных оксидов взаимодействуют с водой. При этом образуются кислоты:
SO2 + Н2О = H2SO3
оксид сернистая
серы (IV) кислота
Р2O5 + 3Н2O = 2Н3РO4
оксид ортофосфорная
фосфора (V) кислота
Некоторые кислотные оксиды (например, SiO2) не взаимодействуют с водой.
K2O + SiO2 = K2SiO3
K2SiO3 + 2HCl = H2SiO3↓ + KCl
2. Кислотные оксиды взаимодействуют с растворимыми в воде основаниями. При этом образуются соль и вода:
SO2 + 2NaOH = Na2SO3 + Н2О
оксид гидроксид соль
серы(IV) натрия сульфит
натрия
Р2O5 + 3Са(ОН)2 = Са3(РO4)2 + 3Н2О
оксид гидроксид соль орто-
фосфора кальция фосфат
(V) кальция
3. Кислотные и основные оксиды могут взаимодействовать между собой. При этом образуется соль:
MgO + SO2 = MgSO3
основной кислотный соль
оксид оксид сульфит
магния серы (IV) магния
Химические свойства амфотерных оксидов. К амфотерным оксидам относятся оксиды некоторых металлов главных подгрупп (оксиды бериллия, алюминия), а также оксиды некоторых металлов побочных подгрупп периодической системы элементов Д. И. Менделеева в промежуточных степенях окисления. Например, ВеО, А12O3, ZnO, МnО3, Fе2О3, Сr2О3 — амфотерные оксиды.
1. Амфотерные оксиды взаимодействуют с кислотами. При этом образуются соли:
ZnO + 2HCI = ZnCl2 + Н2О
оксид хлороводородная соль
цинка кислота хлорид цинка
2. Амфотерные оксиды взаимодействуют со щелочами. При этом тоже образуются соли:
- в расплаве
ZnO + 2NaOH = Na2ZnO2 + H2O
оксид гидроксид соль
цинка натрия цинкат натрия
- в растворе
ZnO + 2NaOH + H2O = Na2[Zn(OH)4]
После сравнения химических свойств оксидов можно сделать следующие определения:
1. Оксиды, которые образуют соли только с кислотами или кислотными оксидами, называются основными.
2. Оксиды, которые образуют соли только с основаниями или основными оксидами, называются кислотными.
3. Оксиды, которые взаимодействуют и с кислотами и со щелочами и при этом образуют соли, называются амфотерными.
Как мы видим, основные и кислотные оксиды имеют противоположные свойства. Амфотерные оксиды в зависимости от условий могут проявлять свойства основных или кислотных оксидов.
Кислоты
Названия и формулы кислот
Кислотами называются соединения, в состав которых входят атомы водорода, способные замещаться атомами металла. При этом образуются соли.
Например,
2НС1 + Mg ® MgС12 + Н2↑
С позиций теории электролитической диссоциации, кислотами называются электролиты, при диссоциации которых в качестве катионов образуются только ионы водороды, способные замещаться на атомы металла.
Классификация. Кислоты различают:
1) по наличию или отсутствию кислорода в составе кислоты
а) бескислородные (это водные растворы водородных соединений неметаллов VI и VII групп периодической системы элементов Н2S, H2Se, H2Te, HF, HC1, HBr, HI, a также HSCN и HCN);
б) кислородсодержащие (это гидраты оксидов неметаллов, а также некоторых металлов в высших степенях окисления (+5, +6, +7) - Н2СО3, H2SO4, H2СrО4 и т.д.).
2) по основности (т.е. по числу атомов водорода в молекуле кислоты, способных замещаться атомами металлов с образованием соли)
а) одноосновные (HCl, HNO3, HCN, CH3COOH),
б) двухосновные (H2S, H2SO4, H2СО3),
в) трехосновные (H3РО4, Н3AsO4) и т.д.
Номенклатура.
а) Названия бескислородных кислот составляют из
названия элемента + О + слово «водородная»:
НCl – хлороводородная кислота, H2S – сероводородная кислота, HCN – циановодородная кислота, HI – йодоводородная кислота.
б) Названия кислородсодержащих кислот образуют от
русского названия элемента + «кислота».
При этом название кислоты, в которой элемент имеет высшую степень окисления, оканчивается на –наяили-овая(H2SO4 – серная кислота, HClO4- хлорная кислота, H3AsO4 – мышьяковая кислота). С понижением степени окисления элемента окончания изменяются так: - оватая (HСlO3 – хлорноватая кислота), -истая (HСlO2 – хлористая кислота), -оватистая(HOCl – хлорноватистая кислота). Если элемент образует кислоты, находясь только в двух степенях окисления, то название кислоты, отвечающей низшей степени окисления, получает окончание –истая (HNO3 – азотная кислота, HNO2 – азотистая кислота)
Кислотные остатки. Отрицательно заряженные группы атомов и одиночные атомы (отрицательные ионы), которые остаются после отрываот молекулы кислоты одного или нескольких атомов водорода, называются кислотными остатками.
Величина отрицательного заряда кислотного остатка определяется числом атомов водорода, замещенных металлом (табл.15).
Таблица 15. Названия и формулы некоторых кислотных остатков.
| Формула кислоты | Название кислоты | Кислотный остаток | Название кислотного остатка | |
| HCl | Хлороводородная (соляная) | Cl- | Хлорид-ион | |
| HBr | Бромоводородная | Br- | Бромид-ион | |
| HI | Йодоводородная | I- | Йодид-ион | |
| H2S | Сероводородная | HS- | Гидросульфид-ион | |
| S2- | Сульфид-ион | |||
| HClO | Хлорноватистая | ClO- | Гипохлорит-ион | |
| HClO2 | Хлористая | ClO 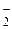 | Хлорит-ион | |
| HClO3 | Хлорноватая | ClO 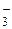 | Хлорат-ион | |
| HClO4 | Хлорная | ClO 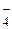 | Перхлорат-ион | |
| H2SO3 | Сернистая | HSO 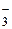 | Гидросульфит-ион | |
SO 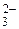 | Сульфит-ион | |||
| H2SO4 | Серная | HSO 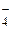 | Гидросульфат-ион | |
SO 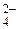 | Сульфат-ион | |||
| HNO2 | Азотистая | NO 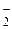 | Нитрит-ион | |
| HNO3 | Азотная | 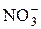 | Нитрат-ион | |
| H3PO4 | Ортофосфорная | 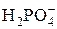 | Дигидрофосфат-ион | |
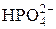 | Гидрофосфат-ион | |||
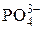 | Ортофосфат-ион | |||
| H2CO3 | Угольная | 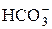 | Гидрокарбонат-ион | |
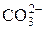 | Карбонат-ион | |||
| H2SiO3 | Кремниевая | 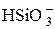 | Гидросиликат-ион | |
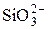 | Силикат-ион | |||
| HMnO4 | Марганцовая | 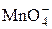 | Перманганат-ион | |
| H3BO3 | Борная (ортоборная) | 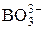 | Борат-ион | |
| H2CrO4 | Хромовая | 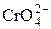 | Хромат-ион | |
| H2Cr2O7 | Дихромовая | 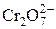 | Дихромат-ион | |
| HCN | Циановодородная (синильная) | 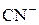 | Цианид-ион |
Получение и свойства кислот
Получение. 1. Кислородсодержащие кислоты можно получить при взаимодействии кислотных оксидов с водой
P2O5 + 3H2O = 2H3PO4 SO2 + H2O = H2SO3
оксид ортофосфорная оксид сернистая
фосфора (V) кислота серы (IV) кислота
2. Бескислородные кислоты получаются при растворении в воде продуктов соединения неметаллов с водоро
