Тема: УСТАНОВЛЕНИЕ ФОРМУЛЫ КРИСТАЛЛОГИДРАТА
Формула химического соединения показывает, из каких элементов состоит данное вещество и сколько атомов каждого элемента входит в состав его молекулы или формульной единицы. Массовые соотношения элементов в молекулах можно представить как отношение произведе-ний соответствующих атомных масс на число атомов каждого элемента в молекуле, т.е. можно записать:
m1 :m2 :m3 = xA1 :yA2 :zA3,
где m1, m2, m3 – содержание элементов в соединении (%); x, y, z – число атомов этих элементов в молекуле или в формульной единице; А1, А2, А3 – атомные массы элементов. Из этого уравнения следует
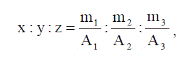
что позволяет находить отношение между числами атомов в молекуле.
Пример. Необходимо определить формулу вещества, которое содержит натрий (32,43%), серу (22,55 %) и кислород (45,02 %).
Соотношение чисел атомов в формуле данного соединения:
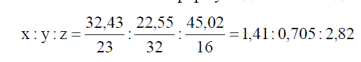
Если самое меньшее число (0,705) принять за единицу, то данное отношение становится отношением целых чисел:
x :y :z = 2 :1 :4,
следовательно, формула соединения Na2SO4. Эта формула будет простейшей, поскольку полученное соотношение может быть выражено также и числами, кратными найденным.
Для установления истинной, или молекулярной, формулы необходимо знать молекулярную (молярную) массу соединения; это позволяет найти истинное соотношение атомов в молекуле. Так, например, бензол содержит углерод (92,3 %) и водород (7,7 %). Найденная из этого состава простейшая формула СН. Но в действительности молекулярная масса бензола, определяемая по плотности его пара, равна не 13 (12 + 1), а 78. Следовательно, истинная формула бензола С6Н6.
Кристаллогидратами называются кристаллические вещества, включающие молекулы воды, например гипс CaSO4·2Н2О, медный купорос CuSO4·5Н2О и т.д. Кристаллогидраты при нагревании теряют кристаллизационную воду, переходя в безводные соли. Пользуясь этим, можно определить содержание воды в кристаллогидрате, а затем, зная формулу безводной соли, рассчитать число молекул воды, присоединяющихся к одной молекуле безводной соли.
Экспериментальная часть
Целью работы является определение количества (моль) воды в кристаллогидрате – медном купоросе.
Ход работы.
1. Взвесить пустой фарфоровый тигель с точностью до 0,01 г. Во взвешенный тигель насыпать 0,5–1 г медного купороса. Тигель с кристаллогидратом снова взвесить.
2. Поместить тигель в нагретую песочную баню на 20–30 минут.
3. Перенести щипцами тигель в эксикатор и охладить.
4. Взвесить охлажденный тигель.
5. Повторить прогревание тигля, снова охладить его в эксикаторе и взвесить. Если масса изменилась не более чем на 0,01 г, прогревание прекратить. По результатам последнего взвешивания заполнить таблицу результатов опыта:
| Масса пустого тигля, г | Масса тигля с кристаллогидратом, г | Масса кристаллогидрата, г | Масса тигля с веществом после прокаливания, г | Масса безводной соли, г | Масса воды, г |
6. Вычислить количество воды, приходящееся на один моль CuSO4, и записать формулу медного купороса, определенную опытным путем.
7. Определить относительную погрешность опыта, исходя из того, что реальная формула медного купороса CuSO4·5Н2О.
8. Сделать вывод о проделанной работе.
Дополнительные задания к лабораторной работе
1. Какие вещества называются кристаллогидратами? Приведите примеры кристаллогидратов.
2. Расположите по увеличению количества сульфаты натрия, лития, бария, цезия, если их массы одинаковы.
3. Для чего применяются в химическом эксперименте тигель, эксикатор, песчаная баня.
4. Какова формула соединения водорода с кислородом, если мольное соотношение Н:О = 1:1, а плотность его газа по водороду равна 17?
5. Определить формулу кристаллической соды, если при нагревании 286 г данной соли образовалось 106 г карбоната натрия.
Лабораторная работа №3
