Как можно доказать наличие белков в продуктах питания, в шерстяных и шелковых тканях?
Билет 1
1. Общие представления о высокомолекулярных соединениях (ВМС), основные понятия и определения.
Высокомолекулярные соединения (ВМС)– вещества, состоящие из молекул больших размеров, большой молекулярной массы. Подавляющую часть ВМС составляют полимеры, хотя достаточно высокую молекулярную массу (более 1000) могут иметь и молекулы веществ неполимерной природы, например сложные производные сахаров.
Полимер – неорганические и органические, аморфные и кристаллические вещества, состоящие из мономерных звеньев, соединенных в длинные макромолекулы химическими или координационными связями.
Олигомер – молекула в виде цепочки из небольшого числа одинаковых составных звеньев. Этим олигомеры отличаются от полимеров, в которых число звеньев теоретически не ограничено.
Мономер — низкомолекулярное вещество, из которого в результате реакции полимеризации или поликонденсации получают полимер.
Степень полимеризации— число мономерных звеньев, образующих макромолекулу.
Структурное (элементарное) звено— повторяющийся участок структуры молекулы полимера. Например, в структуре политетрафторэтилена (тефлона) (-CFj-CF,-),,, получающегося полимеризацией тетрафторэтнлена CF,=CF,. в качестве структурного звена рассматривают группу -CF,-CF2-
Линейныеполимеры. Макромолекулы линейных полимеров не имеют разветвлении, поэтому способны плотно упаковываться при затвердевании вещества. Материалы из линейных полимеров прочны на разрыв, имеют высокую температуру плавления и плотность. Из них изготавливают волокна и пленки. Пример таких полимеров — полиэтилен ннзкого давления.
Разветвленные полимеры. Макромолекулы имеют коро ткие боковые разветвления, поэтому упаковываются более разреженно. Материалы из них имеют более низкую прочность, плотность и температуру плавления. Пример — полиэтилен высокого давления.
Сетчатые (сшитые) полимеры. Твердые хрупкие вещества. Не способны плавиться без разложения, растворя гься и образовывать волокна. Пример — фе- нолформальдегидная смола.
2.Уникальные свойства биополимеров.
Некоторые биополимеры обладают уникальными свойствами – способностью к биоразложению и биологической совместимостью, что делает их предпочтительным, а в отдельных случаях незаменимым материалом во многих отраслях, и позволяет постепенно завоёвывать рынок, вытесняя полимерные материалы, не обладающие данными свойствами. Б. обладают рядом уникальных свойств, не характерных для низкомолекулярных соединений. Назовём некоторые из важнейших свойств биополимеров и их функции:
- нуклеиновые кислоты способны кодировать, хранить и передавать генетическую информацию на молекулярном уровне, являясь материальным субстратом наследственности;
- другой класс биополимеров -мышечные белки, способные превращать химическую энергию в механическую работу; эта их сократительная функция лежит в основе мышечной деятельности белков;
- ферменты, глобулярные белки, обладают каталитической функцией, они с большей скоростью и избирательностью осуществляют в живой природе все химические реакции обмена, распада одних и синтеза других веществ.
Все перечисленные выше особенности свойств полимеров связаны с их цепным строением. Именно цепное строение молекул полимеров является их важнейшим свойством.
Ограниченное набухание.
Ограниченное набухание – процесс взаимодействия полимеров с низкомолекулярными жидкостями, не сопровождающийся растворением. Это наблюдается при невысоком термодинамическом сродстве полимера и растворителя, а также характерно для полимеров, макромолекулы которых соединены прочными поперечными связями в пространственную сетку. Редкие поперечные связи между макромолекулами на первой стадии набухания полимера не затрудняют диффузию в него молекул растворителя. Поэтому в первый период набухание происходит с максимальной скоростью. Однако сольватация растворителя звеньями макромолекул, расположенными между узлами сетки, снижает их подвижность, приводит к увеличению расстояний между ними, к растяжению и распрямлению макромолекул, уменьшению энтропии системы, появлению сильных механических напряжений и разрыву некоторых перенапряженных участков; скорость набухания при этом уменьшается. При определенном давлении набухания процесс прекращается. В этот момент система приходит в равновесие, при котором увеличение энтропии вследствие перемешивания молекул растворителя и сегментов макромолекул равно уменьшению энтропии в результате растяжения сегментов.
Билет 2
Функции белков в организме.
1. Каталитическая функция белков. Все биологические катализаторы - ферменты являются белками. В настоящее время охарактеризовано тысячи ферментов, многие из них выделены в кристаллической форме. Почти все ферменты - мощные катализаторы, повышающие скорости реакций, по крайней мере, в миллион раз. Эта функция белков является уникальной, не свойственной другим полимерным молекулам.
2. Питательная (резервная функция белков). Это, прежде всего белки, предназначенные для питания развивающегося зародыша: казеин молока, овальбумин яиц, запасные белки семян растений. Ряд других белков, несомненно, используется в организме в качестве источника аминокислот, которые, в свою очередь, являются предшественниками биологически активных веществ, регулирующих процесс обмена веществ.
3. Транспортная функция белков.Транспорт многих небольших молекул и ионов осуществляется специфическими белками. Например, дыхательная функция крови, а именно перенос кислорода, выполняется молекулами гемоглобина - белка эритроцитов. В транспорте липидов принимают участие альбумины сыворотки крови. Ряд других сывороточных белков образует комплексы с жирами, медью, железом, тироксином, витамином А и другими соединениями, обеспечивая их доставку в соответствующие органы.
4. Защитная функция белков. Основную функцию защиты выполняет иммуннологическая система, которая обеспечивает синтез специфических защитных белков - антител - в ответ на поступление в организм бактерий, токсинов или вирусов (антигенов). Антитела связывают антигены, взаимодействуя с ними, и тем самым нейтрализуют их биологическое действие и сохраняют нормальное состояние организма. Свертывание белка плазмы крови - фибриногена - и образование сгустка крови, предохраняющего от потери крови при ранениях - еще один пример защитной функции белков.
5. Сократительная функция белков. В акте мышечного сокращения и расслабления участвует множество белков. Главную роль в этих процессах играют актин и миозин - специфические белки мышечной ткани. Сократительная функция присуща также и белкам субклеточных структур, что обеспечивает тончайшие процессы жизнедеятельности клеток,
6. Структурная функция белков. Белки с такой функцией занимают первое место среди других белков тела человека. Широко распространены такие структурные белки, как коллаген в соединительной ткани; кератин в волосах, ногтях, коже; эластин - в сосудистых стенках и др.
7. Гормональная (регуляторная) функция белков. Обмен веществ в организме регулируется разнообразными механизмами. В этой регуляцииважное место занимают гормоны, вырабатываемые железами внутреннейсекреции. Ряд гормонов представлен белками, или полипептидами, например гормоны гипофиза, поджелудочной железы и др
Радикальная полимеризация.
Радикальная полимеризация.Этапы:
-образование активных центров(генерирование свободных радикалов)
осуществляется в результате теплового, светового, радиоактивного или
химического воздействий (соответственно термо-, фото-, радио- и
хемоинициирование.
- рост цепи– основная стадия радикальной полимеризации: неспаренный
электрон переходит от атома углерода радикала R• к концевому атому
молекулы мономера, превращая растущую цепь в макрорадикал, к которому
последовательно присоединяются молекулы мономера
RM•+ M →RMM• (к2).
Скорость стадии определяется по формуле V2=k2[M][RM •]
При этом принимается, что константа k2 не зависит от длины макрорадикала (это справедливо при n>3-5). Величина k2 зависит от реакционной способности мономера и макрорадикала.
- обрыв цепи– заключительная стадия полимеризации. При этом могут протекать две реакции — диспропорционирования или рекомбинации либо обрыв цепи происходит в реакции передачи цепи.
Скорость реакции обрыва цепи определяется уравнением V3=k3[M • ]2
k3=k3a+k3б
Для регулирования длины цепи (принудительный обрыв цепи)
используют реакцию передачи цепи, когда вводимое вещество– регулятор – обрывает растущую цепь, становясь при этом свободным радикалом, начинающим новую цепь реакции полимеризации.
Передача цепи.
Стадия передачи цепи заключается в переносе активного центра макрорадикала на другую молекулу, присутствующую в растворе (мономер, полимер, инициатор, растворитель).
Билет 3
Функции нуклеиновых кислот
Нуклеиновым кислотам присущи три важнейшие функции: хранение, передача и реализация генетической информации. Кроме этих, они выполняют и другие функции, например, участвуют в катализе некоторых химических реакций, осуществляют регуляцию реализации генетической информации, выполняют структурные функции и др. Роль хранителя генетической информации у большинства организмов (эукариот, прокариот, некоторых вирусов) выполняют двухцепочечные ДНК. Только у некоторых вирусов хранителем генетической информации являются одноцепочечные ДНК или одноцепочечные, а также двухцепочечные РНК. Генетическая информация записана в генах. Ген по своей природе является участком нуклеиновой кислоты. В них закодирована первичная структура белков. Гены могут также нести информацию о структуре некоторых типов РНК, например, тРНК и рРНК.
Генетическая информация передается от родителей к потомкам. Этот процесс связан с удвоением нуклеиновой кислоты (ДНК или РНК), выполняющей функцию хранителя генетической информации, и последующей передачи ее потомкам. Например, в результате деления дочерние клетки получают от материнской идентичные молекулы ДНК, а следовательно, и идентичную генетическую информацию (рис. 38). При размножении вирусы также передают дочерним вирусным частицам точные копии нуклеиновой кислоты. При половом размножении потомки получают генетическую информацию от обоих родителей. Вот почему дети наследуют признаки обоих родителей.
Катионная полимеризация.
Катионная полимеризация. При катионной полимеризации растущая цепь на конце имеет положительный заряд. В качестве катализаторов используются соединения, обладающие электроноакцепторными свойствами – протонные кислоты, кислоты Льюиса, совместно с сокатализаторами. По катионному механизму легко полимеризуются виниловые и дивиниловые соединения с электродонорными заместителями (алкил, винил, фенил) у двойной связи (изобутилен, α-метилстирол, винилалкиловые эфиры и др.), а также некоторые карбонильные соединения (формальдегид), гетероциклические мономеры (окись этилена, окись пропилена, тетрагидрофуран и т.д.). Катионную полимеризацию винилового мономера в присутствии и небольших количеств воды (сокатализатора) можно представить следующим образом. Инициирование: а) взаимодействие катализатора и сокатализатора с образованием комплексного соединения, которое проявляет свойства сильной кислоты:10 б) взаимодействие этого комплексного катализатора с молекулой мономера и превращение последнего в карбониевый ион путем передачи протона: Рост цепи - это последовательное присоединение молекул мономера, внедряющихся между макрокарбкатионом и противоионом: Обрыв цепи при катионной полимеризации, в отличие от радикальной полимеризации, не является бимолекулярной, так как два одинаково заряженных активных центров не могут взаимодействовать. Остановка роста цепи идет по мономолекулярному механизму, чаще в результате реакции макрокатиона с противоионом, либо путем передачи цепи на мономер, растворитель и т.д.
Билет 4
Анионная полимеризация.
нионная полимеризация — это процесс образования макромолекул, в котором активные центры несут отрицательный заряд.

Основные катализаторы:
1. Щелочные металлы
2. Амиды щелочных металлов

3. Na- и Li-органические соединения, н-р: Na-нафталиновый комплекс.
4. Алкоголяты
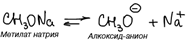
Анионная полимеризация характерна для винильных соединений с электроноакцепторными заместителями: акрилонитрила, алкилакрилатов, стирола и др
Основные стадии:
1. Инициирование
2. Рост цепи
3. Реакция обрыва цепи (протекает с участием растворителя, например аммиаком)
Билет 5
Неограниченное набухание.
Неограниченное набухание– это набухание, самопроизвольно переходящее в растворение. Оно аналогично неограниченному смешению жидкостей, например воды и этилового спирта. Неограниченное набухание характерно для линейных аморфных полимеров с невысокой степенью полимеризации, сольватированные макромолекулы которых легко и быстро могут переходить в раствор. Степень набухания, после которой начинается растворение, должна быть достаточной для полной сольватации макромолекул и их отделения от остальной массы набухающего полимера, т.е. растворения. Таким образом, вокруг набухающего образца полимера образуется слой
раствора полимера.
В результате диффузии макромолекулы равномерно распределяются по всему объему растворителя и в конце растворения образуют однофазную гомогенную систему. Кинетика набухания некоторых полимеров показана на рис. 1.
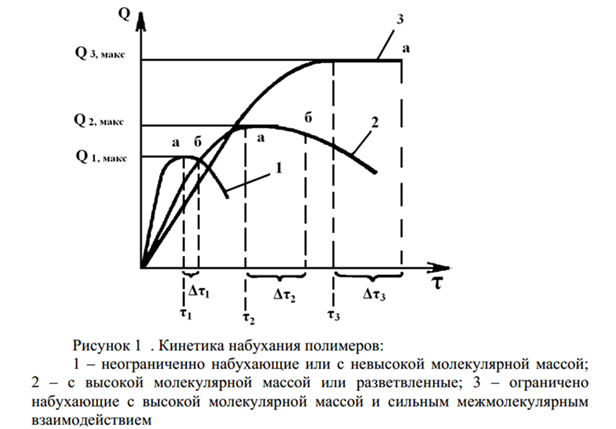
До точки а для всех полимеров наблюдается постепенно замедляющееся увеличение степени набухания (вследствие более интенсивного набухания в начале процесса). В точке а скорость растворения становится равной скорости набухания и некоторое время степень набухания не изменяется. В точке б скорость растворения начинает превышать скорость набухания, и масса образцов уменьшается. Между точками аи б образцы имеют максимальную степень набухания Qмакс. в течение времени Δτ. Из сопоставления кривых набухания можно сделать вывод, что чем ниже молекулярная масса, меньше разветвленность макромолекул и межмолекулярное взаимодействие и выше термодинамическое сродство между полимером и растворителем – тем меньше
Qмакс. и Δτ. При очень высокой молекулярной массе или сильном межмолекулярном взаимодействии некоторые полимеры (например, белки) растворяются крайне медленно (кривая 3) и могут сохранять максимальную степень набухания в течение длительного времени, т.е. Характеризуются ограниченным набуханием. Для растворения таких набухших полимеров требуется перемешивание, повышенная температура; при этом межмолекулярное взаимодействие ослабляется и повышается подвижность макромолекул, что ускоряет их растворение.
Билет 6
Понятие о дендримерах.
Одним из элементов наномира являются дендримеры (древообразные полимеры) – наноструктуры размером от 1 до 10 нм, образующиеся при соединении молекул, обладающих ветвящейся структурой. Синтез дендримеров – это одна из нанотехнологий, тесно соприкасающихся с химией – химией полимеров. Как и все полимеры, дендримеры состоят из мономеров, но молекулы этих мономеров имеют ветвистую структуру. Дендример становится похожим на дерево с шарообразной кроной, если в процессе роста полимерной молекулы не происходит соединения растущих ветвей (подобно тому, как ветви одного дерева, или кроны рядом стоящих деревьев не срастаются). Внутри дендримера могут образовываться полости, заполненные веществом, в присутствии которого дендримеры были образованы. Если дендример синтезирован в растворе, содержащем какой-либо лекарственный препарат, то этот дендример становится нанокапсулой с данным лекарственным препаратом. Кроме того, полости внутри дендримера могут содержать вещества с радиоактивной меткой, применяемые для диагностики различных заболеваний.
Учёные считают, что, заполняя полости дендримеров необходимыми веществами, можно, например, с помощью сканирующего зондового микроскопа собирать из различных дендримеров наноэлектронные схемы. При этом дендример, заполненный медью, мог бы служить проводником и т.п.
Конечно, многообещающим направлением в применении дендримеров является их возможное использование в качестве нанокапсул, доставляющих лекарства непосредственно клеткам, нуждающимся в этих препаратах. Центральная часть таких дендримеров, содержащая лекарство, должна быть окружена оболочкой, предотвращающей утечку лекарства, к внешней поверхности которой необходимо прикрепить молекулы (антитела), способные прилипать именно к поверхности клеток – адресатов. Как только такие нанокапсулы-дендримеры достигнут и прилипнут к больным клеткам, необходимо уничтожить внешнюю оболочку дендримера, например, с помощью лазера или сделать эту оболочку саморазлагающейся.
Первичная структура белка.
Первичная структура белков – последовательность аминокислот в полипептидной
цепи (или цепях) и положение дисульфидных связей, если они есть .
Свойства первичной структуры:
1) Последовательность аминокислот в первичной структуре белка является
специфической видовой характеристикой данного белка.
2) Первичная структура белка является основой для формирования последующих
структур белка за счёт взаимодействия радикалов аминокислотных остатков
полипептидной цепи.
Коллоидные растворы.
Наряду с растворами полимеров широкое применение находят и различные полимерные гетерогенные коллоидные системы, характеризующиеся коллоидной степенью дисперсности. Это означает, что частицы в таких системах представляют собой не отдельные макромолекулы, как в растворах, а их агрегаты. Эти агрегаты нерастворимы в жидкой среде, называемой дисперсионной средой, и образуют в ней отдельную дисперсную фазу. Состав и свойства коллоидных систем существенно отличаются от состава и свойств истинных растворов. Специфической особенностью дисперсных систем является их агрегативная неустойчивость, т.е. способность к разрушению, разделению на отдельные фазы – дисперсионную среду и дисперсную фазу. Разрушение коллоидных систем легко происходит при введении в них электролитов, а также при изменении температуры и других факторов. При разрушении системы отдельные частицы дисперсной фазы соединяются друг с другом, что приводит к снижению степени их дисперсности, отделению дисперсной фазы от дисперсионной среды.
Процесс разрушения коллоидной системы с выделением из дисперсионной среды дисперсной фазы называют коагуляцией, а выделившуюся дисперсную фазу – коагулятом. Неустойчивость коллоидных систем объясняется большой, всегда положительной свободной поверхностной энергией, сосредоточенной на межфазной поверхности раздела. В соответствии с законами термодинамики такие системы неравновесны и стремятся перейти в состояние, соответствующее минимальной свободной энергии, т.е. разделиться на отдельные фазы с минимальной поверхностью раздела. В реальных условиях устойчивость коллоидных систем играет громадную роль. Она зависит от сроков и условий их транспортирования, хранения, переработки.
Изменения структуры коллоидных систем, приводящие к их разрушению, в различных условиях различны и зависят от соотношения и природы сил, действующих между диспергированными частицами. Это могут быть силы сцепления и силы отталкивания. Силы сцепления обычно проявляются при наличии межмолекулярного взаимодействия. Они сильно возрастают при сближении частиц, вызывая их слияние, коагуляцию. Поэтому устойчивость коллоидных систем резко снижается при увеличении концентрации.
Билет 7
Понятие о стереорегулярности полимеров. Примеры.
Стереорегуля́рные полиме́ры (изотактические и синдиотактические) высокомолекулярные полимеры, макромолекулы которых состоят из одинаковых по химическому составу звеньев, имеющих одинаковую (или разную, но чередующуюся в определенной периодичности) пространственную конфигурацию. В таких полимерах все заместители (например, группы –СН3 у полипропилена) расположены в пространстве в каком-то одном, строго определенном порядке, например, мономеры объединены «голова к хвосту». Если при этом все заместители находятся по одну сторону относительно оси молекулярной цепи, то такие полимеры имеют очень высокую стереорегулярность и называются изотактическими. К таким полимерам относятся, например, 1,4-цис- и 1,4-транс-полидиены.
В синдиотактических полимерах заместители у одних мономеров находятся по одну сторону оси молекулярной цепи, у других — по другую сторону.
Стереорегулярные полимеры способны кристаллизоваться, и в ряде случаев стереорегулярность молекулы является необходимым условием реализации кристаллического состояния полимера. Именно в способности образовывать трехмерные кристаллы заключается наиболее существенное отличие стереорегулярных полимеров от нерегулярных (атактических). В низкомолекулярных соединениях нет прямой взаимосвязи между конфигурацией молекул и их способностью к кристаллизации. Мономерные звенья в макромолекулах не могут принимать любые положения, необходимые для вхождения в кристаллическую решетку, без разрыва основной цепи. Поэтому конформация макромолекулы зависит от ее конфигурации, и в общем случае, отсутствие стереорегулярности не позволяет макромолекуле принять регулярную конформацию, необходимую для построения кристалла.
К числу стереорегулярных полимеров относятся, например, изотактический полипропилен, синдиотактический поливинилхлорид, стереорегулярный бутадиеновый каучук, а также некоторые природные полимеры, например целлюлоза, каучук натуральный.
Вторичная структура белка.
Часто в полипептидных цепях содержатся участки, последовательность аминокислотных
остатков которых, образует локально упорядоченные трёхмерные структуры.
Совокупность таких упорядоченных структур называютвторичной структурой
белков.
В результате совокупности действия таких факторов, как - плоское строение пептидной
связи, возможность свободного вращения связей у α-углеродного атома,постоянство
углов и межатомных расстоянийформируются следующие типы вторичной структуры
белков: α-спираль, β-структура и β-складка.
Одним из основных элементов вторичной структуры белков является α‑спираль. Это — правая спираль, которую можно себе представить в виде пептидной цепи,
закрученной вокруг воображаемого цилиндра.
Характеристики α-пирали:
- содержит3,6 аминокислотного остатка на виток с периодом повторяемости 5,4 нм;
- полипептидный остов образует плотные витки вокруг длинной оси молекулы;
- боковые радикалы выступают наружу;
- спираль удерживается водородными связями между группами N-H одной пептидной
связи и кислородом группы С=О, принадлежащей другой пептидной связи, расположенной через четыре аминокислотных остатка над первой в следующем витке спирали;
- в α-спирали полностью использована возможность образования водородных связей
(внутримолекулярные), поэтому она не способна образовывать водородные связи с
другими элементами вторичной структуры.
Степень спирализации в белках колеблется от 5 до 80%.
(При графическом изображении спиральные участки изборажаются цилиндром).
β -структура является вторым элементом вторичной структуры белков. β -складчатые
структуры – графически изображаются стрелкой
Дисперсии и эмульсии.
По строению и степени дисперсности гетерогенные коллоидные полимерные системы подразделяют на дисперсии и эмульсии. Дисперсии и эмульсии – устойчивые коллоидные системы с размерами частиц 0,1 мкм – 1 нм; дисперсная фаза в дисперсиях – твердая, в эмульсиях– жидкая. В состав этих систем входят три компонента– дисперсная фаза, дисперсионная среда, эмульгатор. Молекулы эмульгатора имеют полярные и неполярные участки, взаимодействующие с разными фазами. Агрегативная устойчивость эмульсий обусловлена многими факторами. В определенных условиях они могут самопроизвольно образовываться в двухкомпонентной гетерогенной системе (без эмульгатора). Например, гетерогенная система вода– фенол самопроизвольно переходит в термодинамически устойчивую эмульсию, если межфазное натяжение настолько мало, что оно полностью компенсируется энтропийным фактором. Таким же свойством обладают коллоидные системы поверхностно-активных веществ (ПАВ) и растворы полимеров. Добавление поверхностно-активных веществ вызывает сильное снижение поверхностного натяжения в системе, что способствует образованию термодинамически устойчивых (самопроизвольно образующихся) в обычных условиях эмульсий. Такие эмульсии характеризуются очень невысокой дисперсностью.
Однако большинство эмульсий – это микрогетерогенные термодинамически неустойчивые системы, разрушающиеся при хранении, изменении температуры и т. д. Для стабилизации таких эмульсий применяют эмульгаторы. Они не только повышают агрегативную устойчивость дисперсий и эмульсий, но и изменяют их электрические свойства, уменьшают работу образования новых поверхностей, т.е. облегчают диспергирование. В случае сильного снижения межфазного натяжения дисперсная фаза может самопроизвольно диспергироваться с образованием микрочастиц размером 60-100 нм даже под действием теплового движения. Скорость и степень дробления дисперсной фазы определяются площадью поверхности раздела между фазами, свойствами эмульгаторов. Например, иногда неионогенные эмульгаторы при эмульсионной полимеризации обеспечивают более высокую степень диспергирования мономера, чем ионогенные эмульгаторы. В отличие от растворов полимеров, коллоидные системы обладают низкой вязкостью даже при высокой концентрации, легко разрушаются при замораживании или действии электролитов, обладают незначительным осмотическим давлением.
Билет № 8
Третичная структура белка.
Полипептидная спираль укладывается в глобулу так, что гидрофобные аминокислотные радикалы погружаются внутрь глобулы, а гидрофильные располагаются на поверхности и взаимодействуют с водой. Третичная структура образуется за счет водородных, ионных, дисульфидных связей. Третичной структурой определяется биологическая активность белков и их специфичность.
Студни и гели.
Студни (или гели) - двухкомпонентные системы полимер- растворитель, представляющие собой структуры, образованные из сольватированных макромолекул и их агрегатов, в которых распределены молекулы растворителя. Момент, когда растворы начинают терять текучесть и превращаться в студень, называется точкой гелеобразования.
Существуют два типа студней.
· студни первого типа – это системы, в которых пространственная сетка образована химическими связями. При нагревании не плавятся – называются термонеобратимыми. Образуются при самопроизвольном набухании пространственно-сшитых полимеров, при трехмерной полимеризации или поликонденсации в растворе. Студни первого типа – устойчивые гомогенные системы; они не имеют критических температур растворения, их строение не зависит от температуры вплоть до термораспада. При охлаждении студней иногда происходит синерезис – отделение растворителя от студня;
· студни второго типа — системы, в которых пространственная сетка образована связями различной природы. При нагревании – плавятся. называются термообратимыми. Строение и устойчивость студней второго типа зависят от температуры. При изменении температуры происходит разделение фаз, происходит расслаивание на две фазы – набухший полимер и растворитель или очень разбавленный раствор полимера. Таким образом, студни второго типа являются системами с незавершенным расслаиванием.
Билет №9
Классификация полимеров по отношению к нагреванию. Примеры полимеров.
· термопластичные - при нагреве размягчаются, даже плавятся, а при охлаждении затвердевают. Этот процесс обратим (полиэтилен, полипропилен, полистирол);
· термореактивные - при нагреве подвергаются необратимому химическому разрушению без плавления. Молекулы термореактивных полимеров имеют нелинейную структуру, полученную путём сшивки цепных полимерных молекул. Упругие свойства термореактивных полимеров выше, чем у термопластов, однако, термореактивные полимеры практически не обладают текучестью, поэтому имеют более низкое напряжение разрушения (фенолформальдегидные смолы)
Билет №10
Ступенчатая полимеризация.
Если промежуточные продукты присоединения, образующиеся в результате полимеризации, стабльны и могут быть выделены на каждом этапе присоединения новых мономерных звеньев, реакция полимеризации называется ступенчатой.
Ступенчатая полимеризация характеризуется следующими особенностями:
1) образующиеся промежуточные продукты устойчивы и могут быть выделены из сферы реакции;
2) реакционная способность промежуточных соединений и исходного мономера одинакова;
3) каждая стадия роста полимерной цепи протекает с высокой энергией активации;
4) ступенчатая полимеризация - обратимый процесс.
Ступенчатая полимеризация протекает в присутствии гидролитических агентов (воды, кислот, оснований) и поэтому часто называется гидролитической. Вещества, способствующие такому процессу, называются активаторами.
Билет №11
Билет №12
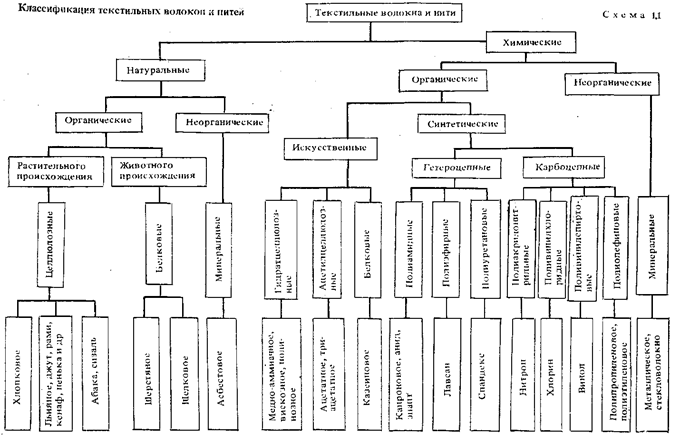
1. Классификация волокон (с примерами).
Олигосахариды.
Олигосахариды – короткие полимеры, состоящие из
моносахаридных единиц, соединённых между собой ковалентной О-гликозидной связью.
Олигосахариды классифицируют:
1) в зависимости от числа моносахаридных фрагментов, входящих в состав
олигосахаридов: дисахариды, трисахариды, тетрасахариды и т.д.
2) по составу моносахаридных остатков:
- гомоолигосахариды - состоят из остатков одного вида моносахарида;
- гетероолигосахариды - состоят из остатков разных моносахаридов.
3) в зависимости от порядка соединения мономеров: линейные и разветвлённые.
Из олигосахаридов в природе наиболее широко распространены дисахариды.
В противоположность олигопептидам и олигонуклеотидам олигосахариды довольно часто представляют собой разветвленные структуры.
У большинства олигосахаридов мономерные остатки связаны О- гликозидной связью.
Гликозидная связь - это сложноэфирная связь, которая всегда образуется между первым ассиметричным атомом углерода одного моносахаридного остатка и атомом
кислорода одной из гидроксильных групп другого моносахаридного остатка.
Билет №13
Билет №14
Резервные полисахариды.
Резервные полисахариды служат энергетическим ресурсом, из которого по мере необходимости в организм поступают моносахариды, являющиеся клеточным "топливом". Молекулы резервных полисахаридов — крахмала и гликогена — представляют собой рыхлые, разветвленные структуры, доступные для ферментативного расщепления в большом количестве участков.
Крахмал образуется в растениях при фотосинтезе и откладывается в виде "резервного" углевода в корнях, клубнях и семенах. Крахмал – это белый порошок, состоящий из мелких зерен, не растворимый в холодной воде. При обработке крахмала теплой водой удается выделить две фракции:
- фракцию, растворимую в теплой воде и состоящую из полисахарида амилозы;
- фракцию, лишь набухающую в теплой воде с образованием клейстера и состоящую из полисахарида амилопектина.
Крахмал представляет собой смесь двух полисахаридов, построенных из α-D- глюкозных звеньев:
- амилозы (10-20%);
- амилопектина (80-90%).
БИЛЕТ №15
Полимеризация в растворе.
Полимеризация в растворе - способ проведения полимеризации, при к-ром исходный мономер находится в жидкой фазе в растворенном состоянии. Реакц. система м. б. гомогенной или гетерогенной в зависимости от р-римости катализатора и образующегося полимера в реакц. среде. Р-ритель должен быть инертен к мономеру и возбудителю полимеризации; чаще всего это алифатич. или арома-тич. углеводороды. Т-ру можно изменять в пределах, в к-рых мономер и р-ритель остаются жидкими. Процессы при высоких т-рах часто проводят при избыточном давлении, чтобы воспрепятствовать кипению реакц. смеси. Концентрацию мономера в р-ре изменяют в широких пределах.
Гомогенная полимеризация в растворе описывается классич. ур-ниями кинетики полимеризации. При гетерог. процессе возможны диффузионные затруднения, связанные с поступлением мономера к активным центрам.
БИЛЕТ №16
Сольватация. Гидрогели.
Сольватация — электростатическое взаимодействие между частицами (ионами, молекулами) растворенного вещества и растворителя. Сольватация состоит в том, что молекула растворенного вещества оказывается окруженной сольватной оболочкой, состоящей из более или менее тесно связанных с ней молекул растворителя. В результате сольватации образуются сольваты — образования постоянного или переменного состава. Время жизни сольватов определяется характером и интенсивностью межмолекулярных взаимодействий; даже в случае сильного взаимодействия время жизни отдельного сольвата мало из-за непрерывного обмена частицами в сольватной оболочке. Выделяют неспецифическую и специфическую сольватацию. Неспецифическая сольватация обусловлена ван-дер-ваальсовыми взаимодействиями, специфическая сольватация проявляется вследствие электростатических взаимодействий, координационных и водородных связей.
Гидрогели - сшитые полимеры на основе гидрофильных макромолекул, способные к равновесному и обратимому набуханию в воде и водных р-рах. Величины степени набухания лежат в интервале от 0,5-1 мл (слабонабухающие полимерные гидрогели) до неск. литров (сильнонабухающие полимерные гидрогели) на 1 г сухого в-ва и определяют области использования этих материалов.
Мукополисахариды.
Мукополисахариды - полимерные углевод-белковые комплексы с преимущественным содержанием углеводной чати.
Мукополисахариды так называются, потому что вещества этого класса имеют слизистую консистенцию. Для муко
