Объясните закономерности в изменении свойств химических элементов и их соединений в зависимости от строения их атомов.
Объясните закономерности в изменении свойств химических элементов и их соединений в зависимости от строения их атомов.
Ответ:
1)Закономерности связанные с металли-кими и неметалл-кими свойствами элементов.
а)При перемещении вдоль периода справа на лево металлические свойства усиливаются. И наоборот слева на права неметаллические свойства увеличиваются.(это связано с тем ,что элементы в правой част периода менее склоны отдавать свои электроны для образование химии-их реакций .
б)При перемещении сверху вниз вдоль групп металлические свойства увеличиваются
(это связано с тем , что ниже расположены элементы ,имеющие уже довольно много заполненных электронных оболочек. Их внешние оболочки находятся дальше от ядра.)
2)размеры атомов :
При перемещении слева на право, вдоль периода уменьшается размера атома. Это связанно с тем, что электроны все сильнее притягиваются к ядру по мере возрастания заряда ядра .
3)закономерности связанные с валентностью элементов :
Элементы одной той же группы имеют одинаковую электронную оболочку ,и следовательно одинаковую валентность в соединения электроны имеют валентность ,совпадающую с номером их группы.
4)закономерности ,связанные с окислительно-востановительными свойствами .
Электроны обычно обнаруживают в нескольких разных валентностей ,которые нельзя точно предсказать .
4)расскажите о водородных соединениях неметаллов ,закономерности в их свойств ,в связи с положением элементов в периодической системе Д.И.Менделеева.
ОТВЕТ:
Водородные соединения неметаллов :в отличии от металлов неметаллические образуют газообразные водородные соединения. Их состав зависимости от степен окисления неметаллов .
Водородные соединения неметаллов можно разделить на 3 группы :
1 )Хорошо растворяются в воде (HCl,HBr,H2S)они проявляют кислотные и основные свойства .
2)Соединения, разлагаемые водой:
BH3+3H20=H3BO3+3H2
3)Летуче водородные соединения.
СН4,РН3,которые не взаимодействуют с водой с увеличением порядкого номера элементы неметаллы усиливается кислотный характер водородного соединения .
SiH4—PH3—H2S—HCl
По тепловому эффекту.
По фазе.
б) Гетерогенные (реакции между несмешивающимися жидкостями)
По использованию катализатора. Катализатор – вещество ускоряющее химическую реакцию.
а) каталитические (в том числе и ферментативные) – без использование катализатора практически не идут.
б) некаталитические.
Скорость хим реакции. Расскажите о зависимости от природы .
1)Скорость химической реакции- это величина, показывающая как изменяются концентрации исходных веществ или продуктов реакции за единицу времени.
А)концентрация
При повышении концентрации хотя бы одного из реагирующих веществ скорость химической реакции возрастает в соответствии с кинетическим уравнением.
Причиной повышения скорости является увеличение числа столкновений реагирующих частиц за счёт увеличения частиц в единице объёма.
Б)площадь соприкосновения реагирующих веществ
Для увеличения площади соприкосновения реагирующих веществ, их измельчают. Наибольшей степени измельчения достигают путем растворения веществ. Быстрее всего вещества реагируют в растворах.
В)природа реагирующих веществ.
Например, металлы магний и железо реагируют с соляной кислотой одинаковой концентрации с различной скоростью. Это связано с разной химической активностью металлов.
Г)Катализатор.
Катализаторы - это вещества, которые повышают скорость химической реакции. Они вступают во взаимодействие с реагентами с образованием промежуточного химического соединения и освобождается в конце реакции.
Влияние, оказываемое катализаторами на химические реакции, называется катализом.По агрегатному состоянию, в котором находятся катализатор и реагирующие вещества, следует различать:
гомогенный катализ (катализатор образует с реагирующими веществами гомогенную систему, например, газовую смесь;
гетерогенный катализ (катализатор и реагирующие вещества находятся в разных фазах; катализ идет на поверхности раздела фаз).
Д)Температура.
Правило Вант - Гоффа является приближенным и применимо лишь для ориентировочной оценки влияния температуры на скорость реакции.
11) Раскройте понятие обратимости химических реакций.Расскажите о химическом равновесии и условиях его смещение.
Ответ:
1)Обратимыми называются реакции, которые могут протекать как в прямом, так и в обратном направлении. Необратимыми называют реакции, протекающие до конца, то есть до тех пор, пока полностью не израсходуется одно из исходных веществ.
Необратимые реакции:
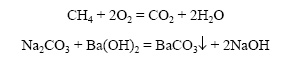
Обратимая реакция:
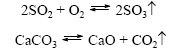
2) Состояние системы, при котором скорость прямой реакции равна скорости обратной реакции, называют химическим равновесием.
А) Влияние концентрации – если увеличить концентрацию исходных веществ, то равновесие смещается в сторону образования продуктов реакции.
Б)Влияние температуры – увеличение температуры смещает равновесие в сторону эндотермической реакции.
В) Влияние давления (только для газообразных веществ) – при увеличении давления, равновесие смещается в сторону образования веществ, занимающих меньший объём.
!12)Раскройте понятие окислительно-восстановительные реакции(на примере алюминия с оксидами некоторых металлов, азотной кислоты с медью).
Ответ:
Б) Химические свойства железа.
Как элемент побочной подгруппы железо может проявлять несколько степеней окисления. Таким образом, можно говорить, что у железа имеется два ряда соединений, в которых оно двух- и трехвалентно.
1) На воздухе железо легко окисляется в присутствии влаги (ржавление):
4Fe + 3O2 + 6H2 O = 4Fe(OH)3
2) Накалённая железная проволока горит в кислороде, образуя окалину - оксид железа (II,III) - вещество чёрного цвета:
3Fe + 2O2 = Fe3O4
3)Железо реагирует с неметаллами при нагревании:
2Fe + 3Br2 t˚C→ 2FeBr3
Fe + S t˚C→ FeS
Защита от коррозии.
1 повышение химического сопротивления конструкционных материалов,
2 изоляция поверхности металла от агрессивной среды,
3 понижение агрессивности производственной среды,
4 снижение коррозии наложением внешнего тока (электрохимическая защита).
16)Расскажите общие способы получения металлов. Раскройте практическое значение электролиза на примере солей.
Способы получения металлов обычно разделяют на три типа:
пирометаллургические(восстановление при высоких температурах);
гидрометаллургические (восстановление из солей в растворах);
электрометаллургические (электролиз раствора или расплава).
Общие способы получения металлов
Сильные основания
NaOH гидроксид натрия (едкий натр)
KOH гидроксид калия (едкое кали)
LiOH гидроксид лития
Ba(OH)2 гидроксид бария
Ca(OH)2 гидроксид кальция (гашеная известь)
Слабые основания
Mg(OH)2 гидроксид магния
Fe(OH)2 гидроксид железа (II)
Zn(OH)2 гидроксид цинка
NH4OH гидроксид аммония
Fe(OH)3 гидроксид железа (III).
Еще одно важное химическое свойство оснований – способность разлагаться при нагревании на воду и основной оксид.
Cu(OH)2 = CuO + H2O (при нагревании)
2 Fe(OH)3 = Fe2O3 + 3 H2O (при нагревании)
Растворы щелочей окрашивают индикаторы: лакмус – в синий цвет, фенолфталеин – в малиновый цвет. Индикатор метиловый оранжевый (или метилоранж) в растворах щелочей имеет желтый цвет.
21)Дайте краткую характеристику классу соли, расскажите о их составе и перечислите названия. Характеризуйте их взаимодействие с металлами и кислотами, щелочами, друг с другом.
ОТВЕТ:
1)Солями называются вещества, в которых атомы металла связаны с кислотными остатками.
Примеры типичных солей приведены ниже.
NaCl – хлорид натрия,
Na2SO4 – сульфат натрия,
СаSO4 – сульфат кальция,
СаCl2 – хлорид кальция,
(NH4)2SO4 – сульфат аммония.
Все соли разделяются на средние, кислые и основные. Средние соли содержат только атомы металла и кислотного остатка
Кислые соли, помимо ионов металла и кислотного остатка, содержат ионы водорода.
NaHCO3 – гидрокарбонат натрия,
Основные соли, помимо ионов металла и кислотного остатка, содержат гидроксильные группы.
Пространственная изомерия
Пространственная изомерия подразделяется на два вида: геометрическую и оптическую.
Геометрическая изомерия характерна для соединений, содержащих двойные связи, и циклических соединений..
Оптическая изомерия возникает, если молекула несовместима со своим изображением в зеркале. Это возможно, когда у атома углерода в молекуле четыре различных заместителя. Этот атом называют асимметрическим. Примером такой молекулы является молекула а-аминопропионовой кислоты.
Физические свойства
При нормальных условиях — бесцветный газ, мало растворимый в воде, легче воздуха. Температура кипения −83,8 °C. При сжатии разлагается со взрывом, хранят в баллонах, заполненных кизельгуром или активированным углем, пропитанным ацетоном, в котором ацетилен растворяется под давлением в больших количествах. Взрывоопасный.
Химические свойства
Ацетилено-кислородное пламя(температура «ядра» 3300 °C)
Для ацетилена (этина) характерны реакции присоединения:
HC≡CH + Cl2 -> СlСН=СНСl
Ацетилен с водой, в присутствии солей ртути и других катализаторов, образует уксусный альдегид (реакция Кучерова). В силу наличия тройной связи, молекулавысокоэнергетична и обладает большой удельной теплотой сгорания — 14000 ккал/м³. При сгорании температура пламени достигает 3300°С. Ацетилен можетполимеризироваться в бензол и другие органические соединения (полиацетилен, винилацетилен). Для полимеризации в бензол необходим графит и температура в 400 °C.
Применение ацетилена:
1) может применяться в качестве горючего при газовой сварке и резке металлов;
2) используется также для синтеза различных органических соединений;
3) в результате присоединения хлора к ацетилену получают растворитель – 1,1,2,2-тетрахлорэтан. Путем дальнейшей переработки тетрахлорэтана получаются другие хлорпроизводные;
4) при отщеплении хлороводорода от 1,1,2,2-тетрахлорэтана образуется трихлорэтен – растворитель высокого качества, который широко применяется при чистке одежды: СНСI = ССI2;
5) в больших количествах ацетилен идет на производство хлорэтена, или винилхлорида, с помощью полимеризации которого получается поливинилхлорид (используется для изоляции проводов, изготовления плащей, искусственной кожи, труб и других продуктов);
6) из ацетилена получаются и другие полимеры, которые необходимы в производстве пластмасс, каучуков и синтетических волокон.
Получение ацетилена:
1)Термическое разложение алканов (электрокрекинг)
2)Гидролиз карбида кальция
3)Дегидрогалогенирование дигалогеналканов:
4)Из ацетиленидов
Получение
1) Каталитическая дегидроциклизация алканов, т.е. отщепление водорода с одновременной циклизацией
2) Каталитическое дегидрирование циклогексана и его производных
3) Циклическая тримеризация ацетилена и его гомологов над активированным углем при 600°C
4) Сплавление солей ароматических кислот со щелочью или натронной известью.
5) Алкилирование собственно бензола галогенопроизводными (реакция Фриделя-Крафтса) или олефинами.
Физические свойства
Бензол и его ближайшие гомологи – бесцветные жидкости со специфическим запахом. Ароматические углеводороды легче воды и в ней не растворяются, однако легко растворяются в органических растворителях – спирте, эфире, ацетоне.
Химические свойства
Бензольное ядро обладает высокой прочностью, чем и объясняется склонность ароматических углеводородов к реакциям замещения. В отличие от алканов, которые также склонны к реакциям замещения, ароматические углеводороды характеризуются большой подвижностью атомов водорода в ядре, поэтому реакции галогенирования, нитрования, сульфирования и др. протекают в значительно более мягких условиях, чем у алканов.
Применение
Ароматические углеводороды являются важным сырьем для производства различных синтетических материалов, красителей, физиологически активных веществ. Так, бензол – продукт для получения красителей, медикаментов, средств защиты растений и др. Толуол используется как сырье в производстве взрывчатых веществ, фармацевтических препаратов, а также в качестве растворителя. Винилбензол (стирол) применяется для получения полимерного материала – полистирола.
29)Расскажите про такое соединение как нефть :состав, свойства, основные способы переработке. Нефть-как источник сырья для органического синтеза.
Нефть- это маслянистая жидкость темного красно-коричневого, иногда почти черного, цвета. В ее состав входит около 1000 веществ! Наибольшую часть из них (80-90%) органические вещества, состоящие из атомов углерода и водорода. Нефть содержит порядка 500 углеводородных соединений
Перегонка нефти
Перегонка нефти. При постепенном нагревании нефти можно последовательно выделять продукты, у которых температура кипения будет всё выше и выше..В конце концов исследования показали, что при нагревании нефти до 450—550 °С под давлением в несколько атмосфер часть тяжёлых углеводородов расщепляется, превращаясь в более лёгкие, как правило непредельного строения. При этом ароматические и насыщенные циклические углеводороды, имеющие длинные боковые цепи, теряют их. В результате продуктом перегонки оказывается широкий спектр углеводородов, из которых основную часть составляет бензиновая фракция
Химический состав нефти.
Нефть — это смесь углеводородов с самыми разнообразными цепочками атомов углерода.
Встречаются и короткие цепи, и длинные, и нормальные, и разветвленные, и замкнутые в кольца, и много кольчатые. Кроме углеводородов, в нефти содержатся в небольшом количестве кислородные и сернистые соединения и совсем немного азотистых.
Получение
этилового спирта (или винный спирт) путём брожения углеводов:
C2H12O6 => C2H5-OH + CO2
Физические свойства
ФенолC6H5OH (карболовая кислота) — бесцветное кристаллическое вещество на воздухе окисляется и становится розовым, при обычной температуре ограниченно растворим в воде, выше 66 °C смешивается с водой в любых соотношениях. Фенол — токсичное вещество, вызывает ожоги кожи, является антисептиком.
Химические свойства
I. Свойства гидроксильной группы
С активными металлами-
2C6H5-OH + 2Na → 2C6H5-ONa + H2
Со щелочами -
C6H5-OH + NaOH (водн. р-р) ↔ C6H5-ONa + H2O
II. Свойства бензольного кольца
1Нитрование.
2Галогенирование
3Конденсация с альдегидами.
Применение фенолов
1. Производство синтетических смол, пластмасс, полиамидов
2. Лекарственных препаратов
3. Красителей
4. Поверхностно-активных веществ
5. Антиоксидантов
6. Антисептиков
7. Взрывчатых веществ
Способ получения
Получение из галогенбензолов. При нагревании хлорбензола и гидроксида натрия под давлением получают фенолят натрия, при дальнейшей обработке которого кислотой образуется фенол:
С6Н5―Сl + 2NaOH → C6H5―ONa + NaCl + Н2О.
32.Охарактеризуйте альдегиды ,их строение и свойства. Расскажите про их получение и про применение муравьиного и уксусного альдегида .
Объясните закономерности в изменении свойств химических элементов и их соединений в зависимости от строения их атомов.
Ответ:
1)Закономерности связанные с металли-кими и неметалл-кими свойствами элементов.
а)При перемещении вдоль периода справа на лево металлические свойства усиливаются. И наоборот слева на права неметаллические свойства увеличиваются.(это связано с тем ,что элементы в правой част периода менее склоны отдавать свои электроны для образование химии-их реакций .
б)При перемещении сверху вниз вдоль групп металлические свойства увеличиваются
(это связано с тем , что ниже расположены элементы ,имеющие уже довольно много заполненных электронных оболочек. Их внешние оболочки находятся дальше от ядра.)
2)размеры атомов :
При перемещении слева на право, вдоль периода уменьшается размера атома. Это связанно с тем, что электроны все сильнее притягиваются к ядру по мере возрастания заряда ядра .
3)закономерности связанные с валентностью элементов :
Элементы одной той же группы имеют одинаковую электронную оболочку ,и следовательно одинаковую валентность в соединения электроны имеют валентность ,совпадающую с номером их группы.
4)закономерности ,связанные с окислительно-востановительными свойствами .
Электроны обычно обнаруживают в нескольких разных валентностей ,которые нельзя точно предсказать .
4)расскажите о водородных соединениях неметаллов ,закономерности в их свойств ,в связи с положением элементов в периодической системе Д.И.Менделеева.
ОТВЕТ:
Водородные соединения неметаллов :в отличии от металлов неметаллические образуют газообразные водородные соединения. Их состав зависимости от степен окисления неметаллов .
Водородные соединения неметаллов можно разделить на 3 группы :
1 )Хорошо растворяются в воде (HCl,HBr,H2S)они проявляют кислотные и основные свойства .
2)Соединения, разлагаемые водой:
BH3+3H20=H3BO3+3H2
3)Летуче водородные соединения.
СН4,РН3,которые не взаимодействуют с водой с увеличением порядкого номера элементы неметаллы усиливается кислотный характер водородного соединения .
SiH4—PH3—H2S—HCl
