Назовите высшие оксиды хим элем третьего периода .Расскажите о закономерностях в изменении их свойств .
ОТВЕТ:
А) Названия (Na2O(оксд натрия),MgO(оксид магния), Al2O3, SiO2, SO3. Cl2O7+)
Б)Изменение свойств кислородных соединений элементов 3-го периода обусловлено строением их атомов ,точнее, изменение числа электронов на внешнем энергетическом уровне.
В связи с уменьшение разницы в электроотрицательности ,изменяется вид связи: от ионной до ковалентной связи.
В)По мере увеличеня степени окисления неметаллов образуемые оксидами высшие кислородсодержащие кислоты проявляют всё более ярко выраженные кислотные свойства .
Кремневая (кислота (Si^+4)-твердая нерастворимая ,довольно слабая кислота.
Серная кислота (S^+6)- маслянистая жидкость раствора в воде .кислота сильная.
!6)Дайте характеристику высших кислородосодержащих кислот хим элем 3 периода ,раскройте их состав и дайте сравнительную характеристику х свойств .
ОТВЕТ:
7)Охарактеризуйте виды хим связей в неорганических и органических соединениях: ионная, металлическая, водородная ковалентная .
ОТВЕТ:
Ионная связь-это связь образует между атомов металлов и не металлов при этом электроны перемещаются из внешнего слоя металлов на внешний слой не металлов.
Ковалентная связь-это связь осуществляется за счёт образование электронных пар в одинаковой мере принадлежащей обоих атомов .
+ + + -
Н+Н НСl
Неполярная Полярная
Металлическая связь- хим связь основанная на обособлений валентных электронов ,принадлежащие всем атомов в кристалле .
Водородная связь- это связь образованная между атомов водорода и атомов другого элемента .
!8)дайте понятие реакция ионного обмена. Расскажите об условиях их необратимости .
Реакция ионного обмена – окислительно-восстановительная реакция, которая идет в направлении связывания ионов, но при которой не происходит изменения степеней окисления.
9) Раскройте классификацию химических реакций в неорганической органической химии.
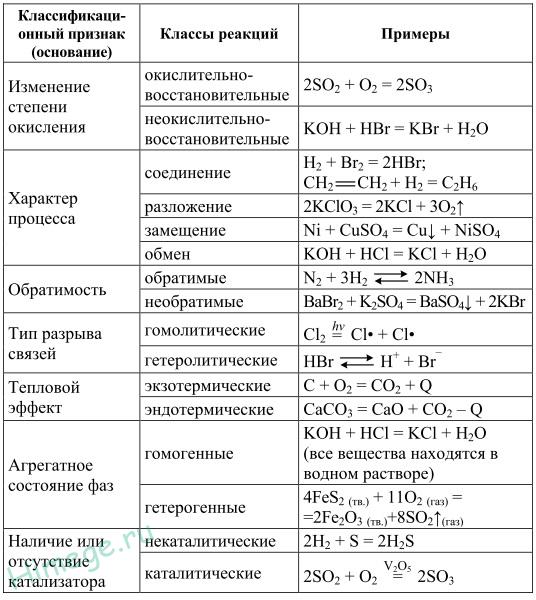
1)Первый признак классификации по изменению степени окисления элементов, образующих реагенты и продукты.<
а) окислительно-восстановительные.
б) без изменения степени окисления.
2) Химические реакции классифицируются по характеру процесса, т.е по числу и составу реагентов и продуктов.
3) По возможности протекать в обратном направлении – обратимые и необратимые.
4) По типу разрыва связей – гомолитические (равный разрыв, каждый атом по 1 электрону получает) и гетеролитический (неравный разрыв – одному достается пара электронов)
По тепловому эффекту.
По фазе.
б) Гетерогенные (реакции между несмешивающимися жидкостями)
По использованию катализатора. Катализатор – вещество ускоряющее химическую реакцию.
а) каталитические (в том числе и ферментативные) – без использование катализатора практически не идут.
б) некаталитические.
Скорость хим реакции. Расскажите о зависимости от природы .
1)Скорость химической реакции- это величина, показывающая как изменяются концентрации исходных веществ или продуктов реакции за единицу времени.
А)концентрация
При повышении концентрации хотя бы одного из реагирующих веществ скорость химической реакции возрастает в соответствии с кинетическим уравнением.
Причиной повышения скорости является увеличение числа столкновений реагирующих частиц за счёт увеличения частиц в единице объёма.
Б)площадь соприкосновения реагирующих веществ
Для увеличения площади соприкосновения реагирующих веществ, их измельчают. Наибольшей степени измельчения достигают путем растворения веществ. Быстрее всего вещества реагируют в растворах.
В)природа реагирующих веществ.
Например, металлы магний и железо реагируют с соляной кислотой одинаковой концентрации с различной скоростью. Это связано с разной химической активностью металлов.
Г)Катализатор.
Катализаторы - это вещества, которые повышают скорость химической реакции. Они вступают во взаимодействие с реагентами с образованием промежуточного химического соединения и освобождается в конце реакции.
Влияние, оказываемое катализаторами на химические реакции, называется катализом.По агрегатному состоянию, в котором находятся катализатор и реагирующие вещества, следует различать:
гомогенный катализ (катализатор образует с реагирующими веществами гомогенную систему, например, газовую смесь;
гетерогенный катализ (катализатор и реагирующие вещества находятся в разных фазах; катализ идет на поверхности раздела фаз).
Д)Температура.
Правило Вант - Гоффа является приближенным и применимо лишь для ориентировочной оценки влияния температуры на скорость реакции.
11) Раскройте понятие обратимости химических реакций.Расскажите о химическом равновесии и условиях его смещение.
Ответ:
1)Обратимыми называются реакции, которые могут протекать как в прямом, так и в обратном направлении. Необратимыми называют реакции, протекающие до конца, то есть до тех пор, пока полностью не израсходуется одно из исходных веществ.
Необратимые реакции:
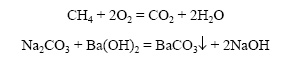
Обратимая реакция:
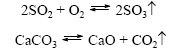
2) Состояние системы, при котором скорость прямой реакции равна скорости обратной реакции, называют химическим равновесием.
А) Влияние концентрации – если увеличить концентрацию исходных веществ, то равновесие смещается в сторону образования продуктов реакции.
Б)Влияние температуры – увеличение температуры смещает равновесие в сторону эндотермической реакции.
В) Влияние давления (только для газообразных веществ) – при увеличении давления, равновесие смещается в сторону образования веществ, занимающих меньший объём.
!12)Раскройте понятие окислительно-восстановительные реакции(на примере алюминия с оксидами некоторых металлов, азотной кислоты с медью).
Ответ:
