Константа гидролиза и степень гидролиза
Кг = 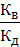 ß =
ß = 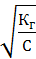 ß =
ß = 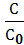
ß – степень гидролиза, (в % или долях ед.)
С – концентрация соли, подвергшейся гидролизу, моль/л;
С0 – концентрация раствора, моль/л
Кг – константа гидролиза;
Кв – константа воды, Кв=10-14
Кд – константа диссоциации слабого электролита, образовавшего данную соль, по последней стадии диссоциации.
Задание:
№ 1. Написать уравнения гидролиза солей А и Б (по ступеням) в молекулярной и ионной формах, указать рН растворов (рН > 7 или рН < 7), тип гидролиза (по катиону, по аниону, по катиону и аниону).
№ 2. Вычислить степень гидролиза и рН раствора соли (Б) заданной концентрации, учитывая первую стадию гидролиза.
Таблица 7.
| № задания | А | Б | С, моль/л |
| K2S | AlBr3 | 0,01 | |
| CrBr3 | Na2CO3 | 0,1 | |
| SnCl2 | K2SiO3 | 0,001 | |
| Be(NO3)2 | KCN | 0,1 | |
| K2SO3 | Al2(SO4)3 | 0,01 | |
| K2SiO3 | FeCl3 | 1,0 | |
| AlCl3 | K2SO3; | 0,1 | |
| CdBr2 | CaF2 | 0,01 | |
| Ba(NO2)2 | CuSO4 | 0,1 | |
| FeI2 | К2CO3; | 0,001 | |
| Fe2(SO4)3 | Na2SO3 | 0,1 | |
| CuCl2 | K2SO3 | 0,01 | |
| K3PO4 | NiCl2 | 0,01 | |
| FeCl3 | Ba(CH3COO)2 | 0,1 | |
| Na2S | ZnSO4 | 0,01 | |
| K2S | Al2(SO4)3 | 0,1 | |
| K2CO3 | (NH4)2SO4 | 0,001 | |
| CdBr2 | K2CO3 | 0,1 | |
| Be(NO3)2 | K3PO4 | 0,01 | |
| Na2SO3 | CrBr3 | 0,01 | |
| BeCl2 | Na2SO3 | 0,1 | |
| K2S | FeSO4 | 0,01 | |
| Na2S | CrBr3 | 1,0 | |
| Cr(NO3)3 | K2SO3 | 0,001 | |
| Be(NO3)2 | Ba(CH3COO)2 | 0,1 | |
| NaCN | Mn(NO3)2 | 0,01 | |
| CoCl2 | K2CO3 | 0,01 | |
| Cr2(SO4)3 | K2S | 0,1 | |
| Fe(NO3)3 | Na2SiO3 | 0,001 | |
| Cr(NO3)3 | K3PO4 | 1,0 |
№ 6. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ПРОЦЕССЫ
Окислительно-восстановительные реакции
Правила использования среды
Таблица 8.
| Процессы | Среда в окислительно-восстановительных реакциях в расчете на «О2-» в соединении | ||
| кислая (Н+) | щелочная (ОН-) | нейтральная (Н2О) | |
Связать «О2–-» 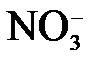 → → 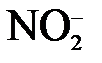 | О2– + 2Н+ = Н2О | О2– + Н2О = 2 ОН– | О2- + Н2О = 2 ОН– |
Ввести «О2–» 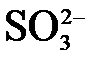 → → 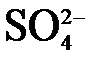 | Н2О = О2– + 2Н+ | 2 ОН– = О2– + Н2О | Н2О = О2– + 2Н+ |
Изменение степени окисления окислителей в зависимости от среды
Перманганатометрия
1. Кислая среда (рН <7):
МnО4- + 8Н+ + 5 е- → Мn2+ + 4Н2О
2. Среда щелочная (рН > 7):
МnО4- + е- → МnО42-
3. Среда нейтральная (рН = 7):
МnО42- + 2Н2О + 2е- → МnО2 + 4ОН-.
Хроматометрия
Cr2O72- + 14H+ +6e- → 2Cr3+ + 7H2O
Йодометрия
I2 + 2S2O32-→ 2I- + S4O62-
Задание:
Расставить коэффициенты электронно-ионным методом в окислительно-восстановительной реакции:
Таблица 9.
| № задания | Окислительно-восстановительные реакции |
| FeSO4 + KClO3 + H2SO4 → Fe2(SO4)3 + KCl + H2O | |
| MnSO4 + NaBiO3 + HNO3 → Bi(NO3)3 + HMnO4 + Na2SO4 + NaNO3 + H2O | |
| KCrO2 + PbO2 + KOH → K2CrO4 + K2PbO2 + H2O | |
| Cr2(SO4)3 + Br2 + NaOH → Na2CrO4 + NaBr + Na2SO4 + H2O | |
| H2O2 + KMnO4 + KOH → K2MnO4 + O2 + H2O | |
| K2Cr2O7 + Na2SO3 + H2SO4 → Cr2(SO4)3 + Na2SO4 +K2SO4 + H2O | |
| MnSO4 + Br2 + KOH → KMnO4 + KBr + K2SO4 + H2O | |
| KMnO4 + KJ + H2SO4 → MnSO4 + J2 + K2SO4 + H2O | |
| KMnO4 + KJ + KOH → K2MnO4 + KJO4 + H2O | |
| Bi(NO3)3 + NaClO4 + NaOH → NaBiO3 + NaCl + NaNO3 + H2O | |
| NaBiO3 + KCr(SO4)2 + H2SO4 → Bi2(SO4)3 + K2Cr2O7 + Na2SO4 + +H2O | |
| K2Cr2O7 + HJ + HClO4 → KClO4 + Cr(ClO4)3 + J2 + H2O | |
| KMnO4 + MnSO4 + H2O → MnO2 + K2SO4 + H2SO4 | |
| Na[Cr(OH)4] + Cl2 + NaOH → Na2CrO4 + NaCl + H2O | |
| (NH4)2S2O8 + Mn(NO3)2 + H2O → (NH4)2SO4 + HMnO4 + H2SO4 + +HNO3 | |
| KMnO4 + FeCO3 + H2SO4 → Fe2(SO4)3 + CO2 + MnSO4 + K2SO4 + H2O | |
| K2Cr2O7 + K2S + H2SO4 → Cr2(SO4)3 + S + K2SO4 + H2O | |
| KNO3 + KJ + H2SO4 → NO + J2 +K2SO4 + H2O | |
| H2O2 + KJO3 → J2 + KOH + O2 + H2O | |
| AgNO3 + AsH3 + H2O → Ag + H3AsO4 + HNO3 | |
| Na2CrO4+NaJ+H2SO4→Cr2(SO4)3+J2+Na2SO4+H2O | |
| K2Cr2O7+H2S+H2SO4→Cr2(SO4)3+S+K2SO4+H2O | |
| KMnO4+FeCO3+H2SO4→MnSO4+Fe2(SO4)3+CO2+K2SO4+H2O | |
| KMnO4+KNO2+H2O→KNO3+MnO2+KOH | |
| NaCrO2+Br2+NaOH→Na2CrO4+NaBr+H2O | |
| MnSO4+PbO2+HNO3→HMnO4+PbSO4+Pb(NO3)2+H2O | |
| K2MnO4+KJ+H2SO4→MnSO4+J2+K2SO4+H2O | |
| KMnO4+CO+H2SO4→MnSO4+CO2+K2SO4+H2O | |
| FeSO4+HJO3+H2SO4→Fe2(SO4)3+J2+H2O | |
| FeSO4+HNO3+H2SO4→Fe2(SO4)3+NO+H2O |
Гальванический элемент
Электродные потенциалы металлов рассчитываются по уравнению Нернста:
φ Mеn+/Me = φ0Mеn+/Me + 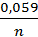 · lg CMen+
· lg CMen+
где φ0Mеn+/Me – величина стандартного электродного потенциала, (В).
Электродвижущая сила процесса:
ЭДС =φ катода – φанода
Задание:
1. Рассчитайте электродные потенциалы металлов по уравнению Нернста.
2. Определите анод и катод. Рассчитайте ЭДС гальванического элемента.
3. Напишите электродные процессы и общую токообразующую реакцию.
4. Напишите схему гальванического элемента и укажите направление движения электронов по внешней цепи.
Стандартные электродные потенциалы (приложение 6).
Таблица 10.
| № задания | Электроды | Концентрация электролита моль/л |
| Cu/CuCl2; Zn/ ZnCl2 | CCu2+= 0,2; CZn2+=10-4 | |
| Cu/CuSO4; Co/CoSO4 | CCu2+= 0,1; CCo2+=10-3 | |
| Fe/FeCl2; Mg/MgCl2 | CFe2+ = 0,2; CMg2+= 0,001 | |
| Cu/CuCl2 ; Cd /CdCl2 | CCu2+= 0,1; CCd2+= 0,002 | |
| Ag/AgNO3; Zn/Zn(NO3)2 | CAg+= 0,2; CZn2+= 0,001 | |
| Pb/Pb(NO3)2; Mg/Mg(NO3)2 | CPb2+= 0,1; CMg2+= 10-4 | |
| Al/Al2(SO4)3; Sn/ SnSO4. | CAl3+ = 0,01; CSn2+= 0,5 | |
| Ag/AgNO3; Co/Co(NO3)2 | CAg+= 0,5; CCo2+= 0,001 | |
| Al/Al2(SO4)3; Au/Au2(SO4)3 | CAl3+= 10-4; CAu3+= 0,25 | |
| Pt/PtCl2; Ni/Ni(NO3)2 | CPt2+= 0,45; CNi2+= 0,01 | |
| Sn/SnCl2; Pb /Pb(NO3)2 | CSn2+= 10-5; CPb2+= 0,5 | |
| Mn/MnSO4; Zn/ZnSO4 | CMn2+= 0,2; CZn2+= 0,001 | |
| Ag/AgNO3; Co/Co(NO3)2 | CAg+= 0,5; CCo2+= 0,001 | |
| Al/Al2(SO4)3; Pt/ PtSO4 | CAl3+= 10-4; CPt3+ = 0,25 | |
| Pt/PtCl2; Cr/CrSO4 | CPt2+= 0,5; CCr2+ = 0,02 | |
| Sn/SnCl2; Pb /Pb(NO3)2 | CSn2+= 10-5; CPb2+= 0,5 | |
| Ni/NiSO4; Cu /CuSO4 | CNi2+= 0,001; CCu2+= 0,5 | |
| Ag/AgNO3; Cd/Cd(NO3)2 | CAg+= 0,1; CCd2+= 0,002 | |
| Sn/Sn(NO3)2; Fe/Fe(NO3)3 | CSn2+= 0,005; CFe3+= 0,1 | |
| Pb/Pb(NO3)2; Fe/Fe(NO3)2 | CPb2+= 0,05; CFe2+= 0,2 | |
| Ni/NiSO4; Cu/CuSO4 | CNi2+= 0,001; CCu2+= 0,5 | |
| Ag/AgNO3; Cd/Cd(NO3)2 | CAg+= 0,1; CCd2+= 0,002 | |
| Sn/Sn(NO3)2; Zn/Zn(NO3)2 | CSn2+= 0,05; CZn2+= 0,1 | |
| Pb/Pb(NO3)4 ; Fe/Fe(NO3)2 | CPb4+= 0,002; CFe2+= 0,2 | |
| Ag/AgNO3; Mn/MnSO4 | CAg+= 0, 1; CMn2+ = 0,01 | |
| Cr/CrSO4; Cd/CdSO4 | CCr2+ = 0,01; CCd2+=0,001 | |
| Ag/AgNO3; Mg /Mg(NO3)2 | CAg+= 0,1; CMg2+= 0,2 | |
| Zn/ZnSO4 ; Fe/Fe(NO3)2 | CZn2+= 0,2; CFe2+= 0,02 | |
| Ag/AgNO3 ; Ni/Ni(NO3)2 | CAg+= 0,001; CNi2+= 0,15 | |
| Sn/SnCl2 ; Co/CoCl2 | CSn2+= 0,1; CCo2+= 0,025 |
