Способы получения предельных углеводородов
1. Промышленные методы выделения из природных и попутных газов.
выс. Р фракц. перегонка

 газ сжиженный газ индивид. углев.
газ сжиженный газ индивид. углев.
низкая Т под давлением
| Т кипения | |
| СН4 | - 161оС |
| С2Н6 | - 88оС |
| С3Н8 | - 42оС |
| С4Н10 | - 0,5оС |
2. Из нефти.
Нефть содержит жидкие и твердые предельные углеводороды. Так в ней содержатся: С5Н12, С6Н14 - вcе изомеры.
С7Н16, С8Н18 - в основном нормальные.
Начиная с С9Н20 – только углеводороды нормального строения. Фракционная перегонка не позволяет выделить индивидуальные углеводороды, отгоняют лишь фракции:
| Петролейный эфир | 40-75оС | Растворитель |
| Бензин | 70-130оС | горючее для двигателей внутреннего сгорания |
| Керосин | 150-300оС | топливо для ракетных двигателей |
| Мазут | >300оС | из мазута перегонкой с паром и под вакуумом выделяют различные масла: соляровое, смазочное, вазелиновое и др. |
Благодаря высокой температуре перегонки и особенно в процессе крекинга идет разложение с образованием низкомолекулярных газообразных углеводородов, которые используются в качестве сырья после разделения на фракции, содержащие: этан – этилен, пропан – пропилен, бутан – бутилен.
Путем дополнительного фракционирования выделяют более узкие фракции: С5Н12 используют в синтезе амиловых спиртов, а на их основе эфиров – растворителей и душистых продуктов.
Из масляных фракций нефти выделяют твердые углеводороды состава: С16Н34 и более (парафин и церезин).
3. Гидрирование непредельных углеводородов, полученных в результате крекинга нефти:
Ni, Pt, Pd, T=30-600C
CH3-CH=CH2 + H2  CH3-CH2-CH3
CH3-CH2-CH3
4. Гидрогенизация окиси углерода (способ Орлова-Фишера):
Fe+Co, T=2000C
nCO + (2n+1)H2  CnH2n+2 + nH2O
CnH2n+2 + nH2O
5. Гидрогенизация бурых углей (Бергиус):
Fe, T=4500C, P=200 ат
nC + (n+1)H2  CnH2n+2
CnH2n+2
6. Получение метана из углерода и его окислов:
1200оС
С + 2Н2  СН4
СН4
сажа
Ni, 500оС
С + 2Н2  СН4
СН4
сажа
Ni, 250оС
СO + 3Н2  СН4 + Н2О
СН4 + Н2О
7. Получение метана из карбидов металлов:
Al4C3 + 12 Н2О  4Al(OH)3 + 3CH4
4Al(OH)3 + 3CH4
Лабораторные способы получения алканов
1.Реакция Вюрца:
СН3Вr + 2 Nа + ВrСН3 → 2 NаВr + СН3-СН3
 2.Сплавление Nа- или К-солей карбоновых кислот со щелочами:
2.Сплавление Nа- или К-солей карбоновых кислот со щелочами:
 О
О
 cплавление
cплавление
 СН3-С + NaOH
СН3-С + NaOH  Na2CО3 +СН4
Na2CО3 +СН4
ONa
сухой (натронная
известь)
Лучше удается для получения метана.
3.Электролиз водных растворов Nа- или К– солей карбоновых кислот (анодный синтез Кольбе):
СН3СООNa  Na+ + СН3СОО-
Na+ + СН3СОО-
НОН  Н+ + ОН-
Н+ + ОН-
На катоде: 2Н+ + 2е  Н2
Н2 
Na+ + ОН-  NaOH
NaOH
На аноде: 2 СН3СОО--2е  2 СН3СОО.
2 СН3СОО.  2СО2 + 2СН3 .
2СО2 + 2СН3 .  СН3 - СН3
СН3 - СН3

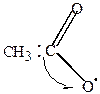
4.Восстановление различных галогенопроизводных углеводородов
Например:
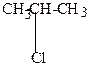 | + 2H  HCl + СН3-СН2-СН3 HCl + СН3-СН2-СН3 |
СН3–СН2J + HJ  СН3-СН3 + I2
СН3-СН3 + I2
Напоминаю, что в молекуле метана все четыре связи С-Н равноценны; это позволяет предположить, что в процессе образования связей происходит перераспределение электронной плотности, а именно, валентные электроны углерода распределяются не на чистых s и р орбиталях, а на смешанных (гибридизованных) орбиталях общей смешанной формы. При гибридизации 1s и 3-х р-электронов образуются четыре гибридных электронных связей.
