Основы теории полимолекулярной адсорбции
Уравнение Ленгмюра даёт хорошие результаты при условии, что адсорбция вещества сопровождается образованием мономолекулярного слоя. Это происходит при хемосорбции и при физической адсорбции газов при небольших давлениях и температуре выше критической (отсутствует конденсация на поверхности адсорбента).
Опыт показал, что, если адсорбция протекает с образованием полимолекулярного адсорбционного слоя, то изотерма отличается от ленгмюровской и имеет более сложный вид. Такие изотермы называют S-изотермы, так как адсорбция не останавливается на образовании монослоя.Возможность образования полимолекулярных адсорбционных слоёв рассматривается в теории Поляни. Эта теория допускает существование на поверхности твёрдых адсорбентах адсорбционных сил, действующих на расстоянии, значительно превышающих диаметр молекул адсорбата.
Основные положения теории Поляни следующие:
1. Адсорбция создаётся чисто физическими силами.
2. На поверхности адсорбента нет активных центров, а адсорбционные силы действуют вблизи от поверхности адсорбента, образуя непрерывное силовое поле.
3. Силовое поле, обусловливающее адсорбцию, действует на расстояния, которые больше, чем размеры отдельных молекул адсорбата. Иначе говоря, у поверхности адсорбента существует так называемый адсорбционный объём, который заполняется при адсорбции молекулами адсорбата.
4. Притяжение молекул адсорбата поверхностью адсорбента не зависит от наличия в адсорбционном объёме других молекул. Поэтому идёт полимолекулярная адсорбция.
5. Адсорбционные силы не зависят от температуры, поэтому с изменением температуры адсорбционный объём не изменяется.
Теория Поляни не дала математического выражения изотермы адсорбции. Однако представления Поляни легли в основу современной теории адсорбции, которую создали С.Брунауэр, П. Эммет и Е. Теллер. Поэтому сокращённо эту теорию называют теорией БЭТ.
Теория постулирует, что при температуре ниже критической каждая молекула, адсорбированная в первом слое является центром для молекул, образующих второй слой, и т.д.
Основные положения теории БЭТ:
1. На поверхности адсорбента имеется определенное число равноценных в энергетическом отношёнии активных центров, способных удерживать молекулы адсорбтива.
2. Для упрощения взаимодействием соседних адсорбированных молекул в первом и последующих слоях пренебрегают.
3. Каждая молекула первого слоя представляет собой возможный центр для адсорбции и образования второго адсорбционного слоя; каждая молекула второго слоя является возможным центром адсорбции в третьем и т. д.
4. Предполагается, что все молекулы во втором и более далеких слоях имеют такую же сумму статистических состояний, как в жидком состоянии (в общем отличающуюся от суммы состояний слоя).
Авторы этой теории вывели уравнение 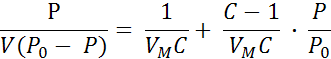
ГдеР0– упругость насыщенного пара,V- объём адсорбированного газа при данном давлении газаР;VM– объём адсорбированного газа в монослое и с = 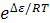 (∆ε – разность между теплотой адсорбции газа в первом слое и теплотой сжижения газа).
(∆ε – разность между теплотой адсорбции газа в первом слое и теплотой сжижения газа).
Уравнение БЭТ получило широкое применение. Из величиныVMможет быть вычислена полная адсорбирующая поверхность адсорбентаS, что имеет важное практическое значение, а из величиныСвычисляется теплота адсорбции газа в монослое. В качестве примера значений площадиSукажем, что адсорбирующая поверхность 1 г испытанного образца силикагеля составила 500м2, а 1 г коллагена – 350м2.Хорошие адсорбенты обладают весьма значительной удельной поверхностью, например, активированный уголь – до 1000м2/г.
Уравнение БЭТ применялось также для определения удельной поверхности различных аморфных и кристаллических полимеров.
