Адсорбция на границе твердое тело – жидкость
Существенным отличием адсорбции веществ из растворов является конкуренция между растворенным веществом и растворителем за возможность взаимодействовать с адсорбционными центрами на поверхности твердого адсорбента. Рассматривая этот вид адсорбции, остановимся на следующем:
1.При адсорбции из раствора важным фактором является величина удельной поверхности адсорбента и его сродство к поглощаемому веществу. Гидрофильные адсорбенты (силикагель, глины, пористые стекла) хорошо поглощают полярные вещества, а гидрофобные (сажа, активированный уголь) -–неполярные вещества.
2.Природа растворителя: чем хуже данный растворитель смачивает поверхность адсорбента и чем хуже растворяет вещество, тем лучше будет происходить адсорбция растворенного вещества.
3.Природа поглощаемого вещества:
а) выполняется правило «подобное взаимодействует с подобным», т.е. должно быть сродство между адсорбентом и адсорбтивом;
б) Выполняется правило Шилова:
Чем больше растворимость вещества в данном растворителе, тем хуже оно адсорбируется на поверхности твердого адсорбента.
в) правило Ребиндера (правило уравнивания полярностей Ребиндера):
На поверхности раздела фаз прежде всего адсорбируются те вещества, при адсорбции которых происходит выравнивание полярностей соприкасающихся фаз, причём с увеличением разности полярности фаз способность к адсорбции этих веществ возрастает
Эффективней всего адсорбируются молекулы веществ, имеющих дифильноестроение. В этом случае идёт эффективная адсорбция на твердом адсорбенте с самопроизвольной четкой ориентацией их молекул на границе раздела, выравнивающей полярности фаз. Полярный фрагмент молекулы обращен всегда к полярной фазе – к воде, силикагелю, а неполярный фрагмент – к неполярной (гидрофобной) фазе – активированному углю, маслу.
4.Влияние концентрации растворенного вещества на процесс адсорбции при постояннойТописывается уравнением Ленгмюра.
5.Повышение температуры снижает эффективность адсорбции. Это объясняется ослаблением взаимодействия между адсорбентом и адсорбатом.
Молекулярная адсорбция из растворов на твердом адсорбенте широко используется в медицинской практике. Активированный уголь хорошо адсорбирует газы, алкалоиды, барбитураты, токсины из пищеварительной системы. Одна таблетка активированного угля массой 0,25 г имеет адсорбционную поверхность около 100 м2.
Адсорбция растворённого в жидкости вещества на твёрдом адсорбенте
Различают молекулярную и ионную адсорбцию.
Молекулярная адсорбция– это адсорбция из растворов неэлектролитов (или очень слабых электролитов). При молекулярной адсорбции вещество адсорбируется на поверхности твёрдого тела в виде молекул.
Особенности молекулярной адсорбции: наряду с растворённым веществом адсорбируются молекулы растворителя. Поэтому для адсорбции растворённого вещества его молекулы должны вытеснять с поверхности молекулы растворителя.
Экспериментально величину адсорбции «а» изучают измеряя молярную концентрацию раствора до контакта с адсорбентом (с0) и после наступления адсорбционного равновесия (сs)
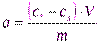 моль/г,
моль/г,
а– количество адсорбированного вещества, приходящееся на 1 г адсорбента;m– масса адсорбента, г:V– объём раствора, из которого идёт адсорбция, л.
На молекулярную адсорбцию влияют:
1. равновесная концентрация растворённого вещества;
2. природа растворителя;
3. природа адсорбента;
4. природа растворённого вещества;
5. температура, время адсорбции.
Адгезия. Виды адгезии
В гетерогенных системах различают межмолекулярные взаимодействия внутри фаз имежду фазами.
Притяжение друг к другу (сцепление) частиц вещества - атомов, молекул, ионов - внутри одной фазы называется когезией (от лат. cohaesus – связанный, сцепленный). Когезияобусловлена межмолекулярными силами различной природы, а во многих случаях, кроме того, водородными и химическими связями. Она является причиной существования веществ в конденсированном – твёрдом или жидком - состоянии. В газах когезия незначительна; наиболее она выражена в твёрдых телах. Когезия характеризует прочность гомогенного тела по отношению к разрыву и другим деформациям. Преодоление сил когезии при разъединении тела на части требует совершения работы, называемой работой когезииWc. При этом подразумевается, что исследуемое тело не имеет дефектов структуры, например, трещин.
В случае легкоподвижных жидкостей обратимая работа когезии равна удвоенному значению поверхностного натяжения жидкости на границе с воздухом:
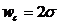 .
.
Это обстоятельство лежит в основе различных методов определения поверхностного натяжения жидкостей, например, метода отрыва кольца, метода отрыва капли (сталагмометрического), метода продавливания сквозь жидкость пузырьков воздуха.
Сцепление приведённых в контакт разнородных твёрдых или жидких тел (фаз) называется адгезией(от лат. adhaesium - прилипание). Подобно когезии, адгезия может быть обусловлена как межмолекулярным взаимодействием, так и химическими связями, в том числе ионной и металлической. Адгезия обусловливает возникновение между двумя телами соединения определённой прочности (прилипание).
В этом смысле когезию можно рассматривать как частный случай адгезии при соприкосновении двух однородных тел. Величиной, характеризующей удельное усилие разрушения адгезионного контакта является адгезионная прочность, используемая в технике для оценки свойств клеев, лакокрасочных покрытий и др.
В фармации адгезионной прочностью могут быть охарактеризованы, например, способность пластыря, мази или горчичника удерживаться на коже, прочность таблеток, спрессованных из различных порошков, прочность связи оболочек с таблетками и т. п. Количественно адгезионная прочность может быть охарактеризована работой адгезионного отрыва Wa.
При длительном контакте разнородных тел (фаз) может происходить взаимная диффузия веществ, что приводит к размытию адгезионного шва и к увеличению адгезионной прочности.
Смачивание. Растекание
В случае одновременного контакта между твёрдой, жидкой и газовой фазами адгезия неразрывно связана со смачиванием. В качестве газовой фазы чаще всего выступает воздух.
При нанесении небольшой капли жидкости на поверхность твёрдого тела (или другой, более плотной жидкости) можно в зависимости от природы контактирующих фаз наблюдать различные явления. В одних случаях капля растекается по поверхности с образованием очень тонкого, практически плоского слоя (растекание). Растекание обычно наблюдается при соприкосновении веществ с близкой полярностью, например, вода растекается по поверхности стекла или кварца (полярные жидкость и твёрдое тело), бензол – по поверхности воска или парафина (неполярные жидкость и твёрдое тело). Но многие неполярные жидкости, такие, как нефть, минеральные масла, бензин и т. п. могут растекаться по практически любым твёрдым (металлы, дерево, стекло, пластмассы и др.) или жидким (вода) поверхностям независимо от их полярности. Такое растекание объясняется слабым межмолекулярным взаимодействием и, как следствие, низким поверхностным натяжением жидкости.
При отсутствии сродства между жидкостью и твёрдой поверхностью наблюдается полное или практически полное несмачивание, когда маленькие капли жидкости принимают почти сферическую форму. Примером полного несмачивания может служить поведение капель ртути на поверхности большинства твёрдых тел (исключая хорошо амальгамирующиеся металлы).
Кроме полного смачивания или несмачивания возможны многочисленные случаи неполного смачивания, когда капля нанесённой жидкости при установившемся равновесии принимает на поверхности твёрдого тела определённую форму (рис. 2.1).
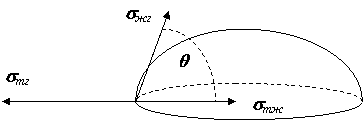
Рис. 1. Взаимодействие сил, определяющих форму капли
На твёрдой поверхности
В такой системе имеются три различных поверхности раздела фаз: между твёрдым телом и жидкостью (т - ж), твёрдым телом и газом (т - г) и между жидкостью и газом (ж - г) с поверхностными натяжениями σтж, σтг и σжгсоответственно.
Линия, в которой пересекаются все три поверхности раздела, называется контуром смачивания. Угол между плоскостью смачиваемой поверхности и плоскостью, касательной к поверхности жидкости в одной из точек контура смачивания, называется краевым углом смачивания q.
Краевой угол всегда измеряется со стороны жидкости. На каждую точку контура смачивания действуют три силы: σтг , стремящаяся растянуть каплю по поверхности (т. е. уменьшить площадь поверхности «т - г»), σтж и σжг, стремящиеся сжать каплю (т. е. уменьшить площадь поверхностей «т - ж» и «ж – г»). Равновесное значение q связано со значением поверхностного натяжения на всех трёх межфазных поверхностях уравнением Т. Юнга:
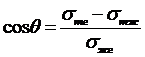
вытекающим из общего условия равновесия трёх сил:
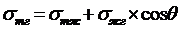 .
.
Из уравнения Юнга видно, что сosq является количественной мерой смачивания. А именно: условие сosq = 1 (q = 0о) отвечает полному смачиванию или растеканию, условие 1 >сosq> 0 (0 о <q< 90о, т. е. краевой угол острый) - неполному смачиванию. При плохом смачивании или полном несмачивании поверхности данной жидкостью краевой угол является тупым (q> 90о; cosq< 0).
Косинус краевого угла смачивания, кроме того, является и мерой работы адгезионного отрыва wa:
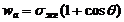 .
.
Соотношение wa и работы когезии для жидкости wк определяет величину краевого угла, а именно: при wa<wкq> 0 о причём с увеличением отношения wa / wк смачивание поверхности улучшается.
Поверхности, хорошо смачивающиеся данной жидкостью, являются по отношению к ней лиофильными (в случае воды – гидрофильными), плохо смачивающиеся – лиофобными (соответственно гидрофобными). Так как гидрофобные вещества обычно хорошо смачиваются маслами, их можно назвать также олеофильными. Гидрофильны, например, желатин, крахмал, глины, стекло; олеофильны - парафин, сажа. Кожа человека почти в одинаковой степени смачивается и водой, и маслами, что существенно при высвобождении и всасывании лекарственных веществ из линиментов, мазей, пластырей, примочек и т. п.
В процессе смачивания жидкостью твёрдой или жидкой поверхности выделяется теплота, называемая теплотой смачивания DHсм. (Правильнее эту величину следовало бы называть теплотой адгезии, так как она обусловлена только взаимодействием конденсированных фаз). В большинстве случаев теплота смачивания имеет значения от 0,4 до 40 кДж/м2. Чем больше теплота смачивания твёрдого тела данной жидкостью, тем лучше смачивание. Таким образом, теплота смачивания, как и краевой угол, может служить количественной характеристикой лиофильности твёрдых поверхностей. Для сравнения гидрофильности различных поверхностей часто используется так называемый коэффициент гидрофильности Kгидр, представляющий собой отношение теплот смачивания данной поверхности водой и бензолом:
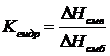
Для гидрофильных веществ Кгидр> 1 для гидрофобных - Кгидр< 1.
Смачивание играет существенную роль во многих технологических и биологических процессах. Так, хорошее смачивание необходимо при нанесении на кожу мазей и линиментов, при стирке и крашении тканей, обработке фотографических материалов, нанесении лакокрасочных покрытий. Смачивание порошков из лекарственных веществ водой (или растворами ПАВ) является одной из важнейших характеристик в технологии лекарств. Избирательное смачивание различных минералов водой или маслами лежит в основе флотации – одного из главных способов обогащения полезных ископаемых, т. е. отделения их от вмещающей горной породы.
