Вывод рабочей формулы
Рассмотрим метод Клемана – Дезорма. Напустим воздух в стеклянный сосуд 1 (см. рисунок) т.е. откроем и закроем кран 10. При быстром сжатии температура воздуха повышается. Поэтому после прекращения напуска разность уровней жидкости в манометре будет постепенно уменьшаться, пока температура воздуха внутри сосуда не сравняется с температурой окружающего воздуха. Назовем состояние воздуха в сосуде после выравнивания температур состоянием 1. Параметры состояния 1: V1 - объем единицы массы воздуха; t1 - температура воздуха; р1 - давление в сосуде.
Откроем кран 3и, как только давление в сосуде сравняется с атмосферным, закроем его. Так как расширение происходит очень быстро, то процесс близок к адиабатическому и, следовательно, температура понизится до t2. Объем единицы массы воздуха станет равным V2. Воздух, оставшийся в сосуде, перейдет в состояние 2 с параметрами V2, t2, р2 (р2 –атмосферное давление). Так как температура t2 меньше наружной, то воздух в сосуде будет постепенно нагреваться (вследствие теплообмена с окружающей средой) до температуры окружающего воздуха t1. Это нагревание происходит изохорически, так как кран закрыт. Давление воздуха в сосуде увеличивается по сравнению с атмосферным, и в манометре возникает разность уровней h2, т.е. воздух переходит в состояние 3 с параметрами V2, t1, р3.
Таким образом, мы имеем три состояния газа со следующими параметрами:
| Состояние Параметр | |||
| Объем | V1 | V2 | V2 |
| Температура | t1 | t2 | t1 |
| Давление | p1 | p2 | p3 |
В состояниях 1 и 3 воздух имеет одинаковую температуру, следовательно, параметры этих состояний можно связать уравнением изотермического процесса (уравнением Бойля – Мариотта):
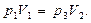 или
или 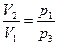 (4)
(4)
Переход от состояния 1 к состоянию 2 происходит адиабатически, поэтому параметры их связаны уравнением Пуассона (3):
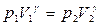 или
или 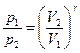 (5)
(5)
Из уравнений (4) и (5) получим
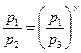 (6)
(6)
Прологарифмировав равенство (6), получим
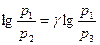 , (7)
, (7)
Если давление измерять жидкостным манометром, то вместо р можно писать соответствующую высоту жидкости. Тогда можно ввести обозначения
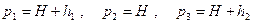
где H – атмосферное давление, h1 – разность уровней манометра в первом состоянии, h2 – разность уровней в третьем состоянии.
Тогда выражение (7) можно переписать в виде
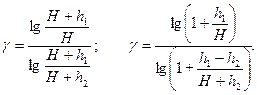
Так как величины h1 и h2, выраженные в миллиметрах ртутного столба, очень малы по сравнению с Н и, следовательно, дроби h1/H и (h1 - h2)/(H + h2) также незначительны, для нахождения величины логарифма можно воспользоваться приближенным выражением
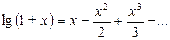 ,
,
где х - малая величина.
Поскольку х2 и, тем более, х3 - величины высших порядков малости, ими можно пренебречь, тогда lg(1+ x) @ x и, следовательно,
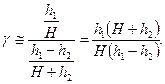
Пренебрегая величиной h2 в сумме H + h2, получим расчетную формулу
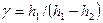 . (8)
. (8)
