Задания для практической части занятия. Практическое занятие № 6
Практическое занятие № 6
Молекулярно-кинетическая теория идеального газа. Статистические распределения
Цель: Обобщение и закрепление теоретического материала по теме «Основы молекулярной физики. Статистические распределения» и рассмотрение решения задач по данной теме.
Требования к исходному уровню знаний и умений
Знать определения следующих физических понятий:
Ø Молекулярная физика;
Ø Статистический метод;
Ø Термодинамика;
Ø Термодинамический метод;
Ø Термодинамическая система;
Ø Равновесная система;
Ø Термодинамические параметры (параметры состояния);
Ø Термодинамический процесс;
Ø Идеальный газ;
Знать определения следующих физических величин, уметь записать формулы, которыми они определяются, указать единицы измерения и значения.
Ø Средняя квадратичная скорость молекул;
Ø Наиболее вероятная скорость молекул;
Ø Средняя арифметическая скорость молекул;
Знать формулировку, уметь записать формулы, определяющие следующие физические законы:
Ø Закон изменения давления с высотой (барометрическая формула);
Ø Распределение Больцмана;
Ø Распределение Максвелла;
Ø Закон Авогадро;
Ø Закон Дальтона..
Уметь записать и назвать величины входящие в них :
Ø уравнение состояния идеального газа и следствия из него;
Ø основное уравнение МКТ идеального газа.
Сведения из теории
Количество однородного вещества (в молях)
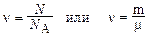 ,
,
где N – число молекул; NА – постоянная Авогадро; m – масса; m – молярная масса вещества.
Если система представляет собой смесь нескольких газов, то количество вещества системы
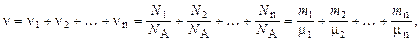 где ni, Ni, mi, mi – соответственно количество вещества, число молекул, масса, молярная масса i-й компоненты смеси.
где ni, Ni, mi, mi – соответственно количество вещества, число молекул, масса, молярная масса i-й компоненты смеси.
Термодинамическая температура
T = 273 + t.
Уравнение состояния идеального газа (уравнение Клапейрона-Менделеева)
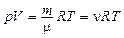 ,
,
где р – давление; V – объем; m – масса; m – молярная масса газа; R – универсальная газовая постоянная; n – количество вещества; Т – термодинамическая температура.
Закон Дальтона, определяющий давление смеси n идеальных газов,
p = p1 + p2 + ... + pn,
где pi – парциальное давление i-й компоненты смеси. Парциальным называется давление, которое производил бы этот газ, если бы только он один находился в сосуде, занятом смесью.
Молярная масса смеси n газов
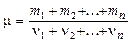 ,
,
где mi и ni – масса и количество вещества 1-го компонента смеси.
Концентрация молекул
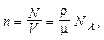
где N – число молекул в системе; V – объем системы; r – плотность вещества; NA – число Авогадро.
Формула справедлива для любого состояния вещества.
Нормальные условия – р0= 1,013·105 Па,
Т0= 273,15 К,
Vm = 22,41·10-3 м3/моль
Зависимость давления газа от концентрации молекул и температуры
p = nkT,
где k –постоянная Больцмана.
Давление газа, оказываемое им на стенку сосуда
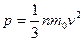 ,
,
где n – концентрация молекул; m0 – масса одной молекулы; v – скорость молекул.
Основное уравнение молекулярно-кинетической теории идеальных газов
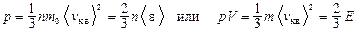 ,
,
где m – масса газа в объёме V; <vкв> – средняя квадратичная скорость молекул; <e> – средняя кинетическая энергия поступательного движения молекул; Е – суммарная кинетическая энергия поступательного движения всех молекул.
Распределение Максвелла
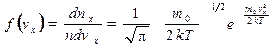
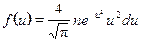
Скорость молекул:
наиболее вероятная – 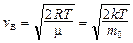 ;
;
средняя квадратичная – 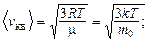
средняя арифметическая – 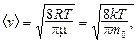
где m0 – масса молекулы.
Барометрическая формула
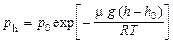 ,
,
где рh и р0 - давление газа на высоте h и h0.
Распределение Больцмана во внешнем потенциальном поле
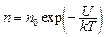 ,
,
где n – концентрация частиц; n0 – концентрация частиц в точках, где U = 0. U – их потенциальная энергия.
Задания для практической части занятия
1. Найти количество вещества ν и число N молекул водорода массой т = 0,5 кг.
2. Баллон объемом 10 л содержит углекислый газ под давлением р = 1,5 МПа и температуре Т = 300 К. Определить массу т газа.
3. Баллон объемом V = 30 л содержит смесь водорода и гелия при температуре T = 300 К и давлении р = 828 кПа. Масса т смеси равна 24 г. Определить массу т1 водорода и массу т2 гелия.
4. При нагревании идеального газа на ΔТ = 2 К при постоянном давлении объем его увеличился на 1/200 первоначального объема. Найти первоначальную температуру Т газа.
5. В баллоне объемом V = 10 л находится гелий под давлением р1 = 1 МПа при температуре T1 = 300 К. После того как из баллона был израсходован гелий массой т = 10 г, температура в баллоне понизилась до T2 = 290 К. Определить давление р2 гелия, оставшегося в бал. лоне.
6. В сосуде вместимостью 3л находится кислород массой 10 г. Определите концентрацию и число молекул кислорода в сосуде.
7. В закрытом сосуде вместимостью V = 20 л находятся водород массой 6 г и гелий массой 12г. Определите давление и молярную массу смеси, если её температура Т = 300 К.
8. В сосуде вместимостью V = 0,3 л при температуре Т = 290 К находится некоторый газ. На сколько понизится давление газа в сосуде, если из него из-за утечки выйдет N = 1019 молекул?
9. В цилиндр длиной l = 1,6 м, заполненный воздухом при нормальном атмосферном давлении, начали медленно вдвигать поршень площадью S = 200 см2. Определить силу, которая будет действовать на поршень, если его остановить на расстоянии 10 см от дна цилиндра.
10. В сосуде объемом V = 15 л содержится азот и водород при температуре t = 230 и давлении р =200 кПа. Определить массы смеси и её компонентов, если массовая доля азота в смеси w1 = 0,7.
11. Оболочка аэростата объемом V = 1600 м3, находящегося на поверхности Земли, на 7/8 заполнена водородом при давлении р = 100 кПа и температуре Т = 290 К. Аэростат подняли на некоторую высоту, где давление давлении р1 = 80 кПа и температура Т 1= 280 К. Определите массу водорода, вышедшего из оболочки аэростата при его подъеме.
12. Колба объемом V = 300 см3 , закрытая пробкой с краном, содержит разреженный воздух. Для измерения давления в колбе горлышко колбы погрузили на незначительную глубину и открыли кран, в результате чего в колбу вошла вода массой т = 292 г. Определить первоначальное давление в колбе, если атмосферное давление равно 100 кПа.
13. Во сколько раз и как изменится средняя скорость движения молекул при переходе от кислорода к водороду?
14. Давление газа равно 1 мПа, концентрация его молекул равна 1010см-3.Определить температуру газа и среднюю энергию поступательного движения молекул газа.
15.Используя основное уравнение МКТ, определите давление, оказываемое газом на стенки сосуда, если его плотность равна 0,01 кг/м3, а средняя квадратичная скорость молекул газа составляет 480 м/с.
16. Определите наиболее вероятную скорость молекул газа, плотность которого при давлении 40 кПа составляет 0,35 кг/м3.
17. На какой высоте давление воздуха составляет 60% от давления на уровне моря? Считайте, что температура воздуха везде одинакова и равна 100С.
18. Пылинки, взвешенные в воздухе, имеют массу т = 10-18 г. Во сколько раз уменьшится их концентрация при увеличении высоты на 10м?. Температура воздуха Т = 300 К.
19. Какая часть молекул кислорода при 00 С обладает скоростью от 100м/с до 110 м/с?
ОТВЕТЫ
№1. ν = 2,5·102 моль; N = 1,5·1026.
№2. m = 0,26 кг.
№3. m1 = 16 г; m2 = 8 г.
№4. Т = 400 К.
№5. р2 = 3,63·105 Па.
№6. 1) n = 6,27·1025 м-3; 2) N = 18,8·1022
№7. 1) М = 0,75 МПа; 2) 3·10-3кг/м3.
№8. Δ р = 133 Па
№9. F = 32, 3 кН.
№10. m1 = 6,87 г; m2 = 4,81 г.
№11. m = 6,2 кг;
№12. р = 2,66 кПа.
№13. Увеличится в 4 раза.
№14. 1) Т = 7250 К; 2) <εп> = 1,5·10-19Дж.
№15 р = 768 Па.
№16 vв = 478 м/с.
№17 h = 4,22 км.
№18 В е 23,6 раза.
№19 f(u) = 0,4%
Практическое занятие № 7
