Обратимые и необратимые процессы.
Обратимым называется такой ТДП, который допускает возвращение тела в первоначальное состояние без каких-либо изменений в окружающей среде. Таким образом, процесс является обратимым, если при совершении его сначала в прямом, а затем в обратном направлении, в исходное состояние возвращается как само тело, так и все внешние тела, с которыми тело взаимодействовало. Необходимым и достаточным условием обратимости ТДП является его равновесность. Характерно, что при обратимом процессе система проходит через те же состояния как в прямом, так и в обратном направлении.
Всякий ТДП, не удовлетворяющий условиям обратимости, называется необратимым ТДП. Так как все реальные процессы являются неравновесными, то и все они необратимы.
Круговой процесс (цикл) – такой ТДП, в результате совершения которого рабочее тело возвращается в исходное состояние, имеющее те же ТД параметры.
Теплоемкость
Теплоемкость тела С – количество энергии в форме теплоты, которое необходимо передать телу, чтобы его температура возросла на 1 К. Q = C ΔT
Удельная теплоемкость тела су - количество энергии в форме теплоты, которое необходимо передать единице массы тела, чтобы его температура возросла на 1 К. Q = су m ΔT
Молярная теплоемкость тела сМ - количество энергии в форме теплоты, которое необходимо передать молю вещества, чтобы его температура возросла на 1 К. Q = сМ νΔT
Удельная теплота фазового перехода (плавление – кристаллизация, испарение – конденсация, возгонка (сублимация)- десублимация) - количество энергии в форме теплоты, которое необходимо передать единице массы вещества, для того, чтобы при температуре фазового перехода перевести ее из менее энергоемкой фазы в более энергоемкую.
Простое вещество – вещество характеризующееся определённым набором физических и химических свойств.
- Оно никаким способом не может быть разложено на два и более веществ.
- Это совокупность атомов, содержащих одинаковое число протонов в ядре.
- Простые вещества могут состоять из одного и того же элемента: белый и красный фосфор, аллотропия углерода.
Химический элемент – вид атомов, характеризующийся определённой совокупностью свойств. Его атрибут валентность. Химический элемент может существовать в виде нескольких простых веществ (аллотропия).
- Это вид атомов, характеризующийся определённой величиной положительного заряда ядра.
Изотопы – атомы, имеющие одинаковое число протонов, но разное число нейтронов в ядре. Химические свойства изотопов тождественны.
Атом – наименьшая частица простого вещества, носитель его свойств, способная существовать самостоятельно и химически связываться с другими элементами.
Молярная масса – отношение массы вещества к его количеству g. Массовое число – общее число нуклонов в ядре.
Литература по темам:
1. И.В. Савельев. Курс общей физики, т. 1. Изд-во «Наука».М.,1973 г. с.511
2. И.В. Савельев. Курс общей физики, т. 1. Изд-во «Наука». М.,1988 г. с.496
3. И.В. Савельев. Курс общей физики, т. 1. Изд-во «Наука». М.,1979 г. с.304
1. Г.А.Зисман и О. М. Тодес. Курс общей физики, т. 1. Изд-во «Наука». М.,1972 г. с.339
2. Г.А.Зисман и О. М. Тодес. Курс общей физики, т. 2. Изд-во «Наука». М.,1965 г. с.366
3. Г.А.Зисман и О. М. Тодес. Курс общей физики, т. 3. Изд-во «Наука». М.,1970 г. с.495
| Тепловые процессы | |||||
| Процесс | Изо- хорический | Изо-барический | Изотерми- ческий | Адиа- батический | Поли- тропный |
| показатель политропы | 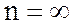 | 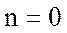 | 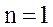 | 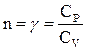 |  |
| уравнение процесса | 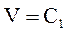 | 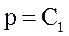 | 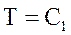 | 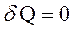 | 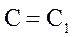 |
| связь между параметрами состояний | 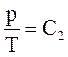 | 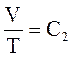 | 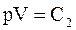 | 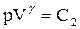 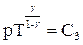 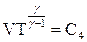 | 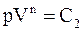 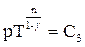 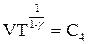 |
| теплота сообщаемая в процессе | 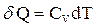 | 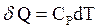 | 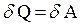 | 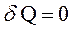 | 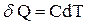 |
| тепло-емкость | 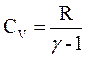 | 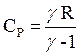 | 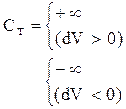 | 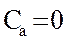 | 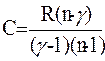 |
| изменение внутренней энергии | 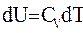 | 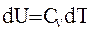 | 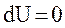 | 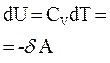 | 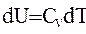 |
| измерение энтальпии | 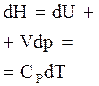 | 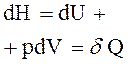 | 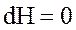 | 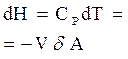 | 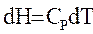 |
| работа в процессе | 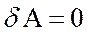 | 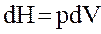 | 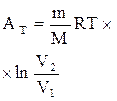 | 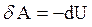 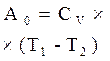 | 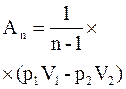 |
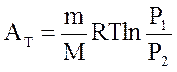 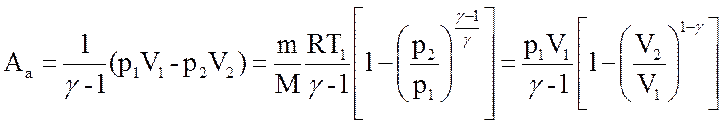 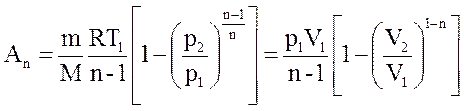 |
