Задания для выполнения на практических занятиях
1. Два моля кислорода очень медленно переводятся из состояния 1 в состояние 2. Какое количество теплоты необходимо подвести к газу, если в координатах PV процесс изображается прямой линией? В состоянии 1 газ характеризуется параметрами Р = 1атм, V = 24,6л, T =300K, P = 3P, V = 2V.
2. Вычислить работу испарения 1 моля воды при переходе ее в пар при 1000С и нормальном давлении. Определить количество теплоты, сообщаемое при этом воде.
3. Вычислить работу, совершаемую за цикл перемагничивания единицы объема сердечника длинного соленоида, если известно, что площадь петли гистерезиса на диаграмме с осями (H, J) равна S.
4. Показать, что элементарная работа поляризации единицы объема диэлектрика равна dW=-(1/4π)E ·dD, а работа поляризации в собственном смысле равна dWc=E ·dP.
5. Термическое и калорическое уравнения состояния идеального электронного газа связаны соотношением PV = 2/3 E. Найти для этого газа уравнение адиабаты в переменных P,V. Е – внутренняя энергия газа.
6. Идеальный газ расширяется по закону р=aV. Найти графически работу, произведенную газом при увеличении объема от V1 до V2. Поглощается или выделяется тепло при таком процессе?
7. Воздух находится в термически изолированной комнате объемом 27 м , в которой имеется небольшое отверстие. Через него воздух может просачиваться наружу, где давление равно 1 атм. Какое количество тепла необходимо подвести в комнату, чтобы температура медленно увеличивалась от 0 до 20°С? Теплоемкость воздуха можно считать постоянной Ср = 103 Дж/(кг • К), г = 1,41
8. Найти работу, совершаемую над молем идеального газа и количество тепла, получаемое им при сжатии от объема V1 до объема V2 в политропическом процессе pVn =const.
9. Молярная теплоемкость идеального газа при некотором процессе изменяется по закону  , где
, где 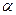 - постоянная величина. Найти уравнение, связывающее параметры Р и V в этом процессе.
- постоянная величина. Найти уравнение, связывающее параметры Р и V в этом процессе.
10. Вычислить разность Cр – Cvдля газа Ван-дерВаальса.
11. Уравнение состояния некоторой термодинамической системы имеет вид Р = АТ3, причем коэффициент пропорциональности А зависит от объема, но не зависит от температуры. Найти ∂Cv/∂V в точке Р= 105 Па, Т = 300К.
12. Процессы PVІ = const, PІV = const, P/V = constявляются политропными PVⁿ = const с различными показателями политропыn. Вычислить соответствующие им теплоемкости.
13. На плоскости с координатными осями V и P через некоторую точку А проведены изотерма Т и адиабата S идеального газа. Показать, что политропные процессы DAD´ и ЕАЕ´ происходят при отрицательной и положительной теплоемкости соответственно.
14. Моль неидеального газа находится в неограниченном сверху цилиндре, помещенном в однородное поле силы тяжести. Вычислить теплоемкость газа.
15. Определить теплоемкости идеального газа в следующих процессах: а) PV2 = const, б) P2V = const, в) P/V = const.
16. Работу двигателей внутреннего сгорания можно моделировать циклом, состоящим из адиабаты, изобары и изохоры. Определить теоретически КПД такого двигателя, если известно, что отношение максимального и минимального объемов газа (степень сжатия) - n.
17. Найти КПД двигателя внутреннего сгорания, работающего по циклу Дизеля. На участке 1 -2 – адиабатное сжатие атмосферного воздуха, 2 -3 изобарное расширение (впрыскивание горючей смеси и ее сгорание), 3 -4 адиабатное расширение, 4 -1 –изохорное охлаждение. Параметрами цикла является степень сжатия е = V1 /V2 и степень предварительного расширения с = V1 /V2.
18. Вычислить энтропию газа Ван – дер – Вальса и найти уравнение его адиабаты.
19. Показать, что энтропия увеличивается, когда, например, горячая вода отдает теплоту такой же массе холодной воды, и температуры их выравниваются.
20. Идеальный газ с показателем адиабаты gсовершает цикл, состоящий из: изохоры, адиабаты и изотермы, причем изотермический процесс происходит при максимальной температуре цикла. Найти КПД каждого цикла, если температура в его пределах изменяется в n раз.
21. Железо массой 200 г при температуре 100 °C опущено в калориметр, в котором находится 300 г воды при температуре 12°C. Пренебрегая теплоемкостью калориметра, найти изменение энтропии системы при выравнивании температур. Удельная теплоемкость железа 500 Дж/кг∙K.
22. Некоторое количество воды нагревают от 10 до 100 °C и дают ей полностью выкипеть. Какой должна быть масса воды, чтобы ее энтропия в данном процессе изменилась на 3,61 кДж/К (парообразованием при t <100°C пренебречь).
23. Методом циклов установить зависимость давления насыщенного пара от температуры.
24. Найти термодинамические потенциалы F,Ф, H для моля одноатомного идеального газа.
25. Определить термодинамические потенциалы при независимых переменных (Р, Н) и (Т, F).
26. Показать, что для веществ, у которых объем линейно зависит то температурыТ, теплоемкость Ср не зависит от давления.
27. Найти уравнение адиабаты и уравнение состояния идеального газа, зная его энтальпию: H=Cp·P(g-1)/g·exp ((s-s0)/ Cp ).
28. Методом циклов найти зависимость ЭДС гальванического элемента от температуры.
29. Показать, что для веществ, у которых давление является линейной функцией температурыТ, теплоемкость Сvне зависит от объема.
30. Энергия Гиббса некоторой системы равна: Ф=аТ(1-lnТ)+RTlnP-TS0 , где a,RиS0 - const. Найти термическое и калорическое уравнения состояния этой системы.
31. Найти условие равновесия в системе, состоящей из жидкости (1) и пара (2) приТ=const, V = const.
32. Показать, что в системе с S = const и Р = const равновесие наступает при минимуме энтальпии Н, а в системе с S = const и V = const - при минимальной внутренней энергии.
33. Определить условия равновесия двух фаз разных веществ, т.е. двухфазной двухкомпонентной системы, когда каждый компонент входит в состав только одной фазы.
34. Определить условия равновесия системы во внешнем силовом поле.
35. Для области температур, в которых удельный объем жидкости можно пренебречь по сравнению с удельным объемом пара, найти зависимость давления насыщенного пара от температуры. Удельную теплоту парообразования считать не зависящей от Т.
36. Идеальный газ находится в адиабатно изолированном цилиндре с поршнем под постоянным давлением. Непосредственно вычислив вариации энтропии дS и дІS, показать, что при равновесии энтропия является максимальной.
37. Показать, что если в некотором состоянии (∂T/∂S)р = 0, то для устойчивости такого состояния должна одновременно обращаться в нуль также и вторая производная, а (∂іT/∂іS)> 0.
38. Найти давление насыщенного пара, учитывая зависимость удельную теплоту перехода л от температуры.
39. Найти выражение для скачка коэффициента теплового расширения Da=an-as и скачкаDК=Кn-Кs модуля упругости при сверхпроводящем переходе.
40. Установить связь между удельными теплотами плавления л 23 (теплота перехода твердого тела 3 в жидкость 2), испарения жидкости л 12 и сублимации л13.
41. Под каким давлением вода будет кипеть при 950С? Удельная теплота испарения воды равна 2258,4 Дж/г.
42. Найти температурную зависимость теплоты фазового перехода dл / dT.
43. Определить коэффициент Джоуля-Томсонав критической точке.
Вопросы, выносимые на самостоятельное изучение:
1. Тема: «Фазовые переходы 2 рода» - Термодинамика сверхпроводящего перехода.
2. Тема: «Термодинамика диэлектриков и магнетиков» - Пьезоэффект. Магнитное (магнитокалорический эффект) и ядерное охлаждения.
3. Тема: «Термодинамика излучения» - Термическое и калорическое уравнение состояния и энтропия равновесного излучения. Термодинамические потенциалы и условие устойчивости равновесного излучения.
4. Тема: «Термодинамика плазмы» - Внутренняя энергия плазмы. Термическое уравнение состояния плазмы.
5. Тема: «Вариационные принципы термодинамики необратимых процессов» - Принцип минимума производства энтропии Пригожина. Вариационный принцип Онзагера. Устойчивость стационарных состояний. Принцип Ле-Шателье в неравновесной термодинамике.
Вопросы для самоподготовки к практическим
Основные понятия и базовые принципы термодинамики
1. Какими независимыми параметрами можно характеризовать состояние равно весной термодинамической системы в отсутствие внешних полей?
2. Как принято называть соотношение, связывающее между собой значения термодинамических параметров вещества в состоянии термодинамического равновесия? Какой вид имеет это соотношение для идеального газа?
3. Что такое состояние термодинамического равновесия?
4. Что такое эмпирическая абсолютная шкала температур?
