Натрия фторид, кальция фторид.
Фтор присутствует в переменных количествах в почве и ествественных водных запасов.
Известны острые и хронические отравления , вызванные приемом пищи, содержащей фториды.Симптомы и признаки острого отравления фторидами включают: тошноту, рвоту, диарею, боль в животе и парастезию.
Объектами исследования на фториды являются главным образом кровь, моча, пищевые продукты и при смертельном исходе — внутренние органы.
Изолирование:тщательно измельченые внутренние органы трупа, содержимое желудка, пищевые продукты и другие объекты в количестве 25 г подщелачивают избытком гидроксида кальция, смачивают раствором нитрата аммония или концентрированной азотной кислотой, высушивают и прокаливаютпри температуре не выше 500 градусов до полного сжигания. Полученную золу смешивают с раствором хлорида кальция, кипетят, охлаждают. Отфильтрованный осадок промывают дистиллированной водой до нейтральной реакции, сжигают остаток вместе с фильтром и золу исследуют на наличие фторидов.
Качественное определение:
1.Часть остатка в платиновом тигле смачивают несколькими каплями воды и обливают небольшим количеством концентрированной серной кислоты, тигель быстро закрывают часовым стеклом, нижняя поверхность которого покрыта воском или парафином. Часть слоя воска или парафина предварительно удаляют. Тигель оставляют на сутки, защитный слой воска или парафина удаляют и наблюдают травление стекла.
2.Часть золы смешивают с SiO2 (песком), помещают в пробирку и приливают концентрированную серную кислоту. В отверстии пробирки держат стеклянную палочку с каплей воды. В случае наличия фтористого водорода капля мутнеет вследствии выделения кремнеевой кислоты.
3.Небольшое количество золы вносят в короткое колено реактивной трубки,заполненной 2% раствором K2Cr2O7 в концентрированной серной кислоте, перемешивают и наблюдают за появлением несмачиваемости стенок трубки в коротком колене — реакция основана на способности HF разрушать стекло и делать его гидрофобным (несмачиваемым).
4.Капельная реакция: при нанесении водного раствора , содержащего F-, на фильтровальную бумагу, пропитанную цирконализариновым лаком, красная окраска бумаги исчезает(красное окрашивание-желтое).
Кремнефтористые соли(фторосиликаты)
Na2SiF6. При выпаривании свободная кремнефтористая кислота разлагается на части:
H2SiF4 ->2HF+SiF4
Сухие кремнефтористые соли разлагаются при нагревании на фтористуюсоль и фтористый кремний:Na2SiF6->2NaF+SiF4.
Качественное определение:
1.К раствору кремнефторида добавляют раствор хлорида бария. Кристаллический осадок отфильтровывают и высушивают на воздухе.
2.Добавление к раствору соли раствора едкого натра вызывает выпадениее осадка кремнеевой кислоты:NaHF2->NaF+HF; 4NaF+SiO2+H2O=SiF4+4NaOH.
3SiF4+3H2O=2H2SiF6+H2SiO3(следы в растворе);
H2SiF6+2NaOH=Na2SiF6+H2O.
Хлор
Свободный хлор имеет широкое применение в технике. Вступая в реакцию с составными частями организма , хлор образует соли хлористоводородной кислоты, являющиеся номальной составной часть организма. Вода действует на хлор очень медленно, но в присутствии легкоокисляющихся веществ происходит быстрый гидролиз хлора,обуславливающий процесс окисления. В связи с этим обнаружение свободного хлора во внутренних органах трупа невозможно. Наблюдающийся иногда в течении двух дней запах хлора от трупа обуславливается продуктами гидролиза хлора, следами хлорноватисной кислоты.
Для обнаружения хлорноватистой кислоты, исследуемый бъект измельчают, помещают в колбу, отверстие колбы закрывают пробкой с двумя трубками, из которых одна доходит до дна трубки и соединена с двумя промывными склянками аппарата Киппа для получения угольного ангидрида. В первую склянку наливают воду , а во вторую раствор нитрата серебра.Другая трубка,оканчивающаяся под пробкой, соединена с двумя склянками Дрекселя, содержащими подкисленный раствор йодида калия,смешанный с крахмальным клейстером. Слабо нагревая колбу с объектом на водяной бане,медленно пропускают ток угольного ангидрида. Отсутствие посинения указывает на отсутствие хлорноватистой кислоты, а также хлора, брома и йода. При появлении посинения ток угольного ангидрида пропускают снова в воду,содержащую сернистую кислоту: NaHSO3+H2SO4=NaHSO4+SO2+H2O.
По кончании пропускания жидкость слабо нагревают до удаления избытка сернистой кислоты и в растворе обнаруживают ион хлора при помощи нитрата серебра, сравнивая цвет осадка с цветом осадка хлорида серебра.
Количественное определение:титрование ратвором нитрата серебра.
Хлорамин
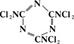 |
представляет собой амид пара-сульфоновой кислоты с толуолом или бензолом, в котором один или два атома водорода амидогруппы замещены активным хлором.
Хлорамины — кристаллические вещества, растворимые в воде и в этиловом спирте.
Качественное определение:
1.При добавлении к раствору хлорамина йодида калия выделяется йод.
2.Ратвор предварительно испытывают реакцией с нитратом серебра на отсутствие иона хлора , затем прибавляют раствор карботана натрия, насыщенного сернистым ангидридом,подкисляют азотной кислотой и добавляют нитрат серебра — оьразуется белый, творожистый осадок, нерастворимый в азотной кислоте.
Йод
Качественное определение,количественное определение:
Лучшим объектом для исследования являются свежие рвотные массы.Пары свободного йода можно вытеснить из объекта током воздуха при слабом нагревании, а затем поглощать разведенным крахмальным клейстером. Посинение раствора укажет на наличие хлора.
Свободный йод легко вступает в соединение с белками и щелочами. Для обнаружение солей йода в биологическом материале ее подщелачивают едким натром и сжигают. Золу после сжигания извлекают горячей водой, раствор фильтруют, сгущают до небольшого объема, прибавляют раствор нитрита натрия, подкисляют разведенной серной кислотой и нагреванием отгоняют йод в раствор крахмального клейстера или в хлороформ. Крахмальный клейстер помещают в две склянки Дрекселя: вторая склянка служит для контроля поглощения. Поглощенный крахмальным клейстером йод титруют 0.1 н раствором тиосульфата натрия, а при малых количествах определяют колориметрически.
Обнаружение йода в моче.
20-100 мл мочи подкисляют разведенной серной кислотой , прибавляют раствор нитрита натрия и взбалтывают с малым количеством хлороформа - получается фиолетовое окрашивание.
Оксид углерода(2)
Оксид углерода (II) представляет собой газ без цвета и запаха. Смесь оксида углерода (II) с воздухом может быть взрывоопасной. При комнатной температуре взрывоопасны смеси, содержащие от 16 до 73 % оксида углерода (II).
Оксид углерода (II) проникает в кровь через дыхательные пути, а затем с гемоглобином крови образует довольно прочное соединение — карбоксигемоглобин (СОНb). Сродство оксида углерода (II) к гемоглобину в 300 раз больше, чем сродство кислорода к указанному оксиду.
В крови лиц, отравленных оксидом углерода (II), содержится гемоглобин и его соединения, к числу которых относятся: гемоглобин, не связанный с кислородом и оксидом углерода (II), или так называемый дезоксигемоглобин (Hb), оксигемоглобин (OHb) — гемоглобин, связанный с кислородом, и карбоксигемоглобин (COHb) — гемоглобин, связанный с оксидом углерода (II). Кроме того, в крови может содержаться некоторое количество метгемоглобина (MtHb). При отравлениях метгемоглобин не связывается с оксидом углерода (II).
В тканях мышц лиц, отравленных оксидом углерода (II), содержится дезоксимиоглобин (MHb), оксимиоглобин (ОMHb) и карбоксимиоглобин (COMHb).
Обнаружение карбоксигемоглобина в крови является доказательством отравления оксидом углерода (II). Для обнаружения и количественного определения карбоксигемоглобина используются: спектроскопические, спектрофотометрические, фотоколориметрические, газо-хроматографические, химические и другие методы.
Качественное определение
1.Спектрофотометрический способ обнаружения:
В крови лиц, отравленных оксидом углерода (II), не весь гемоглобин превращается в карбоксигемоглобин. Смерть наступает значительно раньше, чем достигается полное превращение оксигемоглобина в карбоксигемоглобин.
Карбоксигемоглобин можно обнаружить в крови спектроскопом, который является прибором для визуального спектрального определения ряда веществ, в том числе и карбоксигемоглобина.
При рассматривании крови спектроскопом наблюдаются линии и полосы, позволяющие сделать вывод о наличии или отсутствии карбоксигемоглобина.
Подлежащую исследованию кровь разбавляют водой до тех пор, пока не будет получен раствор, имеющий светло-розовую окраску. При спектроскопическом исследовании этого раствора четко видны соответствующие спектральные полосы.
Спектр оксигемоглобина крови OHb имеет две полосы поглощения между линиями Фраунгофера D и Ε при длинах волн 577—589 и 536—556 нм. Спектр карбоксигемоглобина COHb имеет две полосы поглощения при длинах волн 564—579 и 523— 536 нм.
После прибавления одного объема свежеприготовленного раствора сульфида аммония (NH 4 ) 2 S или других восстановителей (дитионит натрия Na 2 S 2 O 4 ·2H 2 O и др.) к четырем объемам водного раствора исследуемой крови оксигемоглобин (OHb) превращается в дезоксигемоглобин Hb, в спектре которого имеется одна широкая полоса поглощения при 543—596 нм. Карбоксигемоглобин не восстанавливается сульфидом аммония и другими восстановителями. Поэтому после прибавления восстановителей полосы поглощения карбоксигемоглобина не исчезают.
Таким образом, после прибавления раствора сульфида аммония к крови, содержащей окси- и карбоксигемоглобин, сохраняются две полосы поглощения карбоксигемоглобина, но исчезают полосы поглощения оксигемоглобина, а вместо них появляется широкая полоса поглощения дезоксигемоглобина. По наличию соответствующих полос поглощения в спектре крови делают вывод об отравлении оксидом углерода (II).
Спектральный метод оправдывает себя при исследовании крови, содержащей 10—30 % карбоксигемоглобина.
