Термодинамические процессы
Рабочие циклы поршневых двигателей внутреннего сгорания состоят из ряда термодинамических процессов. Под термодинамическим процессом следует понимать определенное, взаимосвязанное изменение основных параметров рабочего тела, т.е. изменение состояния газа. Преобразование тепловой энергии в механическую работу происходит за счет сгорания газовой смеси и изменения состояния рабочего тела (газа). Основное свойство газов – способность равномерно заполнять занимаемый объем. При изменении объема газы сжимаются или расширяются. Во время рабочего цикла, кроме изменения объема, происходит передача или отвод теплоты от находящихся в цилиндре газов. Зависимость между основными параметрами идеальных газов (температурой, давлением и занимаемым объемом) выражается характеристическим уравнением (уравнением состояния):
pV = GRT,
где p – давление газов; V – объем газа; G – масса газа; R – газовая постоянная (величина, зависящая от свойств газа); T – абсолютная температура.
Термодинамические процессы, протекающие с постоянным количеством газа, можно графически изобразить на диаграмме, где по оси ординат откладывают давление p, а по оси абсцисс – объем V. Такая диаграмма называется изображением процесса в p-V координатах или pV – диаграммой.
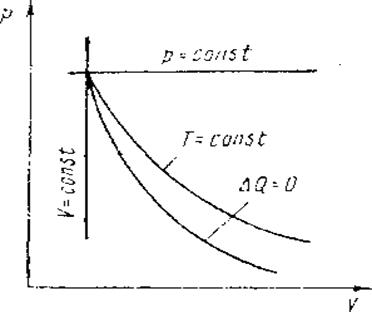
К характерным термодинамическим процессам относятся: изохорный, изобарный, изотермический и адиабатный. Изображения этих процессов в p-V координатах показано на рисунке 1.1.
При изохорном процессе изменение состояния газа происходит при постоянном объеме (V = const). На pV – диаграмме изохорный процесс изображается вертикальной прямой. По характеристическому уравнению при V = const температура изменяется пропорционально изменению давления:
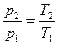 ,
,
где p1 и T1 – давление и температура в начале процесса, а p2 и T2 – в конце процесса.
При изобарном процессе изменение состояния газов происходит при постоянном давлении (p = const). При этом процессе изменение температуры газа пропорционально изменению объема:
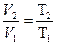 ,
,
где V1 и T1 – объем и температура в начале процесса, а V2 и T2 – в конце процесса.
При изотермическом процессе изменение состояния газов происходит при постоянной температуре (Т = const). В этом случае изменение объема обратно пропорционально изменению давления:
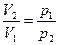 ,
,
где V1 и p1 – объем и температура в начале процесса, а V2 и p2 – в конце процесса.
Если газ расширяется или сжимается без подвода или отвода теплоты, то такой процесс называется адиабатным (ΔQ = 0). Зависимость между объемом и давлением в этом случае определяется уравнением
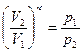 ,
,
а изменение объема и температуры
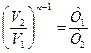 ,
,
Величина κ называется показателем адиабаты. Эта величина неодинакова для разных газов и несколько уменьшается при повышении температуры. Для воздуха κ = 1,41.
Действительные процессы расширения и сжатия газов происходят по политропам (pVn = const). В этом случае
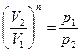 ;
; 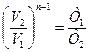 ,
,
где n – показатель политропы.
Политропный процесс является обобщающим. В зависимости от значения показателя политропы (n) можно получить рассмотренные ранее процессы, которые являются частными случаями политропного процесса. Показатель политропы (n) зависит от характера протекания процесса. В теоретических циклах (в отличие от действительных) отсутствуют какие-либо потери. Исключение составляет неизбежная отдача тепла холодному источнику, без которой согласно второму закону термодинамики невозможно превращение в двигателе теплоты в работу.
Для определения наиболее общих закономерностей термодинамических процессов, происходящих в цилиндрах двигателей внутреннего сгорания, рассматривают теоретические циклы ДВС. При этом принимают определенные допущения, упрощающие исследование и расчеты процессов в цилиндрах ДВС.
Рис. 1.1. Характерные термодинамические процессы