Тема 4. Термодинамические процессы
Метод исследования т/д процессов
Как сказано выше первый закон т/д устанавливает взаимосвязь между количеством теплоты, внутренней энергией и работой. При этом, количество теплоты подводимое к телу или отводимое от тела зависит от характера процесса.
К основным т/д процессам относятся: изохорный, изотермический, изобарный и адиабатный.
Для всех этих процессов устанавливается общий метод исследования, который заключается в следующем:
- выводится уравнение процесса кривой Pυ и TS – диаграммах;
- устанавливается зависимость между основными параметрами рабочего тела в начале и конце процесса;
- определяется изменение внутренней энергии по формуле, справедливой для всех процессов идеального газа:
Du = сvм|0t2·t2 - сvм|0t1·t1. (4.1)
или при постоянной теплоемкости DU = m·сv·(t2 - t1); (4.2)
вычисляется работа: L = P·(V2 – V1); (4.3)
определяется количество теплоты, участвующее в процессе:
q = cx·(t2- t1); (4.4)
определяется изменение энтальпии по формуле, справедливой для всех процессов идеального газа:
Di = (i2 – i1) = сpм|0t2·t2 – сpм|0t1·t1, (4.5)
или при постоянной теплоемкости: Di = сp·(t2 – t1); (4.6)
определяется изменение энтропии:
Ds = cv·ln(T2/T1) + R·ln(υ 2/υ 1) ; (4.7)
Ds = cp·ln(T2/T1) - R·ln(P2/P1) ; (4.8)
Ds = cv·ln(T2/T1) + cp·ln(υ 2/υ 1) . (4.9)
Все процессы рассматриваются как обратимые.
Изопроцессы идеального газа
1). Изохорный процесс (Рис.4.1).
n = Const , n 2 = n 1. (4.10)
Уравнение состояния процесса:
P2 / P1 = T2 / T1. (4.11)
Так как υ 2 = υ 1, то l = 0 и уравнение 1-го закона т/д имеет вид:
q = Du = = сv·(t2 - t1); (4.12)

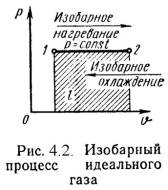
2). Изобарный процесс (Рис.4.2).
P = Const , P2 = P1
Уравнение состояния процесса:
n 2 /n 1 = T2 / T1 , (4.13)
Работа этого процесса:
l = P·(n 2 - n 1). (4.14)
Уравнение 1-го закона т/д имеет вид:
q = Du + l = ср·(t2 - t1); (4.15)
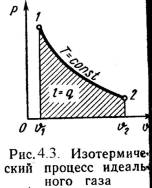
3). Изотермический процесс (Рис.4.3).
Т = Const , Т2 = Т1
Уравнение состояния:
P1 / P2 = n 2 / n 1 , (4.16)
Так как Т2 = Т1, то Du = 0 и уравнение 1-го закона т/д будет иметь вид:
q = l = R·T·ln(n 2/n 1), (4.17)
или q = l = R·T·ln(P1/P2), (4.18)
где R = Rh/ h – газовая постоянная [Дж/(кг·К)].
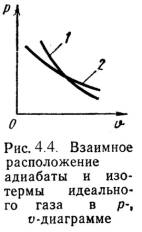
4). Адиабатный процесс (Рис.4.4).
В данном процессе не подводится и не отводится тепло, т.е. q =0.
Уравнение состояния:
P· nl = Const, (4.19)
где l = cp / cv – показатель адиабаты.
Уравнение 1-го закона т/д будет иметь вид:
l = -Du = = -сv·(t2 – t1) = сv·(t1 – t2), (4.20)
или
l = R·(T1 – T2) / (l -1); (4.21)
l = R·T1·[1 – (n 1/ n 2)l -1] /(l – 1); (4.22)
l = R·T2·[1 – (P2/P1) (l -1)/ l] /(l – 1). (4.23)
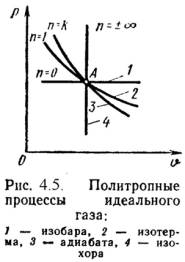
Политропный процесс
Политропным процессом называется процесс, все состояния которого удовлетворяются условию:
P· nn = Const, (4.24)
где n – показатель политропы, постоянная для данного процесса.
Изобарный, изохорный, изотермический и адиабатный процессы являются частными случаями политропного процесса (Рис.4.5):
при n = ± ¥ n = Const, (изохорный),
n = 0 P = Const, (изобарный),
n = 1 T = Const, (изотермический),
n = l P· n= Const, (адиабатный).
Работа политропного процесса определяется аналогично как при адиабатном процессе:
l = R·(T1 – T2) / (n – 1); (4.25)
l = R·T1·[1 – (n 1/ n 2) n-1] /(n – 1); (4.26)
l = R·T2·[1 – (P2/P1) (n-1)/ n] /(n – 1). (4.27)
Теплота процесса:
q = cn ·(T2 – T1), (4.28)
где cn = cv ·(n - l)/(n – 1) – массовая теплоемкость (4.29)
политропного процесса.
Тема 5. Термодинамика потока
