Амиотрофия – это прогрессирующая утрата мышечной массы. Она сопровождается потерей мышечной силы.
Основные пункты:
· Признаки
· Описание
· Диагностика
· Лечение
· Образ жизни
· Профилактика
Признаки
Страдающие амиотрофией чувствуют подергивание в мышцах, боль при ходьбе, мышечную слабость. Со временем изменяется их походка. У них нарушается кожная чувствительность, кожа отечная, приобретает синюшный оттенок. Часто патологический процесс затрагивает и спину, поэтому у страдающих амиотрофией часто развиваются сколиоз, кифоз, а также нарушения дыхания из-за того, что поражаются и межреберные мышцы. Так как первыми поражаются мышцы стоп и голеней, нога пациента похожа на перевернутую бутылку.
Для некоторых амиотрофий характерны чувствительные расстройства в руках и ногах – пациенты ощущают «мурашки». Также возможен и «симптом топтания», при котором при усталости человек начинает переступать с ноги на ногу.
Описание
При амиотрофии нарушается питание мышцы. И нарушается оно из-за дегенерации нерва, который эту мышцу возбуждает. Процесс затрагивает не только периферические нервы, но и спинной мозг – он уменьшается в объеме, происходит дегенерация его передних корешков. Пораженные нервные клетки замещаются глиозной тканью (клетками глии – вспомогательными клетками нервной ткани).
Амиотрофия может быть двух видов: спинальная и невральная.
Спинальная амиотрофия – это наследственное заболевание мотонейронов спинного мозга. Причем кодирует это заболевание рецессивный ген, то есть, проявляется оно у ребенка, только если гены есть у обоих родителей и при этом ребенку от родителей достались оба «неполноценных» гена. При этом заболевании не нарушается чувствительность кожи, не нарушена координация. А так как заболевание наследственное, то возраст начала болезни примерно одинаковый в каждой семье. Существует несколько типов спинальной амиотрофии:
· спинальная амиотрофия Верднига-Гоффмана 1, которая развивается у ребенка до года и приводит к раннему летальному исходу;
· спинальная амиотрофия Верднига-Гоффмана 2, начинающаяся в возрасте 1,5-2 лет. С этой болезнью продолжительность жизни до 30 лет;
· спинальная амиотрофия Кульдберга-Веландер, которая развивается у подростков, и живут с ней более 40 лет;
· спинальная амиотрофия Кеннеди, которая развивается у взрослых людей. При этом заболевании увеличиваются молочные железы.
Невральная амиотрофия Шарко-Мари-Тута – это также наследственное заболевание. Первые признаки этого заболевания проявляются в основном в 15-30 лет, причем мужчины страдают им чаще, чем женщины. Прогрессирует болезнь медленно. При этом заболевании разрушаются периферические нервы.
Амиотрофия может развиться и у тех, у кого нет наследственной предрасположенности – в результате травмы, охлаждения или авитаминоза. Она также может быть симптомом некоторых заболеваний, например, сахарного диабета и некоторых форм сифилиса.
Очень часто страдающие амиотрофией болеют различными простудными заболеваниями – бронхитами, пневмониями. Это происходит из-за слабости межреберных мышц и, как следствие, нарушения дыхательной функции.
Диагностика
Для диагностики амиотрофии необходимо провести игольчатую и стимуляционную электронейромиографию, а также генетический и генеалогический анализы. Важен и тщательный осмотр пациента.
Лечение
Спинальную амиотрофию лечат симптоматически. То есть, только убирают симптомы заболевания. Лечение заключается в хорошем питании, регулярной лечебной физкультуре и проведение мероприятий по предотвращению контрактур (сжатия и укорочения) мышц.
Лечение невральной амиотрофии направлено на прекращение дегенерации нервов. К сожалению, этот процесс нельзя повернуть вспять, можно только остановить. Поэтому важно своевременно начать лечение. Назначают препараты, улучшающие нервно-мышечную передачу, а также Вивитамины Е и группы В, аутогемотерапию, лечебную гимнастику, физиотерапию (электрофорез и ультразвук) и бальнеотерапию (радоновые и сероводородные ванны).
Образ жизни
Страдающие амиотрофией могут работать, но должны выбирать профессии, не связанные с физическими нагрузками. Этим людям не рекомендуется иметь детей, так как высока вероятность передать заболевание по наследству.
Профилактика
Профилактики наследственной амиотрофии не существует. Единственное, что можно сделать – это вовремя пройти обследование, сделать все необходимые анализы и начать лечение как можно раньше.
Если же амиотрофия – симптом другого заболевания, то необходимо лечить основное заболевание. Также нужно избегать переохлаждений и травм.
24. В список прогрессирующих мышечных дистрофий (ПМД) входят миодистрофии: псевдогипертрофическая Дюшенна; псевдогипертрофическая Беккера-Кинера; Эмери-Дрейфуса-Хогана; Роттауфа (фиброзирующая миопатия); ювенильная Эрба-Рота; окулярная (офтальмоплегия Грефе); плече-лопаточно-лицевая (Ландузи); окулофарингеальная; Дрейфуса; митохондриальные. Причины мышечных дистрофий У больных ПМД выявляется врожденный структурный дефект мышечной ткани (например, при ПМД Дюшенна — дефект гена, отвечающего за синтез структурного мышечного белка дистрофина). В отличие от утраты этого белка при миодистрофии Дюшенна, при миодистрофии Беккера дистрофин качественно изменен. У больных ПМД отмечают нарушения: возбудимости и проводимости мышечных волокон; микроциркуляции; нейротрофических влияний; метаболизма мышц. Провоцирующими факторами выступают, в частности, инфекции, интоксикации, травмы (физические и/или психические) и соматические заболевания. Симптомы мышечных дистрофий Общие симптомы ПМД: мышечная слабость (симметричная); отсутствие перманентной боли; более частое проявление слабости в проксимальных отделах, ее преобладание в мышцах тазового, плечевого пояса; снижение и угасание сухожильных рефлексов пропорционально мышечной слабости. В целом клиническая характеристика семейных и спорадических форм миопатий сходна. Прогрессируют медленно и постепенно. Локализация атрофий при различных формах миопатий: плечевые; тазовые; тазо-плечевые; плече-лопаточно-лицевые; дистальные; глазные; глазо-бульбарные; смешанные. Характер распространения мышечной дистрофии — восходящий или нисходящий. Походка принимает так называемый утиный характер. Из положения лежа больные поднимаются с помощью дополнительных движений — приемов миопата. Наряду с атрофиями наблюдаются псевдогипертрофии мышц (у 37% больных), преимущественно в икроножных и четырехглавых мышцах, реже в дельтовидных, надостных, подостных и межреберных мышцах. Слабость мышц нарастают по мере развития заболевания и приводят к снижению мышечной силы, которую в поздних стадиях оценивают в 0-1 балл (по пятибалльной системе). Одновременно с нарастанием выраженности атрофий скелетных мышц отмечается понижение и угасание сухожильных надкостничных рефлексов. У большинства больных (83,5%) определяются вегетативно-сосудистые изменения: гипергидроз, акроцианоз стоп и ладоней, повышенная лабильность вазомоторов, стойкий красный дермографизм. Для различных форм первичных миодистрофий характерны и некоторые общие симптомы и феномены. Миодистрофия псевдогипертрофическая Дюшенна Псевдогипертрофическая мышечная дистрофия Дюшенна — злокачественная форма ПМД. Заболевание наследуется сцепленно с Х-хромосомой. При миодистрофии Дюшенна идентифицировано генетически обусловленное отсутствие структурного мышечного белка дистрофина, что ведет к запуску каскада химических реакций, вызывающих гибель миофибрилл. В соответствии с таким типом наследования болезни болеют обычно мальчики, матери которых являются носителями рецессивного гена. При миодистрофии Дюшенна существует эффект деда: от деда заболевание может передаться через дочь внуку. Первые признаки мышечной дистрофии появляются на первом году, а к его концу становится заметным отставание детей в развитии. С 2 лет отмечается слабость мышц. Основные проявления «Утиная» походка Пациент при ходьбе «переваливается» с ноги на ногу, что обусловлено слабостью ягодичных мышц Псевдогипертрофии — «икры гнома» Псевдогипертрофия икр из-за их жировой инфильтрации, разрастания соединительнотканных образований. Мышцы выпуклые, плотные на ощупь, но сила снижена (признак миопатии Дюшенна) «Лягушачий живот» При некоторых формах нервно-мышечной патологии низкий тонус мышц приводит при мышечной дистрофии к тому, что живот выступает вперед. Симптом «вялых надплечий» Если ребенка приподнять, взяв его подмышки, то предплечья резко поднимаются, и голова больного «тонет» между ними — признак выраженной гипотонии мышц плечевого пояса «Поперечная» улыбка Слабость и гипотрофия лицевой мускулатуры могут сопровождаться изменением мимики, в частности поперечным растягиванием рта. Признак некоторых форм миопатии. Симптом Шерешевского-Говерса Пациент с миопатией, вставая из положения лежа, совершает ряд движений (поворачивается на живот, становится на четвереньки), а затем начинает подниматься, постепенно разгибая ноги и опираясь руками; руки его последовательно меняют положение, при этом больной «вскарабкивается» по собственным ногам, как по приставной лестнице. Триада синдромов при мышечной дистрофии: трех «А» Атрофии (гипотрофии) Атонии (гипотонии) Арефлексии (гипорефлексии) тазового пояса, вследствие чего возникает «утиная» походка. Характерное распространение при мышечной дистрофии миодистрофического процесса восходящее — со временем в процесс вовлекаются все мышцы туловища и плечевого пояса. Грудная клетка уплощена, отмечают сколиоз грудного отдела и поясничный гиперлордоз. К 7 годам больные с трудом передвигаются, к 12-15 годам они утрачивают возможность ходить. Характерны феномены Шерешевского-Говерса, поясничный гиперлордоз, псевдогипертрофия отдельных мышечных групп. Типична псевдогипертрофия икр («икры гнома»), при подъеме больные испытывают выраженные трудности. С вовлечением мышц плечевого пояса формируются «крыловидные» лопатки, кифосколиоз, развивается слабость рук, дыхательной мускулатуры. В поздней стадии миодистрофического процесса возникают гипотрофия мышц лица, глотки и гортани; отмечается сгибательная контрактура в суставах конечностей. Развивается кардиомиопатия (расширение границ сердца, нарушения сердечного ритма), возникают изменения электрокардиограммы (ЭКГ), возможны адипозогенитальный синдром, гипоплазия надпочечников и остеопороз. Около трети больных (30%) отстают в развитии интеллектуальных функций. В ранней стадии резко (в десятки и сотни раз) возрастает активность КФК, а также активность ЛДГ. Миодистрофия псевдогипертрофическая Беккера-Кинера Псевдогипертрофическую мышечную дистрофию Беккера-Кинера рассматривают как мягкую форму ПМД Дюшенна. Заболевание также передается сцепленно с Х-хромосомой. Дебют заболевания отмечается в возрасте от 5 лет. Течение миодистрофического процесса медленно прогрессирующее. Особенности распространения мышечных дистрофий идентичны признакам мышечной патологии при ПМД Дюшенна. Менее выражена патология сердца. Интеллект пациентов сохранен; они долго сохраняют способность самостоятельно передвигаться, могут иметь детей. Миодистрофия Эмери Мышечная дистрофия Эмери-Хогана наследуется сцепленно с Х-хромосомой. Рано развиваются ретракции пяточных сухожилий, при ходьбе отмечают опору на пальцы, а также проявление «утиной» походки. Отмечают миокардиодистрофию, множественные контрактуры крупных суставов, ригидность позвоночника, бочкообразную грудную клетку. Активность КФК умеренно повышена. Течение медленно прогрессирующее. Интеллект сохранен. Миодистрофия Роттауфа (фиброзирующая) Продажа Татами arenasporta.pro Татами от российского производителя по выгодным ценам! Будо-Маты Ролл-Маты Стеновые протекторы Доставка Адрес и телефон Скрыть рекламу: Не интересуюсь этой темой / Уже купил Навязчивое и надоело Сомнительного содержания или спам Мешает просмотру контента Спасибо, объявление скрыто. Надежный брокер AMarkets! amarkets.today Официальный сайт AMarkets. Начни сегодня с бонуса 25%. Бесплатное обучение. Бонус 25% на счет Бесплатное обучение Сервис RoboX Инвестирование Адрес и телефон Скрыть рекламу: Не интересуюсь этой темой / Уже купил Навязчивое и надоело Сомнительного содержания или спам Мешает просмотру контента Спасибо, объявление скрыто. Купить Смартфоны Oppo kaspi.kz Переплата 0 тг на 3 меcяца. Смартфоны Oppo от 2 889 тенге в месяц! OPPO A37f Gold OPPO F3 Gold OPPO A57 Gold PPO A57 Black АО «Kaspi Bank» Скрыть рекламу: Не интересуюсь этой темой / Уже купил Навязчивое и надоело Сомнительного содержания или спам Мешает просмотру контента Спасибо, объявление скрыто. Яндекс.Директ Дебют мышечной дистрофии происходит в детском возрасте, обычно в 4-12 лет. Возникают выраженные сухожильные контрактуры. Отмечают ограничения тыльного разгибания стоп, сгибания шеи. Вследствие фиброза мышц формируются патологические позы, приводящие к невозможности сгибания позвоночника. Миодистрофический процесс медленно прогрессирует. Появляются мышечная слабость и умеренные гипотрофии, больше в лопаточно-плечевой области. Интеллект сохранен. Развивается кардиомиопатия. Характерна выраженная гиперферментемия. ЭМГ выявляет изменения, указывающие на первичный миодистрофический процесс. Ювенильная миодистрофия В первую очередь болезнь характеризуется атрофией мышц таза. Ранним проявлением заболевания служит «утиная» (миопатическая) походка. Пациент испытывает затруднения при попытке сесть из положения лежа. Выявляют поясничный гиперлордоз, «лягушачий» живот, атрофии верхних конечностей (форма Лейдена-Мебиуса). Возможно развитие умеренных псевдогипертрофий. На фоне вовлечения в процесс межреберных мышц, диафрагмы может возникнуть дыхательная недостаточность. У больных вероятны эндокринопатии (ожирение) и вегетативная дистония. Течение миодистрофического процесса относительно мягкое. При неблагоприятных условиях (например, при физических нагрузках) возможно быстрое прогрессирование процесса. На ЭМГ при мышечной дистрофии присутствует картина первичного миодистрофического процесса. На ЭНМГ скорость импульса в пределах возрастной нормы. В крови определяется умеренная гиперферментемия. Миодистрофия плече-лопаточно-лицевая (Ландузи) Заболевание наследуется аутосомно-доминантно. Предположительно патологический ген локализован на хромосоме 4. Отмечается выраженная пенетрантность гена. Дебют заболевания обычно происходит к 20 годам, болезнь начинается со слабости мышц лица. Рано наблюдаются «губы тапира», улыбка Джоконды). Со временем нарастает похудание и слабость передней зубчатой и большой грудной мышц. Позже миодистрофический процесс затрагивает перонеальную группу мышц, возникает походка «степпаж». Развивается умеренная псевдогипертрофия мышц. Креатин-креатининовый обмен нарушен умеренно. Миодистрофия окулярная (Грефе) Заболевание дебютирует до 30-летнего возраста. Нарастает поражение глазных мышц, которое протекает без диплопии, приводит к обездвиженности глазных яблок (параличу взора). Сначала часто поражается мышца, поднимающая верхнее веко; в поздней стадии миодистрофического процесса наблюдается двусторонний птоз. Иногда вовлекаются мимические, бульбарные и скелетные мышцы. Миодистрофия окулофарингеальная Окулофарингеальная миодистрофия — классическая наружная офтальмоплегия с дисфагией и дисфонией, наследуемая аутосомно-доминантно. В 1961 г. заболевание описано у представителей франко-канадской популяции. Классический вариант болезни — прогрессирующая офтальмоплегия с дисфагией и дисфонией, сопровождаемая птозом верхних век. Другой вариант болезни протекает с присоединением пареза мышц, обеспечивающих движения глаз, мимической и жевательной мускулатуры, мышц шеи. При третьем, редком варианте в процесс вовлекаются также мышцы конечностей. Активность ферментов (КФК и ЛДГ) несколько повышена. Миодистрофия Дрейфуса Мышечная дистрофия Дрейфуса проявляется нарастающей слабостью мышц, преимущественно тазового пояса и нижних конечностей. Характерна походка больного с опорой на большие пальцы; отмечается поясничный гиперлордоз. Особенность этой формы миодистрофии — формирование выраженных контрактур локтевых и других суставов. Нередко поражается миокард, больной отстает в психическом развитии. Миопатии митохондриальные При митохондриальных миопатиях биохимический дефект локализован в митохондриях клеток, что выявляют при биохимическом и ультрамикроскопическом исследованиях. Чаще всего дебют заболевания происходит на 2-м десятилетии жизни. На ранних стадиях возникают птоз, наружный офтальмопарез (без диплопии вследствие симметричности поражения глазодвигательных мышц), слабость проксимальных мышцах, сухожильная гипо- и арефлексия. Длительность прогрессирования мышечной дистрофии вариабельна: от месяцев до десятилетий. Клинико-нейрофизиологические исследования (ЭМГ, ЭНМГ) при митохондральных миопатиях выявляют миодистрофические и невропатические проявления. Диагностика Для постановки диагноза необходимы нейрофизиологические, биохимические и патогистологические исследования. Локальная ЭМГ. У больных миопатиями регистрируется патологическая интерференция с высокой частотой полифазных потенциалов и укорочением времени формирования отдельных осцилляций. Биохимическое исследование. На ранних стадиях активность КФК крови увеличивается в 50 раз и более; ЛДГ — в 5-7 раз; ФДА — в 2-5 раз; в поздних стадиях снижается до возрастной нормы. Патогистологическое исследование. Определяются признаки ПМД: перерождение мышечной ткани; беспорядочное расположение разнокалиберных мышечных волокон; чередование нормальных, атрофированных и (в некоторых мышцах) гипертрофированных волокон; атрофия мышечных волокон в длину и в поперечнике; пролиферация ядер с их расположением под сарколеммой и внутри волокна. Лечение мышечных дистрофий Лечение первичных направлено на замедление темпа развития заболевания и максимальное сохранение способности больного к самообслуживанию. Тактика лечения ПМД: диетотерапия с целью избежать развития у больного избыточной массы тела; ЛФК и двигательная активность, в частности, для поддержания функций опорных суставов и предотвращения контрактур; дыхательная гимнастика; медикаментозная терапия; социально-психологическая реабилитация; ортопедическая помощь. При некоторых формах миодистрофий, в частности при миодистрофии Дюшенна, применение глюкокортикоидов иногда позволяет отодвигать наступление обездвиженности больного на годы. Поскольку такое лечение длительное и обычно сопровождается многими осложнениями, необходимо обдуманное назначение глюкокортикоидов. При ПМД применяют (с учетом возможных противопоказаний) преднизолон 1-2 мг/кг утром, через день, возможен и ежедневный прием преднизолона при мышечной дистрофии (утром однократно в дозе 0,75 мг/кг/сутки). Авторы предлагают применять также препарат этой же группы — дефлазакорт, обладающей меньшими побочными эффектами, приблизительно в той же дозе (по эффективности 6 мг дефлазакорта соответствуют 5 мг преднизолона). Длительность лечения зависит от эффективности и выраженности побочных действий препарата. Показана симптоматическая и общеукрепляющая терапия. В частности, рекомендуют применение аденозина фосфата, трифосаденина, витамина Е, коферментов (например, кокарбоксилазы), негормональных анаболических средств (этилтиобензимидазола, оротовой кислоты), инозина, препаратов калия. При этом надо иметь в виду недоказанность объективных проявлений эффективности этих препаратов. Рекомендуемая схема медикаментозного лечения ПМД: Преднизолон внутрь (утром) по 1-2 мг/кг/сутки через день, длительность терапии определяют индивидуально, или Преднизолон внутрь (утром) по 0,75 мг/кг/сутки ежедневно, длительно или Дефлазакорт внутрь по 6 мг, длительно.
Источник: http://surgeryzone.net/nevrologia/myshechnye-distrofii.html
25.Семейная спастическая параплегия (болезнь Штрюмпеля) — дегенеративная наследственная миелопатия с двусторонним поражением боковых и передних спинномозговых столбов преимущественно на поясничном уровне. Базовым клиническим симптомом выступает центральный парапарез нижних конечностей. Диагностировать болезнь Штрюмпеля позволяет типичная симптоматика, наличие семейного анамнеза, данные ЭНМГ, исследования вызванных потенциалов, МРТ и генетических анализов. Лечение основано на постоянном приеме, внутримышечном или эндолюмбальном введении миорелаксантов в комбинации с лечебной физкультурой и физиотерапией.
· Классификация болезни Штрюмпеля
· Симптомы болезни Штрюмпеля
· Диагностика болезни Штрюмпеля
· Лечение и прогноз болезни Штрюмпеля
· Цены на лечение
Болезнь Штрюмпеля
Семейная спастическая параплегия впервые была описана в 1883 г. немецким клиницистом А. Штрюмпелем. В дальнейшем изучением этой патологии занимался М. Лорен. В честь этих исследователей в медицинскую практику было введено эпонимическое название — болезнь Штрюмпеля-Лорена, которое в современной неврологии чаще употребляется как болезнь Штрюмпеля. Патогенетическим субстратом заболевания выступает прогрессирующее глиальное перерождение пирамидных трактов передних и боковых столбов на уровне грудных и поясничных сегментов спинного мозга. Наряду с этим могут наблюдаться атрофические процессы в передних рогах, дегенерация проводящих путей мозжечка, уменьшение числа нейронов моторной зоны коры, глиоз пирамидных трактов на уровне ствола мозга.
Данные о распространенности болезни Штрюмпеля варьируют, в среднем она составляет около 3,8 случаев на 100 тыс. населения. Возрастной период дебюта клинической картины весьма широк: от 1 до 80 лет. Однако чаще всего болезнь Штрюмпеля манифестирует в возрасте 10-30 лет. В результате бурного развития генетики в последнее время было выявлено и продолжает открываться множество генетических вариантов семейной спастической параплегии. В настоящее время выделяют не менее 17 хромосомных локусов, дефекты в которых обуславливают болезнь Штрюмпеля с аутосомно-доминантным наследованием, 29 локусов, ответственных за аутосомно-рецессивные типы заболевания, и 4 локуса, связанные с наследуемыми Х-сцепленно формами.
Классификация болезни Штрюмпеля
В клинической практике применяется классификация семейной спастической параплегии, учитывающая сразу несколько различных аспектов. В зависимости от механизма наследования выделяют аутосомно-доминантные, аутосомно-рецессивные и Х-сцепленные формы. В первом случае, если болезнь Штрюмпеля имеется у одного из родителей, то вероятность заболевания у потомков составляет 50%. Во втором — заболевание у ребенка возможно, если оба родителя являются носителями дефектного гена, риск рождения больного ребенка - 25%. При наследовании, сцепленном с Х-хромосомой, заболевают только лица мужского пола, женщины являются носительницами патологического гена.
По клиническим проявлениям болезнь Штрюмпеля классифицируют на неосложненные (простые) и осложненные (сложные) формы. Первые не сопровождаются другими ведущими симптомами, кроме спастического нижнего парапареза, вторые представляют собой его сочетание с другими неврологическими нарушениями (эпилепсией, задержкой психического развития, расстройством слуха, атрофией зрительных нервов, ретинопатией, мозжечковой атаксией, дизартрией). Различают также болезнь Штрюмпеля с началом в детском, подростковом и взрослом возрасте.
По виду генного дефекта классификация строится в виде числовой последовательности. Используется англоязычная аббревиатура гена семейной спастической параплегии — SPG, после которой следует цифра от 1 до 56 и более (в связи с постоянным обнаружением новых видов мутаций). Исследования показали, что наиболее распространенным является тип SPG4, который составляет до 40% случаев заболевания.
Симптомы болезни Штрюмпеля
При раннем дебюте болезни первыми симптомами выступают задержка при формировании навыков ходьбы и хождение на цыпочках. При начале в более старшем возрасте клиника манифестирует затруднениями при ходьбе с частыми падениями. Зачастую первой жалобой пациентов становиться «плохая опора стоп при ходьбе», «скованность в ногах». Повышение мышечного тонуса в ногах присутствует с самого начала болезни. В период дебюта оно может носить транзиторный характер: усиливаться при ходьбе и исчезать в покое. Спастичность преобладает в камбаловидных мышцах голени, приводящих и задних мышцах бедра. Она может иметь асимметричный характер. В некоторых случаях пациент жалуется на проблемы лишь с одной ногой. Однако неврологический осмотр выявляет двустороннее повышение тонуса и гиперрефлексию обеих ног с наличием пирамидных стопных знаков (Оппенгейма, Бабинского, Бехтерева, Россолимо и пр.), может вызываться клонус стоп.
Болезнь Штрюмпеля характеризуется постепенным развитием. Снижение силы в мышцах ног (парез) появляется спустя достаточно длительный период. При аутосомно-рецессивных формах он составляет несколько лет, при доминантных — еще больше. Из сенсорных расстройств у части пациентов отмечаются легкие нарушения вибрационного восприятия, иногда — парестезии в голенях и стопах. Более выраженные нарушения чувствительности наблюдаются при присоединении полиневропатии, обычно при осложненных формах.
Атрофические изменения мышц ног, как правило, возникают на поздних стадиях болезни Штрюмпеля и обусловлены обездвиженностью вследствие выраженного пареза. Некоторые формы семейной наследственной параплегии (SPG10 и SPG17) сопровождаются атрофией мышц рук. В далеко зашедшей стадии заболевания может возникнуть спастический парез верхних конечностей и недержание мочи. Последнее более типично для пациентов пожилого возраста, однако при SPG19 проявляется еще в начале болезни. Сложные формы заболевания сопровождаются рядом дополнительной неврологической симптоматики, в первую очередь, когнитивным снижением от легкой олигофрении до выраженной деменции. Возможна эпилепсия, оптическая нейропатия, врожденная ретинопатия, дизартрия, мозжечковый синдром, экстрапирамидные расстройства, тугоухость, псевдобульбарный синдром.
Диагностика болезни Штрюмпеля
Решающее диагностическое значение имеет наличие в качестве базового симптома нижней центральной параплегии и ее семейный характер. При спорадических и осложненных формах неврологу приходится проводить дифдиагностику с БАС, опухолью спинного мозга, спинальным вариантом рассеянного склероза, сосудистой миелопатией, нейросифилисом. С целью дифференцировки параплегии Штрюмпеля от лейкодистрофий проводится МРТ головного мозга. В ряде случаев она выявляет атрофические изменения коры мозга. МРТ позвоночника визуализирует дегенеративно-атрофические процессы в боковых и передних столбах на уровне грудных и/или поясничных сегментов спинного мозга.
Вспомогательным методом в диагностике болезни Штрюмпеля выступает электронейромиография (ЭНМГ) и исследование вызванных потенциалов. ЭНМГ позволяет определить наличие и степень нейропатии. Исследование соматосенсорных ВП демонстрирует задержку проведения по задним спинномозговым столбам, исследование корковых ВП — уменьшение скорости проведения по корково-спинальному пути. Важное диагностическое значение имеет генеалогический анализ и молекулярно-генетические исследования. По причине большой гетерогенности патологии последние проводятся только для наиболее встречающихся типов болезни. Возможна пренатальная диагностика.
Лечение и прогноз болезни Штрюмпеля
Основу терапии составляют миорелаксанты (баклофен, толперизон) и транквилизаторы (тазепам, диазепам), которые также оказывают расслабляющий мышцы эффект. Лечение стартует с минимальной дозировки препарата, которая постепенно увеличивается. При достижении эффекта в виде существенного ослабления спастики, дозу препарата прекращают наращивать. При возникновении побочных эффектов останавливают увеличение дозы, если это не помогает — производят ее постепенное снижение. Резкая отмена препарата опасна синдромом отмены, т. е. быстрым нарастанием спастики до степени, превышающей первоначальные проявления. В случаях, когда пероральный прием не дает желаемого эффекта, препараты вводят внутримышечно. Возможно эндолюмбальное локальное введение. При грубой спастике прибегают к установке помпы для постоянной интратекальной инфузии баклофена. Указанное лечение является симптоматическим, оно не позволяет полностью излечить болезнь Штрюмпеля, а лишь дает возможность уменьшить скованность в ногах и, таким образом, улучшить их подвижность.
Альтернативным методом уменьшения спастики является введение ботулотоксина в задние мышцы бедер и икроножные мышцы. Наряду с медикаментозным лечением применяется специальный комплекс ЛФК, физиопроцедуры (парафинолечение, точечный массаж, лечебные ванны). Показана консультация и наблюдение ортопеда, при необходимости — использование ортезов. По показаниям возможно хирургическое ортопедическое лечение возникших контрактур.
Болезнь Штрюмпеля не представляет угрозы для жизни пациента, но снижает его трудоспособность. Скорость прогрессирования и степень выраженности симптоматики весьма варьирует даже среди членов одной семьи. Возникновение заболевания в раннем возрасте обычно характеризуется более злокачественным течением. При неосложненных формах в период пубертата состояние может стабилизироваться; несмотря на значительные трудности при ходьбе, пациенты не теряют способности к самостоятельному передвижению. В других случаях отмечается неуклонное прогрессирование с утратой возможности ходить.
Источник: http://www.krasotaimedicina.ru/diseases/zabolevanija_neurology/hereditary-spastic-paraplegia
Щне
Миастения – это аутоиммунное заболевание, вызывающее слабость мышц из-за нарушения в работе нервно-мышечной передачи. Чаще всего нарушается работа мышц глаз, лицевых и жевательных мышц, иногда – дыхательной мускулатуры. Это определяет характерные для миастении симптомы: опущение нижнего века, гнусавость голоса, нарушения глотания и жевания. Диагноз миастении устанавливается после прозериновой пробы и анализа крови на наличие антител к рецепторам постсинаптической мембраны. Специфическое лечение миастении заключается в назначении антихолинэстеразных препаратов, таких как амбенония хлорид или пиридостигмин. Эти средства восстанавливают нервно-мышечную передачу.
· Причины миастении
· Симптомы миастении
· Диагностика миастении
· Лечение миастении
· Прогноз и профилактика миастении
· Цены на лечение
Миастения
Миастенией (или ложным/астеническим бульбарным параличом, или болезнью Эрба-Гольдфлама) называют заболевание, основным проявлением которого является быстрая (болезненно быстрая) утомляемость мышц. Миастения – это абсолютно классическое аутоиммунное заболевание, при котором клетки иммунной системы, по той или иной причине уничтожают другие клетки собственного же организма. Такое явление можно считать обычной реакцией иммунитета, только направлена она не на чужеродные клетки, а на свои.
Патологическая утомляемость мышц была описана клиницистами в середине XVI века. С тех пор заболеваемость миастенией стремительно растет и выявляется у 6-7 человек на каждые 100 тыс. населения. Женщины болеют миастенией в три раза чаще мужчин. Самое большое количество случаев развития заболевания наблюдается у людей в возрасте от 20 до 40 лет, хотя болезнь может развиться в любом возрасте или быть врожденной.
Причины миастении
Врожденная миастения является следствием генной мутации, из-за которой нервно-мышечные синапсы не могут нормально функционировать (такие синапсы – это что-то вроде "переходников", которые позволяют нерву взаимодействовать с мышцей). Приобретенная миастения встречается чаще врожденной, но легче поддается лечению. Существует несколько факторов, которые при определенных условиях могут стать причиной развития миастении. Наиболее часто патологическая мышечная утомляемость формируется на фоне опухолей и доброкачественной гиперплазии (разрастания тканей) вилочковой железы - тимомегалии. Реже причиной возникновения болезни становятся другие аутоиммунные патологии, например – дерматомиозит или склеродермия.
Описано достаточно случаев выявления миастенической слабости мышц у больных с онкологическими заболеваниями, например, с опухолями половых органов (яичников, предстательной железы), реже - легких, печени и др.
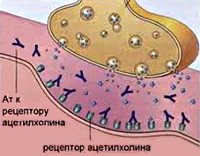
Как уже упоминалось, миастения – это заболевание аутоиммунной природы. Механизм развития болезни основан на выработке организмом антител к белкам-рецепторам, которые находятся на постсинаптической мембране синапсов, осуществляющих нервно-мышечную передачу.
Схематически это можно описать так: отросток нейрона имеет проницаемую мембрану, через которую могут проникать специфические вещества – медиаторы. Они нужны для передачи импульса от нервной клетки к мышечной, на которой есть рецепторы. Последние на мышечных клетках теряют способность связывать медиатор ацетилхолин, нервно-мышечная передача значительно затрудняется. Именно это и происходит при миастении: антитела разрушают рецепторы на "второй стороне" контакта между нервом и мышцей.
Симптомы миастении
Миастению называют "ложным бульбарным параличом" из-за того, что симптомы этих двух патологий действительно похожи. Бульбарный паралич – это повреждение ядер трех черепно-мозговых нервов: языкоглоточного, блуждающего и подъязычного. Все эти ядра располагаются в продолговатом мозге и их поражение крайне опасно. Как при бульбарном параличе, так и при миастении, возникает слабость жевательных, глоточных и лицевых мышц. В итоге это приводит к самому грозному проявлению - дисфагии, то есть нарушению глотания. Патологический процесс при миастении, как правило, первыми затрагивает мышцы лица и глаз, затем – губ, глотки и языка. При длительном прогрессировании заболевания развивается слабость дыхательных мышц и мышц шеи. В зависимости от того, какие группы мышечных волокон поражены, симптомы могут комбинироваться в разных вариантах. Есть и универсальные признаки миастении: изменение выраженности симптомов в течение дня; ухудшение состояния после длительного напряжения мышц.
При глазной форме миастении болезнь затрагивает только глазодвигательные мышцы, круговую мышцу глаза, мышцу, поднимающую верхнее веко. Как следствие, основными проявлениями будут: двоение в глазах, косоглазие, сложность в фокусировке взгляда; невозможность долго смотреть на объекты, расположенные очень далеко или очень близко. Кроме этого, почти всегда присутствует очень характерный симптом – птоз или опущение верхнего века. Особенность этого симптома при миастении заключается в том, что он появляется или усиливается к вечеру. Утром же его может не быть вовсе.
Патологическая утомляемость лицевой, жевательной мускулатуры и мышц, ответственных за речь, приводит к изменению голоса, трудностям с приемом пищи и речью. Голос у больных миастенией становится глухим, "носовым" (такая речь звучит примерно так же, как если бы человек просто говорил, зажав нос). При этом говорить очень тяжело: короткий разговор может настолько утомить больного, что ему необходимо будет несколько часов на восстановление. То же самое касается и слабости жевательных мышц. Жевание твердой пищи может оказаться для человека с миастенией физически непосильной задачей. Больные всегда стараются четко планировать время еды, чтобы принимать пищу в момент максимального действия принимаемых лекарств. Даже в периоды относительного улучшения самочувствия, больные предпочитают есть в первой половине дня, поскольку к вечеру симптомы усиливаются.
Поражение мышц глотки – более
