Апноэ сна у взрослых и детей
СИНДРОМ ОБСТРУКТИВНОГО
АПНОЭ СНА У ВЗРОСЛЫХ И ДЕТЕЙ
Практическое руководство для врачей
Москва
В учебном пособии изложены современные взгляды на этиологию, патогенез, клиническую картину, сердечно-сосудистые, метаболические и неврологические осложнения синдрома обструктивного апноэ сна (СОАС). Дана характеристика основных методов диагностики СОАС в соответствии с международной классификацией. Значительное внимание уделено выбору оптимальной тактики лечения в зависимости от сочетания причин и тяжести заболевания. Приведены общепрофилактические, фармакологические, ортодонтические и хирургические методы лечения. Подробно описан наиболее эффективный метод лечения СОАС средне-тяжелой степени – неинвазивная вспомогательная вентиляция легких постоянным положительным давлением во время ночного сна (СРАР-терапия). Пособие рассчитано на терапевтов, кардиологов, пульмонологов, неврологов, оториноларингологов, эндокринологов, реаниматологов и других врачей, интересующихся проблемами нарушений дыхания во сне.
Авторы – составители:
Бузунов Роман Вячеславович –
Научный руководитель по терапии,
заведующий отделением медицины сна
ФГБУ «Клинический санаторий «Барвиха»
Управления делами Президента РФ,
Заслуженный врач РФ, профессор, д.м.н.
www.buzunov.ru, [email protected]
Легейда Ирина Витальевна –
врач отделения медицины сна
ФГБУ «Клинический санаторий «Барвиха».
Царева Елена Вячеславовна –
врач отделения медицины сна
ФГБУ «Клинический санаторий «Барвиха».
Для контактов:
Московская обл., Одинцовский р-н, санаторий «Барвиха»
(495) 635-69-07, (495) 635-69-08, www.sleepnet.ru
Оглавление
Список сокращений 4
ВВЕДЕНИЕ 5
ОПРЕДЕЛЕНИЕ И КЛАССИФИКАЦИЯ 6
Список литературы 7
ЭПИДЕМИОЛОГИЯ 8
Список литературы 9
ЭТИОЛОГИЯ 11
Список литературы 17
ПАТОГЕНЕЗ 18
Артериальная гипертония 20
Нарушения ритма и проводимости сердца 21
Ишемическая болезнь сердца 23
Атеросклероз 24
Сердечно-сосудистая смертность 25
Метаболические, гормональные и эндокринные расстройства 27
Неврологические и когнитивные осложнения 28
Социально-экономические аспекты СОАС 28
Список литературы 30
КЛИНИЧЕСКАЯ КАРТИНА 35
Список литературы 39
ДИАГНОСТИКА 40
Клиническая диагностика 40
Инструментальная диагностика 41
Тип 1 – Стационарная полисомнографическая система 43
Тип 2 – Мобильная полисомнографическая система 48
Тип 3 - Системы с ограниченным набором параметров 49
Тип 4 – Скрининговые системы 51
Другие типы диагностических систем 57
Диагностика синдрома обструктивного апноэ сна у детей 59
Организационные основы диагностики синдрома обструктивного апноэ сна 59
Дифференциальная диагностика 65
Формулировка клинического диагноза 66
Список литературы 67
ЛЕЧЕНИЕ 69
Лечение храпа и апноэ сна у взрослых 69
Общепрофилактические мероприятия 69
Облегчение носового дыхания 71
Применение снотворных и транквилизаторов при СОАС 73
Применение внутриротовых приспособлений 74
Применение электромеханических подбуживающих устройств 77
Применение фармакологических средств, облегчающих храп 77
Оперативное лечение храпа и СОАС 80
Неинвазивная вспомогательная вентиляция легких постоянным положительным давлением (СРАР-терапия) 90
Лечение храпа и СОАС у детей 100
Заключение 109
Список литературы 109
Список сокращений
АД – артериальное давление
ДТП - дорожно-транспортные происшествия
ИБС – ишемическая болезнь сердца
ИД – индекс десатураций
ИМТ - индекс массы тела
МКП - мониторинговая компьютерная пульсоксиметрия
СОАС – синдром обструктивного апноэ сна
ИАГ – индекс апноэ/гипопноэ
ЛУПП - лазерной увулопалатопластики
ОФД - отделение функциональной диагностики
ПЦПР - прогностическая ценность положительного результата
ПСГ – полисомнография
ЭЭГ – Электроэнцефалограмма
ЭОГ - Электроокулограмма (движения глаз)
ЭМГ - Электромиограмма (тонус подбородочных мышц)
ЭКГ - Электрокардиограмма
Auto-CPAP – СРАР - аппарат с автоматической настройкой лечебного давления в реальном времени
СРАР-терапия - лечение методом создания постоянного положительного давления в дыхательных путях
NYHA - New York Heart Association
РАТ - Peripheral Arterial Tone
RDI/h -индекс дыхательных расстройств
REM – Rapid Eye Movies
SpO2 – Сатурация
ВВЕДЕНИЕ
Около 30% всего взрослого населения постоянно храпит во сне. Храп не только создает очевидные социальные проблемы, но и является предвестником и одним из основных симптомов синдрома обструктивного апноэ сна (СОАС), проявляющегося остановками дыхания во сне с последующими громкими всхрапываниями. При СОАС тяжелой степени может отмечаться до 400-500 остановок дыхания за ночь продолжительностью до минуты и более (суммарно до 3-4 часов!), что ведет к острому и хроническому недостатку кислорода во время сна. Это в свою очередь существенно увеличивает риск развития артериальной гипертонии, нарушений ритма сердца, инфаркта миокарда, инсульта и внезапной смерти во сне.
Каждая остановка дыхания сопровождается частичным или полным пробуждением мозга, что приводит к резкому ухудшению качества сна. У пациента отмечаются частые пробуждения с ощущением удушья и сердцебиения, беспокойный и неосвежающий сон. Утром беспокоит разбитость и головная боль. В течение дня отмечается тяжелая сонливость, раздражительность, сниженный фон настроения. Особенно опасны приступы острой сонливости во время управления автомобилем, существенно увеличивающие риск дорожно-транспортных происшествий. Ухудшается память и внимание, увеличивается масса тела, развивается импотенция.
Как видно, заболевание проявляется множеством симптомов, по поводу которых больной может обращаться к терапевту, кардиологу, неврологу, оториноларингологу, пульмонологу, эндокринологу и даже сексопатологу и психиатру. Особую важность данное заболевание приобретает у пожилых пациентов. Во-первых, в связи с высокой распространенностью СОАС у данной категории лиц. Во-вторых, из-за частых ошибок в его диагностике, когда симптомы СОАС интерпретируются как проявления церебрального атеросклероза, деменции и ряда других заболеваний. Более того, в пожилом возрасте наличие СОАС значительно утяжеляет течение ИБС, артериальной гипертонии и хронической обструктивной болезни легких. Еще одной важной проблемой является ошибочное назначение бензодиазепиновых транквилизаторов у пожилых, которые противопоказаны при СОАС и могут провоцировать гипертонические кризы, инсульты, и внезапную смерть во сне.
Нарушения дыхания во сне актуальны и в педиатрической практике. Храп отмечается у 10-14% детей в возрасте 2-6 лет, СОАС – у 1-3%. Апноэ сна тяжелой степени у детей имеет драматические последствия: выраженный синдром дефицита внимания и гиперактивности, отставание в физическом и психическом развитии.
К сожалению, отечественные врачи еще недостаточно информированы о влиянии СОАС на здоровье человека и не уделяют его диагностике должного внимания. При этом сами пациенты не жалуются на остановки дыхания во сне, а храп считают недостойным внимания врача симптомом и не предъявляют соответствующих жалоб. В этой ситуации даже выраженный СОАС часто остается недиагностированным и нелеченным, что значительно ухудшает качество и прогноз жизни больных.
Постановка точного диагноза важна и потому, что в настоящее время существуют эффективные методы лечения СОАС, в частности применение неинвазивной вспомогательной вентиляции легких постоянным положительным давлением во время сна (СРАР-терапия). Данный метод позволяет даже при очень выраженном СОАС значительно улучшить качество жизни человека и предотвратить серьезные осложнения.
ОПРЕДЕЛЕНИЕ И КЛАССИФИКАЦИЯ
Синдром обструктивного апноэ сна (СОАС) - это состояние, характеризующееся наличием храпа, периодическим спадением верхних дыхательных путей на уровне глотки и прекращением легочной вентиляции при сохраняющихся дыхательных усилиях, снижением уровня кислорода крови, грубой фрагментацией сна и избыточной дневной сонливостью [1].
Из определения видно, что в основе болезни лежит периодическое прекращение дыхания из-за спадения стенок дыхательных путей на уровне глотки. Дыхательные пути могут спадаться полностью, и тогда развивается апноэ - прекращение воздушного потока (легочной вентиляции) длительностью 10 секунд и более. При неполном спадении дыхательных путей отмечается гипопноэ - существенное снижение воздушного потока (более 50% от исходных значений), сопровождающееся снижением насыщения гемоглобина артериальной крови кислородом (сатурации) на 3% и более [2].
Апноэ и гипопноэ могут быть обструктивными и центральными. При обструктивном апноэ сна отмечается коллапс дыхательных путей при продолжающихся дыхательных усилиях (функция дыхательного центра сохранена). При центральном апноэ сна (дыхание Чейна-Стокса и другие формы) отмечается снижение функции или остановка дыхательного центра и прекращение дыхательных усилий. При этом дыхательные пути остаются открытыми. Предметом данного пособия является обструктивное апноэ сна, которое в терапевтической практике встречается существенно чаще, чем различные формы центрального апноэ.
Общепризнанным критерием степени тяжести СОАС является частота апноэ и гипопноэ в час – индекс апноэ/гипопноэ (ИАГ). Считается нецелесообразным подсчитывать отдельно количество апноэ и гипопноэ, так как они несут схожие риски в отношении развития сердечно-сосудистых и иных осложнений. В настоящее время большинство международных консенсусов и клинических рекомендаций [3-5] придерживаются классификации, приведенной в таблице 1.
Таблица 1.
Классификация тяжести СОАС у взрослых на основании ИАГ[5].
| Тяжесть СОАС | ИАГ |
| Легкая степень | от >5 до <15 |
| Средняя (Умеренная) степень | от >15 и <30 |
| Тяжелая степень | >30 |
Применение именно этих пограничных значений в классификации степени тяжести СОАС основывается на результатах крупных проспективных контролируемых исследований, которые показали достоверное увеличение частоты сердечно-сосудистых осложнений при ИАГ >15 в 2-3 раза и при ИАГ >30 в 5-6 раз [6-8]. Мы также применяем эту классификацию в своей практической деятельности.
Дополнительными критериями оценки тяжести СОАС могут служить показатели снижения насыщения крови кислородом (десатурация) на фоне эпизодов апноэ/гипопноэ; степень нарушения структуры ночного сна; сердечно-сосудистые осложнения, связанные с нарушениями дыхания (ишемия миокарда, нарушения ритма и проводимости, артериальная гипертония), выраженность когнитивного дефицита.
У детей следует ориентироваться на классификацию, представленную в таблице 2.
Таблица 2.
Классификация тяжести СОАС у детей на основании ИАГ [9].
| Тяжесть СОАС | ИАГ |
| Легкая степень | от >1 до <5 |
| Средняя (Умеренная) степень | от >5 и <15 |
| Тяжелая степень | >15 |
В педиатрической практике дополнительными критериями степени тяжести состояния являются выраженность синдрома дефицита внимания и гиперактивности, а также степень задержки физического и психического развития.
Список литературы
1. Guilleminault, C; Demen, WC. Sleep apnoea syndromes. New York : Alan R. Liss Inc., 1978.
2. Sleep-related breathing disorders in adults: recommendations for syndrome definition and measurement techniques in clinical research. The Report of an American Academy of Sleep Medicine Task Force. Sleep, 1999, 22- pp. 667–689.
3. Management of obstructive sleep apnoea/hypopnoea syndrome in adults. A national clinical guideline [article online], 2003.- URL: http://www.sign.ac.uk/uidelines/ fulltext/73/index.html.
4. NICE technology appraisal guidance 139, march 2008. Continuous positive airway pressure for the treatment of obstructive sleep apnoea/hypopnoea syndrome, Diagnosis and treatment of obstructive sleep apnea in adults,Institute for Clinical Systems Improveme. Bloomington (MN): Institute for Clinical Systems Improvement (ICSI), 2008.
5. Punjabi, NM; Newman, A; Young, T; Resnick, HE; Sanders, M. Sleep disordered breathing and cardiovascular disease: an outcome-based definition of hypopneas. Am J Respir Crit Care Med, 2008, 177(10)-pp. 1150-1155.
6. Marin, JM; Carrizo, SJ; Vicente, E; Agusti, AG. Long-term cardiovascular outcomes in men with obstructive sleep apnoea-hypopnoea with or without treatment with continuous positive airway pressure: an observational study. Lancet, 2005, 365-pp.1046-1053.
7. Marshall, NS; Wong, KKH; Liu, PY; Cullen, SRJ; Knuiman, MW; Grunstein, RR. Sleep Apnea as an Independent Risk Factor for All-Cause Mortality: The Busselton Health Study. Sleep, 2008, 31(8)- pp. 1079–1085.
8. Young, T; Finn, L; Peppard, PE; Szklo-Coxe, M; Austin, D; et al. Sleep Disordered Breathing and Mortality: Eighteen-Year Follow-up of the Wisconsin Sleep Cohort . Sleep, 2009, 31(8)-pp. 1071-1078.
9. Gozal, D; Kheirandish-Gozal, L. New approaches to the diagnosis of sleep-disordered breathing in children . Sleep Medicine, 2010, 11 (7) -pp. 708-713.
ЭПИДЕМИОЛОГИЯ
Распространенность СОАС составляет 5-7% от всего населения старше 30 лет. СОАС тяжелой степени страдают около 1-2% из указанной группы лиц [1-3]. Данные показатели превышают распространенность бронхиальной астмы [4]. Наши данные по распространенности СОАС у пациентов санатория приведены на рисунке 1.

Рис.1.Частота выявления и тяжесть СОАС у первичных пациентов Клинического санатория «Барвиха» (2006-2008 гг.).
У лиц старше 60 лет частота СОАС значительно возрастает и составляет около 30% у мужчин и около 20% у женщин [5]. У лиц старше 65 лет частота заболевания может достигать 60% [6]. Распространенность храпа у детей в возрасте 2-6 лет составляет порядка 10-14% [7], апноэ сна – 1-3% [8].
Распространенность клинически значимых нарушений дыхания во сне достигает 15% у пациентов терапевтического профиля в стационаре [9-11]. У кардиологических больных распространенность СОАС еще выше. У пациентов с системной артериальной гипертензией этот показатель составляет 30% [12], а при рефрактерных формах гипертонической болезни достигает 83% [13]. У больных с ночными брадиаритмиями обструктивное апноэ сна выявляется в 68% случаев [14]. При ИБС и сердечной недостаточности II-IV функционального класса по классификации NYHA распространенность СОАС достигает 43% [15]. Таким образом, пациенты с кардиологической патологией находятся в группе риска по наличию нарушений дыхания во сне и требуют пристального внимания и более тщательного обследования с целью выявления СОАС.
Нами было проведено исследование распространенности апноэ сна у пациентов кардиологического стационара. Протокол исследования предполагал сплошное проведение мониторинговой компьютерной пульсоксиметрии (МКП) во время ночного сна у всех пациентов, поступивших в стационарное кардиологическое отделение ФГБУ «ЦКБ с поликлиникой» Управления делами Президента РФ в течение двух месяцев. В анализ было включено 125 человек, что составило 89,9% от всех пациентов, поступивших в отделение за изучаемый период. У 72% пациентов выявлен индекс десатураций > 5, что указывало на вероятность наличия у них апноэ сна обструктивного или центрального генеза. Из них у 36% пациентов индекс десатураций был > 15, что соответствовало апноэ сна средней и тяжелой степени. И только у 28% пациентов не было патологических изменений на кривой ночной сатурации. Таким образом, больше трети обследованных пациентов кардиологического профиля имеют высокую вероятность наличия клинически значимых апноэ сна средне-тяжелой степени различного генеза, что подтверждается работами зарубежных авторов [12,13,15-17].
Распространенность СОАС также высока при ожирении [18], метаболическом синдроме [19], сахарном диабете [20], гипотиреозе [21].
Список литературы
1. Lindberg, E; Elmasry, A; Gislason, T; et al. Evolution of sleep apnea syndrome in sleepy snorers: a population-based prospective study. Am J Respir Crit Care Med, 1999, 159- pp.6024-6027.
2. Marin, JM; Gascon, JM; Carrizo, S; Gispert, J. Prevalence of sleep apnoea syndrome in the Spanish adult population. Int J Epidemiol, 1997, 26- pp. 381-386.
3. Stradling, JR; Crosby, JH. Predictors and prevalence of obstructive sleep apnoea and snoring in 1,001 middle aged men. Thorax, 1991, 46- pp. 85-90.
4. Young, T; Palta, M; Dempsey, J; at al. The occurrence of sleep-disordered breathing among middle-aged adults. N Engl J Med, 1993, 328- pp. 1230-1235.
5. Lindberg, E. Epidemiology of OSA. Eur Respir Mon, 2010, 50 - pp. 51-68.
6. Ancoli-Israel, S; Kripke, DF; Klauber, MR; Mason, WJ; Fell, R; Kaplan, O. Sleep-disordered breathing in community-dwelling elderly. Sleep, 1991, 14(6)- pp.486-495.
7. Young, T; Peppard, PE; Gottlieb, DJ. Epidemiology of obstructive sleep apnea: A Population Health Perspective. Am J Resp Crit Care Med, 2002, 165(9)-pp.1217-1239.
8. Sohn, H; Rosenfeld, RM. Evaluation of sleep-disordered breathing in children. Otolaryngol Head Neck Surg, 2003, 128(3) - pp.344-352.
9. Jennum, P; Soul, A. Epidemiology of snoring and obstructive sleep apnoea in the Dannish population age 30-60. J Sleep Res, 1992, 1- pp. 240-244.
10. Lavie, P; Ben-Yosef, R; Rubin, AE. Prevalence of sleep apnea syndrome among patients with essential hypertension. Am Heart J,1984, 108- pp. 373-376.
11. Lindberg, E; Gislason, T. Epidemiology of sleep-related obstructive breathing. Sleep Med Rev, 2000, 4- pp. 411–433.
12. Schulz, R; Grebe, M; Eisele, HJ; Mayer, K; Weissmann, N; Seeger, W. Obstructive sleep apnea-related cardiovascular disease. Med Klin (Munich), 2000, 101(4) - pp.321-327.
13. Logan, AG; Perlikowski, SM; Mente, A; et al. High prevalence of unrecognized sleep apnoea in drug-resistant hypertensions. J Hypertens, 2001, 19 - pp.2271—2277.
14. Курлыкина, Н.В.; Певзнер,А.В.; Литвин, А.Ю.; Галицин, П.В.; Чазова, И.Е.; Соколов, С.Ф.; Голицын, С.П. Возможности лечения больных с длительными ночными асистолиями и синдром обструктивного апноэ сна созданием постоянного положительного давления воздуха в верхних дыхательных путях.// Кардиология.- 2009.- 6 (49). - С.36-42.
15. Schulz, R; Blau, A; Borgel, J. Sleep apnoea in heart failure. Eur Respir J, 2007, 29 - pp.1201–1205.
16. Marin, JM; Carrizo, SJ; Vicente, E; Agusti, A.G. Long-term cardiovascular outcomes in men with obstructive sleep apnoea-hypopnoea with or without treatment with continuous positive airway pressure: an observational study. Lancet, 2005, 365 - pp.1046-1053.
17. Bitter, T; Langer, C; Vogt, J; Lange, M; Horstkotte, D; Oldenburg, O. Sleep-disordered breathing in patients with atrial fibrillation and normal systolic left ventricular function. Dtsch Arztebl Int, 2009, 106(10) - pp.164-170.
18. Bahammam, A; Kryger, M. Decision making in obstructive sleep disordered breathing. Putting It Al Together. Otolaryngologic Clinics of North America, 1999, 32- pp. 333-348.
19. Wilcox, I; McNamara, SG; et al. Syndrome Z: the interaction of sleep apnea, vascular risk factors and heart disease. Thorax, 1998, 53(3) -pp.5-28.
20. Katsumata, K; Okada, T; Miyao, M; Katsumata, Y. High incidence of sleep apnea syndrome in a male diabetic population. Diabetes Res Clin Pract, 1991, 13 – pp.45–51.
21. . Lin, C-C; Tsan, K-W; Chen, P-J. The relationship between sleep apnea syndrome and hypothyroidism. Chest, 1992, 102 - pp.1663–1667.
ЭТИОЛОГИЯ
Во сне закономерно снижается общий мышечный тонус, в частности расслабляются подвижные структуры на уровне глотки. Если имеются предрасполагающие факторы, приводящие к сужению глотки, то может возникнуть храп, обусловленный биением мягкого неба о стенки дыхательных путей. Дальнейшее сужение просвета дыхательных путей может приводить к полному их спадению и развитию эпизода обструктивного апноэ.
Величина просвета верхних дыхательных путей на уровне глотки зависит от исходного внутреннего диаметра, степени снижения давления в просвете во время вдоха и тонуса глоточных мышц во время сна. На рис.1 представлены причины развития патологического сужения и спадения дыхательных путей во время сна.

Рис.1. Причины и механизм обструкции дыхательных путей во сне.
Наиболее частой причиной сужения просвета дыхательных путей на уровне глотки у взрослых является ожирение (рис.2). У пациентов с индексом массы тела (ИМТ), превышающим 29 кг/м2 (ожирение 1 степени и выше), вероятность наличия СОАС в 8-12 раз выше, чем у пациентов без ожирения [1]. У пациентов с ожирением 3 степени (ИМТ>40) тяжелая степень СОАС отмечается более чем в 60% случаев [2].









А Б
Рис.2. Сагиттальный и поперечный срез головы в норме (А) и у пациента с ожирением и тяжелой формой СОАС (Б). Отложения жира отображаются белым цветом. Магнитно-резонансная томография [3].
На рис 2Б на сагиттальном срезе отмечается значительное сужение просвета глотки на уровне мягкого неба, корня языка и надгортанника (отмечено стрелками); на поперечном срезе видны значительные отложения висцерального жира рядом с латеральными стенками глотки (отмечено стрелками).
При осмотре у пациентов с ожирением отмечается существенное сужение просвета глотки как за счет отложения жира в самих ее структурах (мягкое небо, небный язычок, боковые дужки), так и сдавления глотки висцеральным жиром преимущественно в области латеральных стенок (рис.3).


А Б
Рис.3. Просвет глотки при визуальном осмотре в норме (А) и при ожирении (Б) (собственные данные).
Увеличение небных миндалин также может приводить к значительному сужению просвета дыхательных путей на уровне глотки и их спадению во время сна (рис.4).



Рис. 4. Гипертрофия небных миндалин 3-й степени (собственные данные).
 |
 Основными причинами формирования СОАС у детей являются адено-тонзиллярная гипертрофия, деформации лицевого скелета и ожирение. Важную роль играет аллергический ринит, который рассматривается как самостоятельный фактор риска СОАС у детей [4]. При данном заболевании часто отмечается хроническая носовая обструкция и аденоиды аллергического или воспалительного генеза. Это обуславливает постоянное дыхание через рот. Впоследствии развивается вторичная гипертрофия небных миндалин [5-7]. Длительно сохраняющееся ротовое дыхание приводит к формированию у ребенка вытянутого по вертикали лица, маленькой и смещенной назад нижней челюсти (микро- и ретрогнатия), «скученности» зубов, увеличенного с горбинкой носа. Данный характерный вид получил название «птичьего» лица (рис.5).
Основными причинами формирования СОАС у детей являются адено-тонзиллярная гипертрофия, деформации лицевого скелета и ожирение. Важную роль играет аллергический ринит, который рассматривается как самостоятельный фактор риска СОАС у детей [4]. При данном заболевании часто отмечается хроническая носовая обструкция и аденоиды аллергического или воспалительного генеза. Это обуславливает постоянное дыхание через рот. Впоследствии развивается вторичная гипертрофия небных миндалин [5-7]. Длительно сохраняющееся ротовое дыхание приводит к формированию у ребенка вытянутого по вертикали лица, маленькой и смещенной назад нижней челюсти (микро- и ретрогнатия), «скученности» зубов, увеличенного с горбинкой носа. Данный характерный вид получил название «птичьего» лица (рис.5).  |
Рис.5. Пациентка К., 11 лет. Тяжелая степень СОАС (ИАГ 60 в час) (собственные данные).
У пациентки имеется носовая обструкция, обусловленная аденоидами, гипертрофия небных миндалин 3-й степени, «птичье» лицо: выраженная ретро- и микрогнатия, «скученность» зубов, нос с горбинкой.
Если ребенка с хронической носовой обструкцией активно не лечить с самого начала болезни, то сформированные к 10-12 годам дефекты развития лицевого скелета сами по себе будут являться факторами риска развития храпа и СОАС. И даже удаление аденоидов и увеличенных небных миндалин в этом возрасте не всегда даст четкий положительный эффект. У этих пациентов к 25-30 годам может развиваться СОАС умеренной и тяжелой степени даже без существенного набора массы тела (рис.6).




 |
Рис.6. Пациент С., 34 года. Тяжелая степень СОАС (ИАГ-54 в час), ИМТ -28 (собственные данные).
Пациент с характерным «птичьим» лицом. В анамнезе с детства практически не леченная хроническая носовая обструкция на фоне аллергического ринита, аденоидов и хронического тонзиллита. Аденэктомия не производилась. Тонзиллэктомия в возрасте 18 лет в армии. В 30 лет безуспешное оперативное лечение храпа методом лазерной увулопалатопластики (удаленный небный язычок, рубцовые изменения небных дужек).
Предрасположенность к развитию СОАС у пациентов с гипотиреозом обусловлена набором массы тела, глобальным снижением мышечного тонуса и отеком висцеральных тканей при снижении функции щитовидной железы [8,9]. При акромегалии у взрослых отмечается непропорциональный рост отдельных органов и, в частности, языка. Это, в свою очередь, обуславливает сужение просвета глотки на уровне корня языка и увеличивает риск развития СОАС [10].
Нервно-мышечные дистрофические процессы (старение, нейромышечные заболевания, боковой амиотрофический склероз) обуславливают нарушение работы мышц, в частности, отвечающих за поддержание просвета дыхательных путей в открытом состоянии во сне. Это увеличивает риск спадения стенок глотки и развития СОАС. Алкоголь обладает миорелаксирующим действием и тормозит активность головного мозга, что способствует возникновению храпа и СОАС [11,12]. Курение также оказывает разноплановое отрицательное воздействие на верхние дыхательные пути, что провоцирует нарушения дыхания во сне.
Следует учитывать, что у одного пациента может сочетаться 2-3-4 различных этиологических фактора СОАС. Это важно учитывать с точки зрения выбора комплексной тактики лечения пациента.
Список литературы
1. Deegan, PC; McNicholas, WT. Predictive value of clinical features for the obstructive sleep apnoea syndrome. Eur Respir J, 1996, 9- pp.117-124.
2. Бузунов, Р.В.; Ерошина, В. А. Зависимость тяжести синдрома обструктивного апноэ во время сна от увеличения массы тела после возникновения у пациентов симптома храпа //Терапевтический архив.- 2004.- №3.- С. 59-62.
3. Schwab, RJ. Airway imaging. Clinics in Chest Medicine, 1998 , 19- pp. 33-54.
4. Anuntaseree, W; Rookkapan, K; Kuasirikul, S; Thongsuksai,P. Snoring and obstructive sleep apnea in Thai school-age children: prevalence and predisposing factors. Pediatric Pulmonology, 2001, 32-pp.222-227.
5. Abreu, RR; Rocha, RL; Lamonier, JA; Guerra, AF. Etiology, clinical manifestations and concurrent findings in mouth-breathing children. JPediatr (Rio J), 2008, 84-pp. 529-535.
6. Modrzynski, M; Zawisza, E. An analysis of the incidence of adenoid hypertrophy in allergic children. Int J Pediatr Otorhinolaryngol, 2007, 71(5)-pp.713-719.
7. Berardino, FD. Adenoidal hypertrophy and allergic rhinitis. Pediatric Allergy and Immunology, 2011, 22(6) - p. 646.
8. Grunstein, RR; Sullivan, CE. Sleep apnea and hypothyroidism: mechanisms and management. Am J Med, 1988, 85 - pp.775–779.
9. Lin, C-C; Tsan, K-W; Chen, P-J. The relationship between sleep apnea syndrome and hypothyroidism. Chest. 1992, 102 - pp.1663–1667.
10. Blanco Pérez, JJ; Blanco-Ramos, MA; Zamarrón Sanz, C; Souto Fernández, A; Mato Mato, A; Lamela López, J. Acromegaly and sleep apnea. Arch Bronconeumol, 2004, 40(8) - pp.355-359.
11. Peppard, PE; Austin, D; Brown, RL. Association of alcohol consumption and sleep disordered breathing in men and women. J Clin Sleep Med, 2007 , 3(3) - pp.265-270.
12. 12. Tanigawa, T; Tachibana, N; Yamagishi, K; Muraki, I; Umesawa,M; Shimamoto, T; Iso, H . Usual Alcohol Consumption and Arterial Oxygen Desaturation During Sleep. JAMA, 2004, 292(8) - pp.923-925.
ПАТОГЕНЕЗ
Реализация механизма обструкции дыхательных путей во сне на уровне глотки происходит следующим образом. Человек засыпает. Происходит постепенное расслабление мышц мягкого неба и стенок глотки. Данные структуры начинают вибрировать при прохождении струи воздуха и создавать звуковой феномен храпа. Дальнейшее углубление сна и снижение мышечного тонуса приводит в определенный момент к полному спадению глотки и развитию острого эпизода удушья.
Зона, в которой наступает нарушение проходимости верхних дыхательных путей во время сна, может находиться на уровне мягкого неба, корня языка или надгортанника, то есть в нижней части носоглотки и ротоглотке (рис.1).

Рис.1. Локализация обструкции верхних дыхательных путей во время сна.
При этом дыхательные усилия сохраняются и даже усиливаются в ответ на развивающуюся гипоксемию. Острый недостаток кислорода в артериальной крови приводит к стрессовой реакции, сопровождающейся активацией симпатоадреналовой системы и подъемом АД. В конце концов, негативная информация от различных органов и систем вызывает частичное пробуждение мозга (микроактивацию). Мозг, в свою очередь, восстанавливает контроль над глоточной мускулатурой и быстро открывает дыхательные пути. Человек громко всхрапывает, делает несколько глубоких вдохов. В организме восстанавливается нормальное содержание кислорода, мозг успокаивается и засыпает вновь...цикл повторяется. За ночь может отмечаться до 400-500 остановок дыхания до минуты и более. В нашей практике максимальная остановка дыхания у пациента составила 3 минуты 10 секунд. При этом сатурация упала ниже 50% и оставалась в этом диапазоне около полутора минут. Интересно отметить, что, по мнению реаниматологов, снижение сатурации ниже 50% в течение 2 минут приводит к смерти коры мозга.
Частые эпизоды удушья и выраженной гипоксемии обуславливают развитие сердечно-сосудистых, метаболических, эндокринных, неврологических и психических нарушений. Схематично патогенез СОАС представлен на рис.2. Ниже мы более подробно остановимся на различных аспектах патогенеза СОАС.

Рис.2. Патогенез СОАС.
Артериальная гипертония
В настоящее время доказано, что СОАС является независимым фактором риска артериальной гипертонии [1-4]. У 50% больных СОАС отмечается артериальная гипертония [5]. В то же время у 30% пациентов с артериальной гипертонией имеется СОАС [6,7]. В 7-м отчете Объединенного Национального комитета США по профилактике, диагностике, оценке и лечению повышенного артериального давления (JNC 7) апноэ сна поставлено на первое место среди всех причин вторичных артериальных гипертоний, что говорит о значительной распространенности и клинической значимости артериальной гипертонии, обусловленной СОАС [8]. Следует отметить, что данный отчет был опубликован в 2004 году, но большинство отечественных кардиологов до сих пор не учитывают эту информацию в своей практической работе.
У пациентов с СОАС отмечается отсутствие снижения артериального давления в ночное время («non-dipper») или даже его превышение над дневным давлением («night peaker») [9]. Отмечается также повышение артериального давления (преимущественно диастолического) в утренние часы [10]. Интересной особенностью динамики АД у пациентов с СОАС является его существенное снижение через 20-30 минут после пробуждения без какого-либо медикаментозного вмешательства. По данным Logan и соавт. [11] у 41 пациента с рефрактерной артериальной гипертонией (>140/90 мм рт.ст.), не поддающейся лечению тремя и более препаратами, синдром обструктивного апноэ сна (ИАГ>10) был выявлен в 83% случаев. Таким образом, у пациентов с преимущественно ночной и утренней артериальной гипертонией, особенно рефрактерной к лечению, всегда следует предполагать наличие СОАС.
Ишемическая болезнь сердца
Распространенность нарушений дыхания во сне у пациентов с ИБС составляет около 30%, что в два раза выше, чем у сравнимых пациентов без ИБС [28-30]. Тяжелая интермиттирующая гипоксемия, ацидоз, повышение и нестабильность АД, симпатическая вазоконстрикция в сочетании со скачками внутригрудного давления и трансмурального давления в сердце могут быть провоцирующими факторами развития ишемии миокарда. У пациентов с тяжелой степенью СОАС депрессия сегмента ST в ночное время отмечалась приблизительно в 30% случаев [31]. Пробуждение мозга и вентиляционная фаза после апноэ сопровождается выраженной симпатической активностью и резким ускорением ЧСС. В этот момент значительно возрастает потребность миокарда в кислороде, однако оксигенированная кровь достигает миокарда лишь спустя 10-20 секунд после начала вентиляции в зависимости от скорости системного кровотока. Возникает резкий дисбаланс между быстрым увеличением потребности миокарда в кислороде на фоне тахикардии и его доставкой, что способствует развитию преходящей ишемии миокарда непосредственно после эпизода апноэ (рис.4).
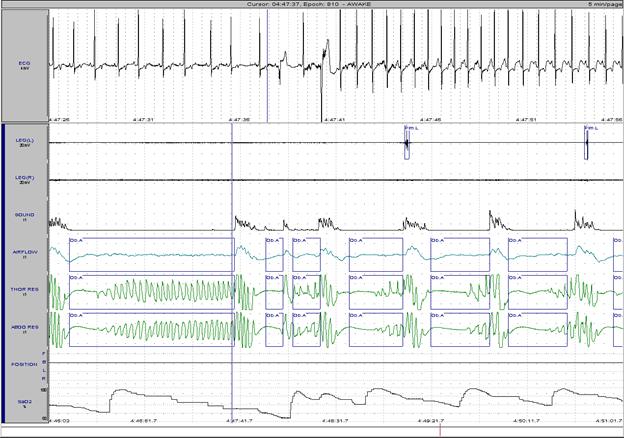
Рис.4. Пациент П., 49 лет. СОАС тяжелой степени. Развитие депрессии сегмента ST в вентиляционную фазу после длительного (85 с) эпизода апноэ с резким снижением сатурации до 65%. В верхнем окне – канал ЭКГ (развертка 30 с на экран). В нижнем окне – дыхательные каналы (развертка 5 мин на экран). Вертикальная черта – синхронизация по времени (собственные данные).
При обследовании больных с исключительно ночной стенокардией СОАС был выявлен у 9 из 10 пациентов, причем лечение CPAP эффективно устраняло ишемию миокарда [32]. Таким образом, у пациентов с ИБС целесообразно исключить СОАС, особенно в случае наличия ночной ишемии, стенокардии и других маркеров заболевания (храп, указания на остановки дыхания во сне, ожирение). Применение СРАР-терапии у пациентов с сочетанием ИБС и СОАС может облегчить течение ИБС и улучшить прогноз.
Атеросклероз
Обструктивные апноэ приводят к циклическим эпизодам гипоксемии. При длительных остановках дыхания во сне сатурация может падать ниже 60% (визуально человек синеет), что свидетельствует о критической тканевой гипоксемии. В фазу гипервентиляции после апноэ сатурация быстро восстанавливается до 95-99%.
При СОАС тяжелой степени циклы гипоксемии и реоксигенации повторяются 40-60 раз в час. Продолжительная симпатическая активность, колебания внутригрудного давления, циклы гипоксемии/реоксигенации, окислительный стресс вызывают эндотелиальную дисфункцию, повреждение сосудистой стенки и, в конечном итоге, способствуют более раннему развитию атеросклероза [33].
Список литературы
1. Davies, CWH; Crosby, JH; Mullins, RL; Barbour, C; Davies, RJO; Stradling, JR. Case-control study of 24 hour ambulatory blood pressure in patients with obstructive sleep apnoea and normal matched control subjects. Thorax, 2000, 55 -pp.736-740.
2. Lavie, P; Herer, P; Hoffstein, V. Obstructive sleep apnoea syndrome as a risk factor for hypertension: population study. BMJ, 2000, 320- pp.479–482.
3. Nieto, FJ; Young, T; Lind, B; Shahar, E; Samet, JM; Redline, S; D'Agostino, RB; Newman, AB; Lebowitz, MD; Pickering, TG. Association of Sleep-disordered breathing, sleep apnea, and hypertension in a large community-based study. JAMA, 2000, 283 -pp.1829-1836.
4. Peppard, PE; Young, T; Palta, M; Skatrud, J. Prospective study of the association between sleep-disordered breathing and hypertension. N Engl J Med, 2000, 342, -pp.1378-1384.
5. Silverberg, DS; Oksenberg, A; Iaina, A. Sleep-related breathing disorders as a major cause of essential hypertension: fact or fiction? Curr Opin Nephrol Hypertens, 1998, 7- pp.353–357.
6. Kales, A; Bixler, EO; Cadieux, RJ; Schneck, DW; Shaw, LC 3rd; Locke, TW; Vela-Bueno, A; Soldatos, CR. Sleep apnoea in a hypertensive population. Lancet, 1984, 2- pp.1005–1008.
7. Lavie, P; Ben-Yosef, R; Rubin, AE. Prevalence of sleep apnea syndrome among patients with essential hypertension. Am Heart J,1984,108- pp.373-376.
8. Chobanian, AV; Bakris, GL; Black, HR; Cushman, WC; Green, LA; Izzo, JL Jr; Jones, DW; Materson, BJ; Oparil, S; Wright, JT Jr; Roccella, EJ. National Heart, Lung, and Blood Institute, Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure; National High Blood Pressure Education Program Coordinating Committee. The Seventh Report of the Joint NationalCommittee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure: the JNC 7 report. JAMA, 2003, 289- pp.2560 –2572.
9. Suzuki, M; Guilleminault, C; Otsuka, K; Shiomi, T. Blood pressure «dipping» and «non-dipping» in obstructive sleep apnea syndrome patients. Sleep, 1996, 19- pp.382–387.
10. Hoffstein, V; Mateika, J. Evening to morning blood pressure variations in snoring patients with and without obstructive sleep apnea. Chest, 1992, 101-pp.379-384.
11. Logan, AG; Perlikowski, SM; Mente, A; Tisler, A; Tkacova, R; Niroumand, M; et al. High prevalence of unrecognized sleep apnoea in drug-resistant hypertension. J Hypertens, 2001, 19- pp.2271-2277.
12. Koehler, U; Schafer, H. Is obstructive sleep apnea (OSA) a risk factor for myocardial infarction and cardiac arrhythmias in patients with coronary heart disease (CHD)? Sleep, 1996, 19-pp. 283–286.
13. Liston, R; Deegan, PC; McCreery, C; McNicholas, WT. Role of respiratory sleep disorders in the pathogenesis of nocturnal angina and arrhythmias. Postgrad Med J, 1994, 70-pp.275–280.
14. Shepard, JW Jr. Hypertension, cardiac arrhythmias, myocardial infarction, and stroke in relation to obstructive sleep apnea. Clin Chest Med, 1992, 13- pp.437– 458.
15. Guilleminault, C; Connolly, SJ; Winkle, RA. Cardiac arrhythmia and conduction disturbances during sleep in 400 patients with sleep apnea syndrome. Am J Cardiol, 1983, 52 - pp.490–494.
16. Hoffstein, V; Mateika, S. Cardiac arrhythmias, snoring, and sleep apnea. Chest, 1994, 106- pp.466–471.
17. Miller, WP. Cardiac arrhythmias and conduction disturbances in the sleep apnea syndrome. Prevalence and significance. Am J Med, 1982, 73-pp.317–321.
18. Randazo, DN; Winters, SL; Schweitzer, P. Obstructive sleep apneainduced supraventricular tachycardia. J Electrocardiol, 1996, 29-pp.65– 67.
19. Tilkian, AG; Guilleminault, C; Schroeder, JS; Lehrman, KL; Simmons, FB; Dement, WC. Sleep-induced apnea syndrome. Prevalence of cardiac arrhythmias and their reversal after tracheostomy. Am J Med, 1977, 63- pp.348–358.
20. Zwillich, C; Devlin, T; White, D; Douglas, N; Weil, J; Martin, R. Bradycardia during sleep apnea. Characteristics and mechanism. J Clin Invest, 1982, 69- pp.1286 –1292.
21. Курлыкина, Н.В., Певзнер, А.В. ; Литвин, А.Ю.; Галицин, П.В.; Чазова, И.Е.; Соколов, С.Ф. ; Голицын, С.П. Возможности лечения больных с длительными ночными асистолиями и синдром обструктивного апноэ сна созданием постоянного положительного давления воздуха в верхних дыхательных путях. //Кардиология.- 2009.- Т. 49(6).-C. 36-42.
22. Garrigue, S; Pépin, J.L; Defaye, P; et al High Prevalence of Sleep Apnea Syndrome in Patients With Long-Term Pacing. Circulation, 2007, 115-pp.1703-1709.
23. Becker, H; Brandenburg, U; Peter, JH; Von Wichert, P. Reversal of sinus arrest and atrioventricular conduction block in patients with sleep apnea during nasal continuous positive airway pressure. Am J Respir Crit Care Med, 1995, 151-pp.215–218.
24. Grimm, W; Hoffmann, J; Menz, V; Kohler, U; Heitmann, J; Peter, JH; Maisch, B. Electrophysiologic evaluation of sinus node function and atrioventricular conduction in patients with prolonged ventricular asystole during obstructive sleep apnea. A
