Физиологические эффекты глюкокортикоидов
Метаболические эффекты
Влияние на обмен углеводов
1. Стимуляция глюконеогенеза в печени – образование глюкозы из аминокислот. Действие обусловлено главным образом двумя различными механизмами. Это: активация транскрипции ДНК в ядрах печеночных клеток с образованием транспортной РНК и последующим синтезом ферментов глюконеогенеза и мобилизация аминокислот из других тканей, главным образом из мышц.
2. Способствуют отложению гликогена в печени и мышцах.
3. Вызывают гипергликемию через:
Ø повышение активности фосфорилазы (глюкозо-6-фосфатазы) печени → усиление расщепления гликогена → выход глюкозы в кровь; в свою очередь, гипергликемия способствует отложению гликогена в печени и мышцах;
Ø увеличение способности пирувата ресинтезироваться в глюкозу в результате торможения его декарбоксилирования;
Ø повышение физиологических эффектов инсулина;
Ø понижение использования глюкозы периферическими тканями и мышцами за счет торможения активности гексокиназы;
Ø активацию всасывания глюкозы в кишечнике.
Длительно протекающая гипергликемия вызывает перенапряжение и функциональную неполноценность инсулярного аппарата, особенно при его генетически обусловленной недостаточности.
Влияние на обмен белков
1. Снижают содержание белков во всех клетках тела за исключением печени в результате угнетения их синтеза и усиления катаболизма. Механизмы эффекта: снижение транспорта аминокислот и угнетение образования РНК во многих тканях, кроме печени (особенно в мышцах и лимфоидной ткани).
2. Активируют синтез белков в клетках печени и повышают их содержание в крови. Механизмы эффекта: увеличение транспорта аминокислот в клетки печени и активности ферментов, необходимых для синтеза белков. Катаболизм белков в клетках способствует выходу аминокислот и увеличению их концентрации в крови. Таким образом, глюкокортикоиды мобилизуют аминокислоты из внепеченочных клеток.
Влияние на жировой обмен
1. Мобилизуют жирные кислоты из жировой ткани, увеличивают их содержание в плазме и утилизацию как источника энергии. Возможный механизм – смешанный транспорт глюкозы в жировые клетки и недостаток α‑глицерофосфата, образующегося из глюкозы. Этот эффект кортизола особенно важен для сохранения глюкозы и гликогена.
2. Стимулируют синтез сурфактанта в легочной ткани. Сурфактант – лецитин, снижающий поверхностное натяжение альвеол и обеспечивающий их расправление. При недостатке синтеза (у недоношенных детей) развивается респираторный дистресс-синдром.
Влияние на минеральный обмен
Кортизол обладает слабо выраженной минералокортикоидной активностью. Он также снижает реабсорбцию кальция и фосфора в почках, что может привести к развитию остеопороза.
Противовоспалительное действие кортизола
Кортизол имеет практически системное действие, подавляя все фазы воспаления. Он блокирует ранние стадии процесса воспаления и препятствует его развитию. Основные механизмы действия в виде патогенетических цепочек следующие.
1. Стабилизация клеточных и лизосомальных мембран → предупреждение их разрыва → лизосомальные ферменты выделяются в чрезвычайно малом количестве (эти ферменты, выделяемые поврежденными клетками – индукторы воспаления).
2. Повышение активности гистаминазы (инактивация гистамина) и инактивация гиалуронидазы (фермент, вызывающий деполимеризацию гиалуроновой кислоты) → снижение проницаемости стенок капилляров.
3. Активация синтеза белка липокортина → угнетение активности фосфолипазы-А2 → угнетение каскада арахидоновой кислоты, т.е. процессов образования эйкозаноидов (простагландинов, простациклина, тромбоксанов, лейкотриенов), являющихся чрезвычайно активными медиаторами воспаления.
4. Стабилизация мембран и уменьшение выделения лизосомальных ферментов → уменьшение миграции лейкоцитов и фагоцитов в очаг воспаления.
5. Блокада транскрипции генов цитокинов и выработки многих факторов макрофагов и лейкоцитов, вовлекаемых в развитие воспаления (интерлейкина-1, интерлейкина-6, фактора некроза опухолей).
6. Снижение экспрессии на эндотелиальных клетках молекул адгезии → ослабление процессов адгезии и эмиграции лейкоцитов.
7. Уменьшение выделения интерлейкина-1 лейкоцитами → снижение лихорадки и степени дилатации.
8. Угнетение иммунной системы, особенно Т-лимфоцитов → снижение количеств Т-лимфоцитов и антител в области воспаления.
9. Блокирование активации системы комплемента.
10. Угнетение белкового синтеза в клетках соединительной ткани и активности фибробластов → ухудшение регенерации соединительной ткани и заживления ран → уменьшение числа коллагеновых нитей в подкожном слое и его легкое растяжение.
Влияние на тимус и лимфоидную систему
Кортизол вызывает лизис клеток тимуса и лимфоидной ткани, а также разрушение Т-клеток в периферической крови и в периферических лимфоидных органах. Механизмы эффекта: активация дезоксирибонуклеазы → разрушение ДНК → освобождение нуклеотидов. Значение: использование освобожденных нуклеотидов для процесса синтеза в надпочечниках и других тканях.
Влияние кортизола на клетки крови
Кортизол снижает число эозинофилов и лимфоцитов в периферической крови. Эффект начинается через несколько минут и становится выраженным через несколько часов. Появление лимфоцитопении и эозинопении используется как диагностический критерий выделения кортизола надпочечниками. Кортизол увеличивает образование эритроцитов.
Влияние кортизола на ЦНС
Глюкокортикоиды обладают нейротропным действием. Установлено наличие рецепторов к кортизолу в нейронах ряда мозговых областей. В физиологических дозах гормон повышает возбудимость мозговых структур и активацию мозга через усиление тонизирующих влияний стволовой ретикулярной формации.
Пермиссивное действие кортизола
Проявляется, например, в модуляции реактивности клеток по отношению к адреналину.
Влияние на эмбриогенез
Основано на ана- и катаболических эффектах глюкокортикоидов. Введение больших доз кортизола во время беременности может вызвать появление пороков развития.
Основные формы патологии
Повышенное содержание в крови глюкокортикоидов (гиперкортизолизм) может быть вызвано экзогенными причинами (введение значительных доз кортизола с лечебными целями) и эндогенными нарушениями, приводящими к гиперсекреции собственного гормона. Гиперпродукция кортизола служит проявлением как первичной патологии коры надпочечников – синдром Иценко-Кушинга (АКТГ-независимый), так и гиперплазии коркового вещества, вызванной повышенной секрецией гипофизарного АКТГ – болезнь Иценко-Кушинга при опухоли передней доли гипофиза или при эктопической продукции АКТГ или кортикотропин-рилизинг фактора (абдоминальная карцинома).
Отличительные признаки
Болезнь Иценко-Кушинга характеризуется двусторонней гиперплазией коры надпочечников и измеримо повышенным уровнем АКТГ в крови.
Синдром Иценко-Кушинга отличается повышенными уровнями кортизола при низких уровнях АКТГ (ниже нормы в результате торможения секреции гормона по механизму отрицательной обратной связи).
Схематически изменения соотношений в гипоталамо-гипофизарно-адреналовой системе приведены на рис. 6, 10, 11 и 12.
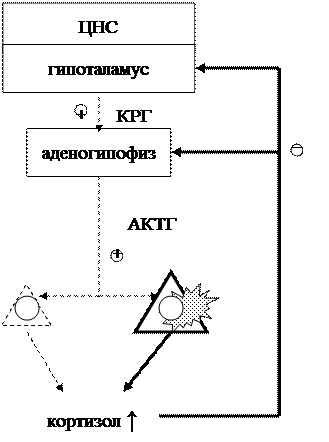 |
Рис. 10. Схема соотношений компонентов гипоталамо-гипофизарно-адрена-ловой оси при первичном гиперкортизолозме вследствие аденомы надпочечника (АКТГ-независимый синдром Иценко-Кушинга).
Условные обозначения как на рис. 5, 6.
