Экспериментальная часть. Изучение процесса кристаллизации
Изучение процесса кристаллизации
Цель работы
1. Познакомиться с процессом кристаллизации и формой растущих кристаллов на примере кристаллизации из растворов солей.
2. Охарактеризовать влияние условий кристаллизации на строение металлического слитка по лабораторным образцам.
Теоретическая часть
Обычно в микроструктуре металлического слитка просматриваются три зоны:
1) наружная, состоящая из мелких, беспорядочно ориентированных кристаллов, образующихся в начальный период затвердевания;
2) зона столбчатых кристаллов из зерен, вытянутых перпендикулярно охлаждающим поверхностям изложницы;
3) внутренняя зона из равноосных зерен.
Наличие зон связано с особенностями кристаллизации, изменяется соотношение между объемами, занятыми различными зонами, и даже можно получить слиток, состоящий только из 2-х или 1-ой зоны.
Процесс кристаллизации состоит из двух элементарных актов:
1) образования зародышей (центров кристаллизации);
2) роста кристаллов из этих центров.
Процесс кристаллизации протекает только тогда, когда кристаллическое состояние обладает меньшей свободной энергией по сравнению с жидким.
На рис. 1 представлено изменение свободной энергии жидкости и кристаллов в зависимости от температуры.
Выше температуры Тр более устойчивое жидкое состояние, ниже температуры Тр - кристаллическое, в связи с более низким значением свободной энергии. При температуре Тр величины свободных энергий обоих состояний равны: металл при температуре Тр может находиться как в жидком, так и в твердом состоянии. Температуру Тр называют равновесной или теоретической температурой кристаллизации.
Однако, при температуре Тр процесс кристаллизации протекать не может. Основной трудностью на пути кристаллизации является необходимость образования зародышей. Образование зародыша сопряжено с возникновением границ раздела. Поскольку атомы, находящиеся на границах, обладают более высокой энергией, чем атомы в объеме самих кристаллов, кристаллизация сможет начаться только тогда, когда разность свободных энергией Df (см. рисунок 1) жидкости и кристаллов будет достаточной для компенсации энергии, необходимой для образования границы раздела фаз.
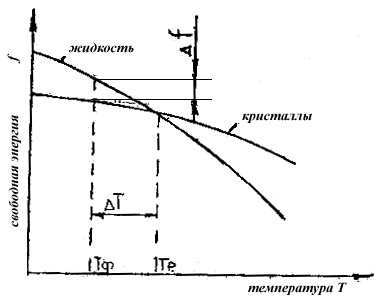 |
Рисунок 1. Изменение свободной энергии жидкого и кристаллического состояния в зависимости от температуры
Такая разность свободных энергий Df имеет место только при температурах ниже Тр. Температура, при которой практически происходит кристаллизация, называется фактической температурой кристаллизации Тф (см. рисунок 1.). Разность между теоретической и фактической температурами кристаллизации называется величиной или степенью переохлаждения.
DТ = Тр – Тф (1)
Общее изменение свободной энергии системы при образовании кристаллического зародыша можно записать следующим образом:
DF = - VDf + Sd, (2)
где Df – разность свободных энергий жидкости и кристаллов на единицу объема;
V – объем зародыша;
d - поверхностное натяжение, энергии на единицу поверхности раздела;
S – суммарная величина поверхности кристаллов.
Если условно принять, что зародыш имеет сферическую форму, то это выражение примет вид:
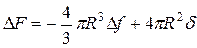 , (3)
, (3)
где R – радиус зародыша.
Анализ этой функции показывает, что при увеличении радиуса зародыша R, она сначала растете, а затем уменьшается. Максимум функция имеет при
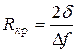 . (4)
. (4)
Следовательно, рост зародышей размером менее Rкр. привел бы к повышению свободной энергии системы. Такие зародыши будут исчезать. Зародыши размером более Rкр. способны к росту, так как при увеличении их размеров свободная энергия системы уменьшается. Минимальный размер способного к росту зародыша при данной температуре называется критическим размером зародыша.
При увеличении переохлаждения поверхностное натяжение не изменяется, а Df непрерывно растет (рис. 1), поэтому с ростом переохлаждения критический размер зародыша уменьшается (см. выражение 4). С уменьшением критического размера зародыша повышается вероятность его образования.
При малом числе зародышей зерно получается крупным, при большом числе зародышей вырастают мелкие кристаллы, тормозящие рост друг друга.
Следовательно, условия охлаждения определяют размеры кристаллов: чем больше переохлаждение или чем больше скорость охлаждения, тем мельче размер зерна. Направленный теплопровод способствует возникновению вытянутых (столбчатых) кристаллов, растущих в направлении противоположном теплоотводу
Условия охлаждения определяют также форму растущих кристаллов. При очень малом переохлаждении образуются правильно ограненные кристаллы. При увеличении переохлаждения образуются обычно кристаллы дендритной (древовидной) формы. Схема дендритного кристалла показана на рис. 2.
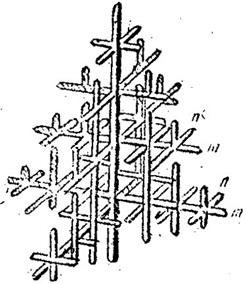 |
Рисунок 2. Схема дендритного кристалла
Металлам, кристаллизующимся с большой скоростью, наиболее присуща дендритная форма кристаллов.
Экспериментальная часть
Для выполнения работы необходимы:
1.Биологический микроскоп;
2. Лупа;
3. Пересыщенные растворы солей NH4Cl и NaCl;
4. Электрическая плитка;
5. Предметные стекла;
6. Образцы слитков стали и алюминия лабораторной коллекции с выявленной макроструктурой.
Экспериментально наиболее просто осуществить непосредственное наблюдение процесса кристаллизации из пересыщенных водных растворов солей.
Работа выполняется в следующей последовательности:
Нагреть растворы солей NH4Cl и NaCl до полного растворения кристаллов.
На чистое предметное стекло вылить каплю горячего раствора хлористого аммония и, поместив каплю под лупу, наблюдать за изменениями, происходящими в капле. При этом нужно обратить внимание на следующие моменты:
а) где начинается процесс кристаллизации;
б) какова форма первых кристаллов;
в) в каком направлении продолжается процесс кристаллизации;
г) какова форма кристаллов, образующихся в следующую очередь;
д) где завершается кристаллизация;
е) какие кристаллы появляются в конце кристаллизации;
ж) какие три зоны кристаллизации можно выделить.
Сделав указанные наблюдения, схематически зарисовать строение закристаллизовавшейся капли хлористого аммония, обозначив три зоны кристаллизации.
На чистое предметное стекло вылить каплю горячего раствора поваренной соли и провести аналогичные наблюдения.
Исследовать форму отдельных кристаллов NH4Cl и NaCl при помощи биологического микроскопа и зарисовать их.
Описать последовательность кристаллизации солей NH4Cl и NaCl, указывая на общие черты и различия. Обратить внимание на размер и форму кристаллов в разных зонах, связывая эти параметры с величиной переохлаждения и направлением теплоотвода.
На готовых образцах слитков и алюминия из лабораторной коллекции изучить макроструктуру: число зон, протяженность зон, размеры и форму кристаллов в каждой зоне.
Зарисовать макроструктуру этих образцов: написать условия образования структуры каждого из образцов (переохлаждение, направленность теплоотвода).
Содержание отчета
Отчет должен содержать следующие части:
1. Название работы.
2. Цель работы.
3. Теоретическую часть, в которой кратко изложено влияние условий охлаждения на величину и форму образующихся кристаллов и на строение металлического слитка.
4. Экспериментальная часть, включающая:
а) схематические рисунки закристаллизовавшихся капель NH4Cl и NaCl с обозначением отдельных зон;
б) схематические рисунки отдельных кристаллов NH4Cl и NaCl;
в) описание процесса кристаллизации;
г) схематические рисунки макроструктуры образцов слитков стали и алюминия из лабораторной коллекции с описанием условий их образования.
