Определение рн растворов. гидролиз солей
Цель работы: практическое определение рН растворов, изучение реакций гидролиза солей.
ОПРЕДЕЛЕНИЕ рН РАСТВОРОВ
Водородный показатель – это величина, характеризующая концентрацию водородных ионов и численно равная отрицательном десятичному логарифму этой концентрации, моль/л:
рН = – lg [H+].
При рН = 7 – среда нейтральная; при рН < 7 среда кислая; при рН > 7 – среда щелочная.
Для определения рН применяют калориметрические и электрометрические методы.
При калориметрическом методе определения рН пользуются индикаторной бумагой и жидкими индикаторами.
ОПЫТ 1.1. Определение рН растворов посредством универсальной индикаторной бумаги.
Пользуясь индикаторной бумагой, определить рН растворов воды, уксусной, соляной кислот, гидроксида аммония, гидроксида натрия, сульфата алюминия, карбоната натрия, гидрокарбоната натрия, хлорида натрия, ацетата натрия и ацетата аммония.
Таблица 6
| № п/п | Формула вещества | рН | [H+] | [OH–] | Характер среды |
| H2O | 10-7 | 10-7 | нейтральная | ||
| CH3COOH | |||||
| HCl | |||||
| NH4OH | |||||
| NaOH | |||||
| Al2(SO4)3 | |||||
| Na2CO3 | |||||
| NaHCO3 | |||||
| NaCl | |||||
| CH3COONa | |||||
| CH3COONH4 |
Для определения рН растворов на листе белой бумаги разложить 11 полосок индикаторной бумаги и перенести на каждую по одной капле исследуемого раствора. Сравнить окраску еще сырого пятна, полученного на бумаге с цветной шкалой. На последней указано, при каких значениях рН индикаторная бумага окрашивается в тот или иной цвет. Сделать вывод о величине рН данного раствора и указать реакцию среды. Результаты опытов занесите в таблицу (табл. 6).
ГИДРОЛИЗ СОЛЕЙ
Гидролиз соли - это взаимодействие ионов соли с водой, приводящее к образованию слабого электролита и сопровождающееся изменением концентрации ионов водорода и гидроксила.
ОПЫТ 2.1. Гидролиз солей.
Какие из взятых в предыдущем опыте солей подвергаются гидролизу? Написать уравнения реакций в молекулярной и ионной формах. Объяснит, почему рН карбоната и гидрокарбоната натрия различны.
ОПЫТ 2. Совместный гидролиз двух солей.
В пробирку внести по 3 - 4 капли растворов сульфата алюминия и карбоната натрия. Отметить выделение оксида углерода (IV) и выпадение осадка гидроксида алюминия. Написать уравнение реакции в молекулярной и ионной формах.
Сделайте вывод по работе на основании проделанных опытов.
Контрольные вопросы
1. Для одного раствора рН = 5, для другого – рН = 2. Какой раствор более кислый? Во сколько раз в нем концентрация водородных ионов выше, чем в другом?
2. Чему равен рН 0,0001 М раствора соляной кислоты?
3. Какова концентрация гидроксид-ионов в растворе с рН = 4?
4. Какие факторы влияют на степень гидролиза?
5. Напишите уравнения реакций гидролиза следующих солей (если таковой происходит): K3PO4, CrCl3, Fe2S3, Na2SO4 в молекулярном и ионном виде.
Лабораторная работа № 9
ЖЕСТКОСТЬ ВОДЫ
ЦЕЛЬ РАБОТЫ: изучение и определение различных видов жесткости воды.
ОПЫТ 1. Определение временной жесткости.
Временная жесткость определяется титрованием природной воды соляной кислотой, которая переводит гидрокарбонаты кальция и магния в хлориды.
Выполнение работы
В две конические колбочки отмерить пипеткой по 50 мл водопроводной воды и оттитровать ее 0,1н раствором соляной кислоты в присутствии 1 - 2 капель индикатора метилоранжа до слабой желто-розовой окраски. Если результаты титрования расходятся в допустимых пределах (0,1 мл), то титрование можно считать законченным. В противном случае, вымыв тщательно колбочки, повторить титрование с новыми порциями исследуемой воды.
Расчет временной жесткости производят по формуле:
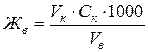 ,
,
ЖВ – временная жесткость воды, мг-экв/л;
VК – объем раствора кислоты, израсходованный на титрование, мл;
CК – нормальность раствора кислоты;
VB – объем воды, мл.
 ОПЫТ 2. Определение общей жесткости трилонометрическим методом.
ОПЫТ 2. Определение общей жесткости трилонометрическим методом.
В настоящее время общую жесткость воды определяют с помощью трилона-Б. Метод основан на образовании трилоном-Б малодиссоциированных комплексов с солями жесткости. В качестве индикаторов используются оксинитрокрасители, например, хромоген-черный (ЕТ-00).
Этот метод применятся для воды с различным содержанием солей. Однако реакция раствора при титровании должна быть слабо щелочной.
При титровании и отборе проб воды необходимо придерживаться следующих объемов (см. табл. 7):
Таблица 7
| Концентрация ионов кальция и магния в мл в мг-экв/л | Объем воды для титрования в мл |
| 0,5-5,0 | |
| 5,0-10,0 | |
| 10,0-20,0 | |
| 20,0-50,0 |
Выполнение работы
В две конические колбы емкостью 200 мл отмерить пипеткой 50 мл исследуемой воды, добавить мензуркой 50 мл дистиллированной воды, 5 мл буферного раствора (20 г хлорида аммония + 100 мл гидроксида аммония в литре раствора), поддерживающего рН исследуемой жидкости, затем добавить 7 капель индикатора хромогена-черного. Жидкость перемешать и оттитровать 0,04н раствором трилона-Б до перехода фиолетово-красной окраски в зеленовато-голубую.
Вычислить общую жесткость воды по формуле:
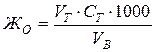
где ЖО – общая жесткость воды, мг-экв/л;
VT – объем раствора триллона-Б, израсходованного на титрование, мл;
СТ – нормальность раствора трилона-Б;
VB – объем исследуемой воды, мл.
ЖП = ЖО + ЖВ
ЖП – постоянная жесткость, мг-экв/л.
ОПЫТ 3. Определение ионов кальция в воде.
Данный метод, как и определение общей жесткости, основан на применении трилона-Б с той разницей, что индикатором служит мурексид, позволяющий вести титрование в сильнощелочной среде, когда ионы Mg2+ практически полностью выпадают из раствора.
«Свидетель» готовят в отдельной колбе, для чего берут 25 мл дистиллированной воды, добавляют 0,15 г мурексида, 2 мл 2н NaOH и 2 -3 капли трилона-Б. Трилон-Б в присутствии 2н NaOH (рН = 13) не образует комплекса с ионами магния.
В две конические колбы емкостью 200 мл отмерить пипеткой 50 мл исследуемой воды, добавить 2 мл 2н раствора гидроксида натрия, 10 - 15 мг индикатора мурексида (приблизительно на кончике маленького шпателя) и немедленно титруют 0,04н раствором трилона-Б до перехода красно-фиолетового цвета раствора в сине-фиолетовый (лиловый, что лучше всего установить по «свидетелю»).
Вычисление:
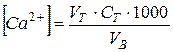 ,
,
где ЖВ – временная жесткость воды, мг-экв/л;
VT – объем раствора триллона-Б, израсходованного на титрование, мл;
СТ – нормальность раствора трилона-Б, г-экв/л;
VB – объем исследуемой воды, мл.
Содержание Mg2+ определяют по разности [Мg2+] = ЖO – [Са2+].
Опыт 4а. Очистка воды с помощью ионитов.
При контакте с ионитами происходит обмен содержащихся в воде катионов на Н+ катионита и анионов на ОН- анионита в эквивалентных количествах, например
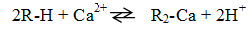
катионит р-р катионит р-р
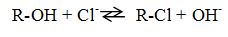
анионит р-р анионит р-р
В результате этого процесса содержание в воде примесей уменьшается, и она становится мягкой.
опыт 4Б. Очистка воды от ионов кальция.
Отбирают цилиндром 250 мл исследуемого раствора и вносят в колонку с катионитом КУ-2 в R-H форме. Осторожно открывают зажим внизу колонки и вытекающий из колонки со скоростью одна капля в секунду раствор собирают в колбу.
Во время обработки раствора нужно следить за тем, чтобы поверхность ионита в колонке все время оставалась покрытой жидкостью. Затем производят определение общей жесткости воды, как в опыте 2.
Сравнение результатов анализа покажет, что содержание ионов кальция и общая жесткость воды значительно понижаются, вода становится мягкой даже после однократного пропускания раствора через колонку с катионитом.
Опыт 5 .Очистка воды от ионов хлора.
В растворе, полученном в опыте 4а, после пропускания его через колонку с катионитом, качественно определяют ионы Сl-.
Для этого в пробирку берут 0,3 мл раствора, добавляют несколько капель раствора AgNO3. Присутствие при этом белого творожистого осадка AgCl свидетельствует о том, что катионит не извлекает из воды ионы хлора.
Для удаления ионов хлора отбирают 25 мл обработанного катионитом раствора и пропускают его через колонку с анионитом АВ-17 в R-OH форме (как в опыте 4а).
Собирают 0,3 мл вытекающего из колонки раствора и снова выполняют качественную реакцию на ион Сl-. При этом обычно белый осадок хлорида серебра не выпадает, что указывает на полное поглощение хлорид-ионов анионитом АВ-17 (R-OH формы).
ОПЫТ 6. Определение рН.
О процессах обмена ионов водорода катионита и гидроксид-ионов анионита соответственно на ионы Са2+ и Сl-, содержащихся в исследуемом растворе (жесткая вода), можно судить по изменению его рН, нанося пробу на индикаторную бумажку.
При пропускании через катионит раствор становится более кислым, на что укажет заметное снижение его рН (2R-H + Са2+ Û R2-Ca + 2Н+).
После обработки анионитом рН раствора, наоборот, повышается, в результате повышения в нем концентрации ионов ОН-.
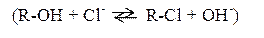
Контрольные вопросы
1. Написать уравнение реакции взаимодействия гидрокарбоната кальция или
магния с кислотой.
2. С какой целью добавляется буферный раствор, концентрированный раствор гидроксида натрия?
3. Почему в воде, пропущенной через колонку с катионитом, при добавлении раствора нитрата серебра выпадает осадок хлорида серебра?
4. Как изменяется рН воды после обработки ее катионитом и анионитом? Написать уравнения реакций.
Лабораторная работа № 10.
ГАЛЬВАНИЧЕСКИЙ ЭЛЕМЕНТ
Цель работы: измерение электродвижущей силы гальванического элемента.
ОПЫТ 1. Определение ЭДС гальванического элемента Вольта
Налить, в стаканчик (2/3 объема) 1М-ный раствор серной кислоты. Поставить его в углубление подставки и опустить в раствор H2SO4 медный и цинковый электроды. Наблюдать отклонение стрелки гальванометра.
1. Запишите показания вольтметра.
2. Из таблицы нормальных стандартных потенциалов выпишите значения электродных потенциалов металлов.
3. Запишите схему гальванического элемента, укажите на ней стрелками направление движения электронов и ионов.
4. Запишите уравнения электродных процессов.
5. Рассчитайте стандартную ЭДС элемента и сравните ее с экспериментальным значениям. Объясните различие в значениях ЭДС.
ОПЫТ 2. Определение ЭДС гальванического элемента Даниэля-Якоби
В один из стаканчиков налейте 2/3 его объема 2М раствор сульфата цинка ZnSO4, во второй стаканчик такой же объем 2М раствора сульфата меди CuSO4. Оба стаканчика поставить в углубления подставки. Цинковую и медную пластинки погрузите в растворы солей соответствующих металлов. Соедините стаканчики электролитным мостиком.
1. Запишите показания вольтметра.
2. Запишите схему гальванического элемента и уравнения электродных процессов.
3. По уравнению Нернста рассчитайте величины равновесных потенциалов электродов, использованных в элементе.
4. Рассчитайте ЭДС элемента и сравните ее с экспериментальным
значениям. Объясните различие в значениях ЭДС.
Контрольные вопросы
1 - 4. Напишите схему гальванического элемента, составленного из электродов А и Б, погруженных в растворы их солей указанных концентраций. Рассчитайте значения равновесных потенциалов обоих электродов и ЭДС элемента. Составьте уравнения реакций, протекающих на электродах и суммарное уравнение токообразующей реакции.
| Задача | А | Б |
| 1. | Cu 0,01 M CuSO4 | Mg 0,3 M MgCl2 |
| 2. | Zn 1,0 M ZnSO4 | Cr 0,002 M Cr(NO3)3 |
| 3. | Sn 0,2 M SnCl2 | Fe 0,5 M FeSO4 |
| 4. | Ni 0,5 M NiCl2 | Ag 0,03 M AgNO3 |
5 - 9. Рассчитайте ЭДС электрохимической цепи, образованной электродами из одного и того же металла, погруженными в растворы разных концентраций.
| Задача | Металл | Соль | Концентрация соли, моль/л | |
| С1 | С2 | |||
| 5. | Ag | AgNO3 | 0,04 | 0,002 |
| 6. | Ni | NiSO4 | 1,0 | 0,006 |
| 7. | Cd | CdCl2 | 0,2 | 0,005 |
| 8. | Cr | Cr(NO3 | 0,03 | 0,004 |
| 9. | Pb | Pb(NO3)2 | 0,5 | 0,001 |
Лабораторная работа № 11.
ЭЛЕКТРОЛИЗ растворов
Цель работы: ознакомление с процессами, протекающими на электродах при электролизе водных растворах электролитов.
ОПЫТ 3. Электролиз водных растворов с инертными электродами
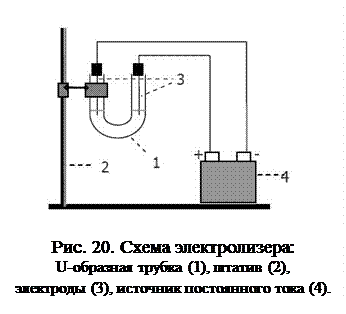 Электролиз водных растворов с инертными электродами. Опыты проводятся в электролизере – U-образной стеклянной трубке, которая закрепляется в зажиме штатива (рис. 20). В качестве электродов используются графитовые стержни. Электролизер заполняется электролитом на 2/3 его объема. Электроды перед каждым опытом тщательно промывают дистиллированной водой и опускают в оба колена электролизера.
Электролиз водных растворов с инертными электродами. Опыты проводятся в электролизере – U-образной стеклянной трубке, которая закрепляется в зажиме штатива (рис. 20). В качестве электродов используются графитовые стержни. Электролизер заполняется электролитом на 2/3 его объема. Электроды перед каждым опытом тщательно промывают дистиллированной водой и опускают в оба колена электролизера.
