Кривая титрования сильной кислоты щёлочью
Аналитическая реакция – реакция нейтрализации
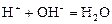 .
.
1 этап. В растворе присутствует только сильная кислота, рН раствора определяется её концентрацией:
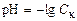 ,
,
где СK – нормальная концентрация кислоты.
2 этап. Процесс титрования. Происходит постепенная нейтрализация кислоты щёлочью:
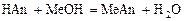 .
.
рН вычисляется по уравнению:
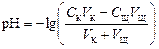 ,
,
где VK – объём пробы кислоты, взятый для титрования (аликвота), СЩ – нормальная концентрация раствора щёлочи, VЩ – объём раствора щёлочи, добавленного в процессе титрования.
3 этап. Точка эквивалентности. В системе находится только негидролизующаяся соль. рН = 7. На нейтрализацию кислоты затрачен эквивалентный объём щелочи VЭ.
4 этап. Добавление избытка титранта после точки эквивалентности. рН определяется только количеством добавленной щёлочи и вычисляется по уравнению:
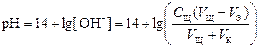 .
.
Пример. Рассчитать кривую титрования 10 мл 0,1 н. соляной кислоты 0,1 н. раствором гидроксида натрия.
| VNaOH, мл | Система | Расчётная формула | рН |
| 0,1 н. раствор HCl | 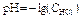 | 1,00 | |
| Титрование соляной кислоты. | 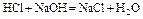 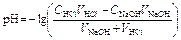 | 1,09 | |
| 1,48 | |||
| 1,75 | |||
| 2,28 | |||
| 9,5 | 2,59 | ||
| 9,9 | 3,30 | ||
| NaCl | Точка эквивалентности, VЭ = 10 мл, VΣ = 20 мл | 7,00 | |
| 10,1 | Избыток щёлочи | 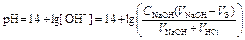 | 10,70 |
| 11,68 | |||
| 11,96 | |||
| 12,30 | |||
| 12,52 |
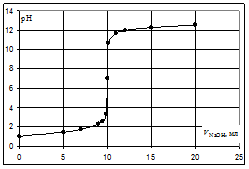
Кривая титрования сильной кислоты щелочью
Точка эквивалентности соответствует объёму титранта 10 мл. Обращает внимание резкий скачок величины рН в этой области. Объём одной капли раствора обычно составляет 0,01-0,02 мл. В области эквивалентной точки при добавлении капли щёлочи рН возрастает на 3-6 единиц. Поэтому эквивалентную точку можно определить с помощью любого цветного индикатора, изменяющего окраску в области значений рН от 4 до 10.
Кривая титрования сильного основания кислотой
Аналитическая реакция – реакция нейтрализации
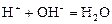 .
.
1 этап. В растворе присутствует только щёлочь и рН раствора определяется её концентрацией:
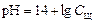 .
.
2 этап. Процесс титрования. Происходит постепенная нейтрализация щелочи кислотой:
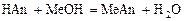 .
.
рН вычисляется по уравнению:
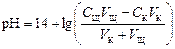 .
.
3 этап. Точка эквивалентности. В системе находится только негидролизующаяся соль. рН = 7. На нейтрализацию кислоты затрачен эквивалентный объём кислоты VЭ.
4 этап. После точки эквивалентности рН определяется только количеством добавленной кислоты и вычисляется по уравнению:
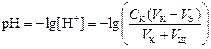 .
.
Пример. Рассчитать кривую титрования 10 мл 0,1 н. гидроксида натрия 0,1 н. раствором соляной кислоты.
| VNaOH, мл | Система | Расчётная формула | рН |
| 0,1 н. раствор NaOH | 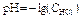 | 13,00 | |
| Титрование гидроксида натрия. | 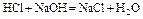 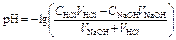 | 12,91 | |
| 12,52 | |||
| 12,25 | |||
| 11,72 | |||
| 9,5 | 11,41 | ||
| 9,9 | 10,70 | ||
| NaCl | Точка эквивалентности, VЭ = 10 мл, VΣ = 20 мл | 7,00 | |
| 10,1 | Избыток кислоты | 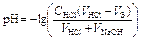 | 3,30 |
| 2,32 | |||
| 2,04 | |||
| 1,70 | |||
| 1,48 |
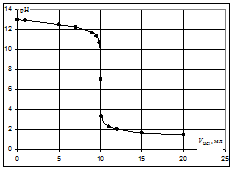
Кривая титрования сильного основания кислотой
Кривая титрования щёлочи кислотой является зеркальным отражением кривой титрования сильной кислоты щёлочью. Эквивалентную точку можно определить с помощью любого цветного индикатора, изменяющего окраску в области значений рН от 4 до 10.
