Классификация методов оптического анализа
1. Методы, основанные на поглощении веществом светового потока. К ним относятся фотоколориметрия и спектрофотометрия.
2. Методы, основанные на излучении веществом электромагнитных волн. К ним относятся фотометрия пламени, атомно-флуоресцентный анализ и др.
В основе фотоколориметрического анализа лежит закон светопоглощения Бугера-Ламберта-Бера: при прохождении светового потока через поглощающий раствор интенсивность прошедшего светового потока (I) отличается от интенсивности падающего светового потока (Io) на поглощение света раствором.
Обычно Т выражают в %: 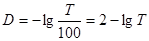
D– 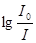 – важная характеристика раствора, называется оптической плотностью.
– важная характеристика раствора, называется оптической плотностью.
Т – I/Io называется пропусканием раствора.
Уменьшение интенсивности света при прохождении через поглощающий раствор подчиняется закону Бугера-Ламберта-Бера:
I = I0 · 10‾cb или D = ε bc,
где ε– молярный коэффициент поглощения, являющийся основной характеристикой поглощения света системой при данной длине волны.
Причины отклонения от закона:
1) изменение степени диссоциации при разбавлении;
2) изменение степени гидратации ионов;
3) присутствие посторонних электролитов
Важным дополнением к закону Б-Л-Б является закон аддитивности светопоглощения.Если в растворе присутствует несколько поглощающих веществ, то оптическая плотность раствора равна сумме вкладов каждого из компонентов:Д=Д1+Д2+Д3
Чтобы обеспечить максимальное поглощение в ФЭКе есть набор светофильтров. Светофильтры – это специальные стёкла, поглощающие излучение определённых длин волн.
53. Величины, характеризующие лучистую энергию: оптическая плотность и пропускание. Выбор оптимальных условий проведения фотометрической реакции. Фотометрическое определение железа (III) сульфосалициловой кислотой.
Рассчитывают концентрации (мг/см3) Fe3+ в стандартных растворах:
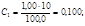
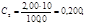
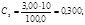
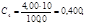
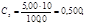
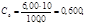
Градуировочный график линеен, выходит из начала координат:
D
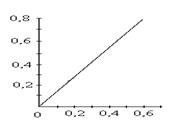 См(Fe3+), мг/см3
См(Fe3+), мг/см3
Для расчета концентрации Fe3+ в анализируемых растворах применяют соотношение: 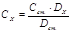
где СХ и Сст. – концентрации определяемого вещества в анализируемом и стандартном растворах;
DХ и Dст. – оптические плотности растворов.
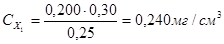
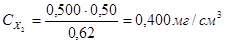
54. Основы фотометрического анализа. Фотометрические методы определения одного вещества в растворе (метод градуировочного графика, метод добавок, метод сравнения оптический плотности стандартного и исследуемого окрашенных растворов).
Фотометрический анализ (молекулярная абсорционная спектроскопия) основан на способности вещества поглощать электромагнитные излучения оптического диапазона. В основе фотометрического анализа лежит избирательное поглощение света частицами (молекулами и ионами) вещества в растворе. При некоторых длинах волн свет поглощается интенсивно, а при некоторых – не поглощается совсем.
Методы фотометрического анализа
 |  |
фотоколориметрия спектрофотометрия
анализ на основе измерения анализ на основе измерения
поглощения излучения видимой поглощения УФ, видимой и
области спектра ИК областей спектра
Прибор: Прибор: спектрофотометр
фотоэлектроколориметр (ФЭК)
Фотоколориметрические методы широко распространены в работе клинических лабораторий для количественного определения йода, азота, мочевой кислоты в моче, билирубина и холестерина в крови и желчи, гемоглобина в крови и т.д. В санитарно-гигиеническом анализе колориметрия применяется для определения аммиака, фтора, нитратов и нитритов, солей железа, витаминов и других веществ.
Фотоколориметрический метод анализа основан на сравнении интенсивности окраски исследуемого раствора с окраской раствора, концентрация которого неизвестна. Раствор с известной концентрацией называется стандартным или образцовым раствором.
Этим методом можно анализировать лишь окрашенные растворы. Если раствор бесцветный, то в него добавляют реагент, образующий окрашенное соединение с исследуемым веществом (фотометрическая реакция).
исслед. в-во + реагент ↔ окраш. соед.
Cu2+ + 4NH3 ↔[Cu(NH3)4]2+
Fe3+ +6CN- ↔ [ Fe(CN)6]3-
Существуют различные методы фотоколориметрического определения вещества в растворе:
1. Метод калибровочного (градуировочного) графика. Готовят серию из 5-8 стандартных растворов разных концентраций, измеряют их оптическую плотность, строят график в координатах Д–С. Затем измеряют поглощение анализируемого раствора и по графику определяют его концентрацию (см. рис. 4).
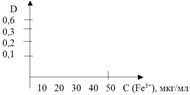 График зависимости оптического поглощения от концентрации
График зависимости оптического поглощения от концентрации
2. Метод добавок. К анализируемому раствору добавляют точную навеску вещества. Измерив оптическую плотность раствора с добавкой (D) и без добавки (D0), рассчитывают концентрацию анализируемого раствора (С0): 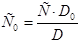
3. Метод стандартных растворов. Оптическую плотность исследуемого раствора (DX) сравнивают с оптической плотность стандартного раствора (Dст.) этого же вещества. Неизвестную концентрацию исследуемого раствора (СХ) рассчитывают по формуле: 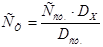 где Сст. – концентрация стандартного раствора, моль/л.
где Сст. – концентрация стандартного раствора, моль/л.
55. Потенциометрический метод. Теоретические основы метода, классификация
Потенциометрия– совокупность физико-химических методов анализа, основанных на измерении э.д.с специально составленных ГЭ.
Классификация по способу применения электрохимических методов.
а) Прямые методы. Измеряют электрохимический параметр как известную функцию концентрации раствора и по показанию соответствующего измерительного прибора находят содержание определяемого вещества в растворе (определение рН растворов).
б) Косвенные методы — это методы титрования, в которых окончание титрования фиксируют на основании измерения электрических параметров системы (потенциометрическое титрование).
В соответствии с данной классификацией различают, например, прямую кондуктометрию и кондуктометрическое титрование, прямую потенциометрию и потенциометрическое титрование и т.д.
Потенциометрическое титрование – это любой метод титриметрического анализа, в котором точка эквивалентности фиксируется по резкому изменению э.д.с гальванического элемента, опущенного в исследуемый раствор.
При потенциометрическом титровании анализируемый раствор, находящийся в электрохимической ячейке, титруют подходящим титрантом, фиксируя конец титрования по резкому изменению ЭДС измеряемой цепи — потенциала индикаторного электрода, который зависит от концентрации соответствующих ионов и резко изменяется в точке эквивалентности.
Применение потенциометрического титрования. Метод универсальный, его можно применять для индикации конца титрования во всех типах титрования: кислотно-основном, окислительно-восстановительном, комплексиметрическом, осадительном, при титровании в неводных средах. В качестве индикаторных используют стеклянный, ртутный, ион-селективные, платиновый, серебряный электроды, а в качестве электродов сравнения — каломельный, хлорсеребряный, стеклянный.
Методами потенциометрического титрования анализируют многие лекарственные вещества, например, аскорбиновую кислоту, сульфамидные препараты, барбитураты, алкалоиды и др.
Потенциометрические методы анализа позволяют:
• анализировать окрашенные растворы, растворы с осадком и гели,
• получать точные результаты в короткое время (экспресс-анализ),
• анализировать состав биологических жидкостей человека без их разрушения, путем введения электродов в пораженные органы и ткани.
56. Прямая потенциометрия и потенциометрическое титрование, их область применения. Электроды и их классификация. Методы измерения ЭДС.
Потенциометрический анализ основан на измерении ЭДС и электродных потенциалов как функции концентрации анализируемого раствора.
Применение прямой потенциометрии. Метод применяется для определения концентрации ионов водорода (рН растворов), анионов, ионов металлов (ионометрия).
При потенциометрических измерениях в электрохимической ячейке используют два электрода: индикаторный электрод, потенциал которого зависит от концентрации определяемого вещества в анализируемом растворе, и электрод сравнения, потенциал которого в условиях проведения анализа остается постоянным. Поэтому величину ЭДС можно рассчитать как разность реальных потенциалов этих двух электродов.
В потенциометрии используют электроды следующих типов: электроды первого, второго рода, окислительно-восстановительные, мембранные электроды.
Типы электродов, применяемых в потенциометрии:
Электроды 1-го рода – металл, опущенный в раствор своей соли:
Cu / Cu2+aq; Zn / Zn2+aq
Электроды 2-го рода – металл, покрытый слоем своего труднорастворимого соединения и опущенный в раствор соли.
