Физико-химические методы количественного анализа позволяют определять состав вещества, не прибегая к использованию химикатов, т.е. когда химические реакции не протекают
Лекция 14. Аналитическая химия
Аналитическая химия, представляя собой один из разделов прикладной химии, определяется как наука, изучающая свойства и процессы превращения веществ с целью установления их химического состава.
Установить химический состав вещества - это ответить на вопрос о том, какие элементы или их соединения и в каком количестве содержатся в анализируемом веществе.
В зависимости от характера анализируемого вещества различают анализ неорганических и органических материалов, что обусловлено особенностью органических соединений по сравнению с неорганическими.
В зависимости от характера поставленной задачи различают два вида анализа - качественный и количественный. Качественный анализ позволяет ответить на вопрос, какие вещества находятся в данной пробе; количественный анализ отвечает на вопрос, в каких количествах обнаруженные вещества присутствуют в данной пробе.
Качественный анализ. Химический анализ состоит в основном из следующих этапов - отбор пробы, разложение пробы с переводом в раствор, проведение химической реакции или измерение какого-либо физического параметра.
В основе деления катионов на группы лежат реакции с кислотами и основаниями. При последовательной обработке смеси: а) соляной кислотой, б) серной кислотой, в) избытком щелочи в присутствии пероксида водорода, г) раствором аммиака – выделяют следующие группы:
1. Ионы, не образующие осадки не с одним из перечисленных реактивов: К+, Na+ и NH4+.
2. Ионы, образующие нерастворимые хлориды: Ag+,Pb+2,Hg2+2
3. Ионы, образующие нерастворимые сульфаты: Вa+2, Ca+2, Sr+2
4. Ионы, образующие гидроксиды, растворимые в избытке щелочи: Al3+, Cr3+, Zn2+, Sn2+, Sn4+
5. Ионы, образующие гидроксиды, нерастворимые ни в избытке щелочи, ни в аммиаке: Fe2+, Fe3+, Mn2+, Mg2+, Bi3+, Sb3+
6. Ионы, образующие гидроксиды, растворимые в аммиаке: Co2+, Cu2+, Ni2+, Hg2+, Cd2+.
В основу классификации анионов положена растворимость солей бария и серебра соответствующих кислот (таблица 1.).
Количественный анализ. Предмет количественного анализа - изучение методов, позволяющих определять количественный состав вещества.
Задача количественного анализа - определение количественного содержания химических элементов в соединениях. Методы количественного анализа разделяются на химические, физические и физико-химические.
К химическим методам анализа относятся гравиметрический (весовой) и титриметрический (объемный).
Сущность гравиметрического (весового) метода анализа состоит в том, что определяемый компонент переводится в нерастворимое состояние, т.е. в осадок, который отделяется путем фильтрования от раствора, а затем после высушивания или сжигания взвешивается.
Таблица 1. Классификация анионов
| Номер группы | Характеристика группы | Анионы, образующие группу | Групповой реагент |
| Соли бария трудно растворимы в воде | SO42–, SO32–, S2O32–, CO32–, PO43–, AsO43, AsO3–, SiO32–, BO2–B4O72–, CrO42–, F–, C2O42- и др. | ВaCl2 в нейтральном или слабощелочном растворе | |
| Соли серебра трудно растворимы в воде и разбавленной HNO3 | Cl–, Br–, J–, S2– и др. | AgNO3 в присутствии HNO3 | |
| Соли бария и серебра растворимы в воде | NO3–, NO2–, CH3COO–, MnO4-. | Нет |
При выполнении титриметрического (объемного) метода взвешивание заменяется измерением объема. В качестве примера можно привести метод кислотно-основного титрования, который основан на использовании реакции нейтрализации между кислотами и основаниями: Н+ + ОН- ® Н2О.
Методы кислотно-основного титрования позволяют определять концентрации растворов (и, следовательно, количество в смесях) неорганических и органических кислот и оснований и некоторых солей, подвергающихся гидролизу или реагирующих с кислотами и основаниями.
При кислотно-основном титровании реакция среды в момент эквивалентности - точка эквивалентности (т.е. когда кислота полностью прореагировала, а избытка щелочи еще нет) может быть нейтральной, кислой или щелочной в зависимости от природы вступающих в реакцию нейтрализации кислоты и основания. Продуктами реакции между сильной кислотой и сильным основанием являются соль, не подвергающаяся гидролизу, и вода: HCl + NaOH = NaCl + H2O.
В этом случае раствор в точке эквивалентности имеет нейтральную реакцию, т.е. рНт.э.=7. Фиксирование точки эквивалентности в кислотно-основном титровании проводят с помощью химических индикаторов или физико-химическими методами. Индикаторы кислотно-основного титрования - это сложные органические вещества, которые способны изменять свою окраску в зависимости от рН раствора.
Согласно ионной (протолитической) теории, кислотно-основные индикаторы, которые в растворах могут существовать в ионизированной и неионизированной формах. Эти формы окрашены в разный цвет и находятся в равновесии, зависящем от рН среды (HInd (окраска 1)« H+ + Ind- (окраска 2)).
Хромофорная теория кислотно-основных индикаторов связывает изменение их окраски с изменением строения индикаторов в результате внутримолекулярной перегруппировки.
Физико-химические методы определения точки эквивалентности основаны на анализе изменения свойств раствора в процессе титрования, например изменения рН среды в потенциометрическом методе, электрической проводимости раствора в кондуктометрическом, оптических свойств в фотометрии и спектрофотометрии, силы тока, проходящего через раствор, в амперометрическом методе и др.
В химическом анализе используется йодометрия. Иодометрияметод окислительно-восстановительного анализа, при котором о количестве определяемого вещества судят по количеству поглощенного или выделенного йода. В йодометрии в качестве окислителя выступает элементарный йод, способный вступать в реакцию с некоторыми восстановителями, стандартный потенциал которых отрицательнее потенциала окислительно-восстановительной реакции:I2 + 2e– = 2I– , Е = 0,54 В.
Вещества, окислительно-восстановительный потенциал которых больше 0,54 В, будут являться окислителями по отношению к иону йода и в данном случае будет выделяться элементарный йод. В качестве индикатора в йодометрии используется раствор крахмала.
Физико-химические методы количественного анализа позволяют определять состав вещества, не прибегая к использованию химикатов, т.е. когда химические реакции не протекают.
Методы анализа, основанные на наблюдении физических явлений, происходящих при протекании определенных химических реакций, называют физико-химическими методами. Наибольшее распространение среди физико-химических методов нашли методы колориметрии, потенциометрического титрования, кулонометрии и хроматорграфии.
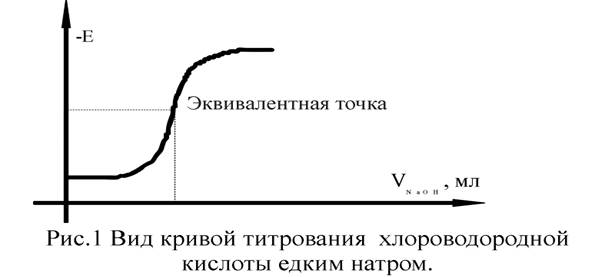
Сущность метода потенциометрического титрования заключается в том, что эквивалентную точку определяют не по изменению цвета индикатора, а по изменению потенциала электрода. Электрод, которым пользуются при потенциометрическом титровании для определения точки эквивалентности, носит названия индикаторного. Индикаторный электрод должен быть обратим по отношению к титруемому веществу или к ионам прибавляемого реагента. В зависимости от того, является ли электрод обратим по отношению к ионам реагента или титруемого вещества, потенциал его по мере титрования будет изменяться согласно уравнению:
E = Eом + 0,059/z lg[M+z]
или для водородного электрода E = Eон + 0,03 lg[Н+]
где Ео – стандартный потенциал электрода при концентрации иона металла или иона водорода равном 1. В данном уравнении принято, что коэффициент активности металла равен 1.
Потенциометрический метод титрования используется для количественного определения содержания в растворе кислот (метод нейтрализации), галогенов (метод осаждения) и ряда других ионов (метод комплексообразования).
Колориметрия или колориметрический анализ основан на определении концентрации вещества по интенсивности окраски раствора или на переводе определяемой части анализируемого объекта в окрашенное соединение. Для окраски исследуемого вещества используются как органические, так и неорганические реагенты
Из оптических методов анализа наиболее широкое распространение нашли колориметрические методы, основанные на измерении интенсивности светового потока, прошедшего через окрашенный раствор. В колориметрии используется, как правило, длина воды от 400 до 750 нм.
Зависимость между интенсивностью прошедшего света через раствор (J) и концентрацией окрашенного вещества (с), толщиной светопоглощающего раствора (l) и интенсивностью падающего на раствор света (Jo) носит название закона Бугера-Ламберта-Бера и выражается уравнением: D = lgJo/J = e c l, (где e - коэффициент поглощения света, постоянная величина, характерная для каждого окрашенного вещества и зависящая от его природы).
Величина lgJo/J является важной характеристикой окрашенного раствора, ее называют оптической плотностью раствора (D). Из всего этого следует, что оптическая плотность раствора прямо пропорциональна концентрации окрашенного вещества и толщине слоя раствора. Данное соотношение справедливо для разбавленных концентраций растворов (меньше 0,01 М). При более высоких концентрациях закон Бугера-Ламберта-Бера не соблюдается, вследствие взаимного влияния частиц на их способность поглощать свет. Закон Бугера-Ламберта-Бера справедлив для монохроматического излучения, тогда как при использовании светофильтра с достаточно широкой областью пропускания наблюдается отклонение от прямолинейности.
Определение концентрации окрашенного вещества методом фотоколориметрии производят методом сравнения оптических плотностей стандартного и исследуемого растворов, методом построения градуировочного графика и методом добавок.
