Реальные газы. Уравнение Ван-дер-Ваальса.
Основное уравнение молекулярно-кинетической теории. Средняя кинетическая энергия молекул, молекулярно-кинетический смысл температуры.





Идеальный газ в поле силы тяжести. Барометрическая формула. Распределение Больцмана.
 Для идеального газа, имеющего постоянную температуру T и находящегося в однородном поле тяжести (во всех точках его объёма ускорение свободного падения g одинаково), барометрическая формула имеет следующий вид:
Для идеального газа, имеющего постоянную температуру T и находящегося в однородном поле тяжести (во всех точках его объёма ускорение свободного падения g одинаково), барометрическая формула имеет следующий вид:
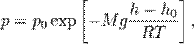 где p — давление газа в слое, расположенном на высоте h, p0 — давление на нулевом уровне (h = h0), M — молярная масса газа, R — газовая постоянная, T — абсолютная температура.
где p — давление газа в слое, расположенном на высоте h, p0 — давление на нулевом уровне (h = h0), M — молярная масса газа, R — газовая постоянная, T — абсолютная температура.
Барометрическая формула позволяет найти атмосферное давление в зависимости от высоты или измерив давление найти высоту. Идеальный газ — модель, в которой пренебрегают потенциальной энергией взаимодействия молекул. Между молекулами не действуют силы притяжения, соударения частиц между абсолютно упругие, время взаимодействия между молекулами пренебрежимо мало.
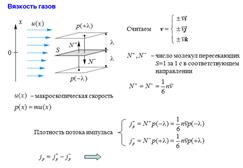
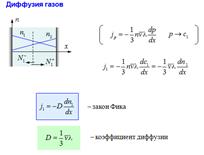
Явления переноса. Вязкость, теплопроводность и диффузия газов.
Явление переноса – необратимый процесс, в результате которого происходит пространственный перенос энергии, массы и импульса. Теплопроводность – обусловлена переносом энергии, диффузия – переносом массы. Вязкость – переносом импульса.




Первое начало термодинамики. Применение его для различных процессов.
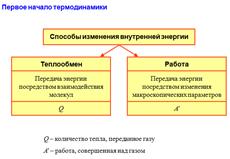
Количество теплоты, полученное системой, идёт на изменение её внутренней энергии и совершение работы против внешних сил. Первое начало термодинамики: при изобарном процессе 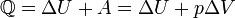
при изохорном процессе (A = 0) 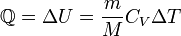
при изотермическом процессе (ΔU = 0) 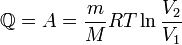
Здесь 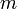 — масса газа,
— масса газа, 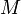 — молярная масса газа,
— молярная масса газа, 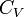 — молярная теплоёмкость при постоянном объёме,
— молярная теплоёмкость при постоянном объёме, 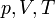 — давление, объём и температура газа соответственно, причём последнее равенство верно только для идеального газа.
— давление, объём и температура газа соответственно, причём последнее равенство верно только для идеального газа.

Изопроцессы, изопроцессы идеального газа.
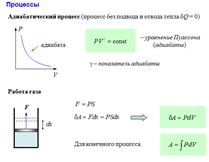


Изопроцессы — термодинамические процессы, во время которых количество вещества и ещё одна из физических величин — параметров состояния: давление, объём или температура — остаются неизменными.
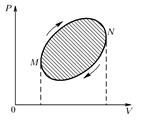 14. Круговые процессы. Тепловой двигатель. Цикл Карно и теорема Карно.
14. Круговые процессы. Тепловой двигатель. Цикл Карно и теорема Карно.



Реальные газы. Уравнение Ван-дер-Ваальса.
 Реальный газ — газ, который не описывается уравнением состояния идеального газа Клапейрона — Менделеева. Зависимости между его параметрами показывают, что молекулы в реальном газе взаимодействуют между собой и занимают определенный объём.
Реальный газ — газ, который не описывается уравнением состояния идеального газа Клапейрона — Менделеева. Зависимости между его параметрами показывают, что молекулы в реальном газе взаимодействуют между собой и занимают определенный объём.


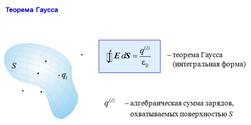
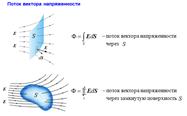
18. Поток вектора E. Теорема Гаусса для вектора E (в интегральной и дифференциальной формах).



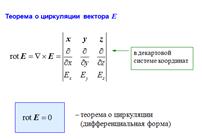
 20. Циркуляция вектора E. Теорема о циркуляции вектора E (в дифференциальной и интегральной формах). Потенциал. Потенциал точечного заряда и системы зарядов.
20. Циркуляция вектора E. Теорема о циркуляции вектора E (в дифференциальной и интегральной формах). Потенциал. Потенциал точечного заряда и системы зарядов.




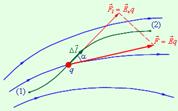
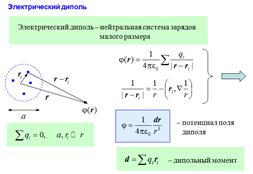 22. Электрический диполь. Электрический момент диполя. Поле диполя. Сила и момент сил, действующие на диполь в электрическом поле.
22. Электрический диполь. Электрический момент диполя. Поле диполя. Сила и момент сил, действующие на диполь в электрическом поле.


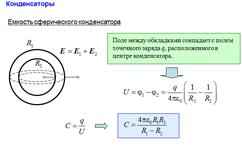
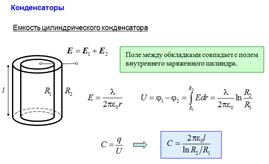
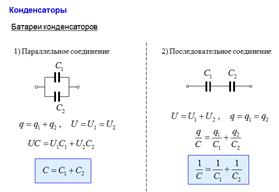
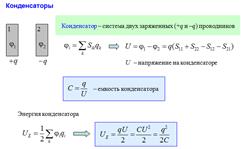 24. Конденсаторы. Емкость и энергия конденсатора. Емкость плоского, цилиндрического и сферического конденсаторов. Последовательное и параллельное соединение конденсаторов.
24. Конденсаторы. Емкость и энергия конденсатора. Емкость плоского, цилиндрического и сферического конденсаторов. Последовательное и параллельное соединение конденсаторов.
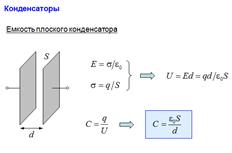

 26. Вектор электрической индукции. Теорема Гаусса для вектора электрической индукции (в интегральной и дифференциальной формах). Граничные условия на границе раздела двух диэлектриков.
26. Вектор электрической индукции. Теорема Гаусса для вектора электрической индукции (в интегральной и дифференциальной формах). Граничные условия на границе раздела двух диэлектриков.




 28. Закон Ома для однородного и неоднородного участка цепи (в дифференциальной и интегральной формах).
28. Закон Ома для однородного и неоднородного участка цепи (в дифференциальной и интегральной формах).

закон Ома для однородного участка цепи: сила тока в проводнике прямо пропорциональна приложенному напряжению и обратно пропорциональна сопротивлению проводника. 


 30. Работа сил электрического поля. Закон Джоуля-Ленца (в дифференциальной и интегральной формах).
30. Работа сил электрического поля. Закон Джоуля-Ленца (в дифференциальной и интегральной формах).
При перемещении пробного заряда q в электрическом поле электрические силы совершают работу. Работа сил электростатического поля при перемещении заряда из одной точки поля в другую не зависит от формы траектории, а определяется только положением начальной и конечной точек и величиной заряда. 

 32. Классическая электронная теория металлов. Основные положения и обоснование законов Ома и Джоуля-Ленца. Затруднения теории.
32. Классическая электронная теория металлов. Основные положения и обоснование законов Ома и Джоуля-Ленца. Затруднения теории.


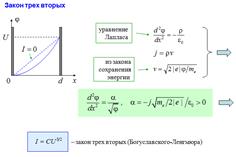
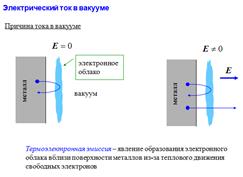 34. Электрический ток в вакууме. Термоэлектронная эмиссия. Формула Ричардсона-Дешмана. Закон “трех вторых”.
34. Электрический ток в вакууме. Термоэлектронная эмиссия. Формула Ричардсона-Дешмана. Закон “трех вторых”.