Потенциометрическое титрование
Потенциометрическое титрование чаще всего используют в титриметрическом анализе для определения точки эквивалентности. При потенциометрическом титровании концентрация (активность) участвующих веществ или ионов все время изменяется, следовательно, изменяется и равновесный потенциал электрода.
1. интегральная кривая
Если построить график в координатах Е= f (Vтитр), то получится кривая отражающая динамику процесса титрования с резким изменением потенциала в точке эквивалентности. Резкое изменение потенциала (скачка титрования) в точке эквивалентности или вблизи нее даст возможность найти эквивалентную точку титрования. На точку эквивалентности четко будет указывать вертикальный участок кривой титрования (рис. 15)
2. дифференциальная кривая
2.1 В отдельных случаях кривая получается размытой и точка эквивалентности отчетливо не просматривается. В этом случае рекомендуется пользоваться дифференциальной потенциометрической кривой, которая строится в координатах 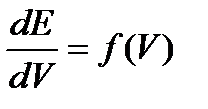 , где
, где 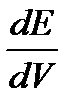 - изменение потенциала электрода между двумя порциями добавленного раствора, а V порция добавленного рабочего раствора титранта.
- изменение потенциала электрода между двумя порциями добавленного раствора, а V порция добавленного рабочего раствора титранта.
Точка эквивалентности определяется как точка максимума на кривой.
2.2 Метод гранка. Его отличие от предыдущего метода, в том, что титруют очень разбавленные растворы.
2.3
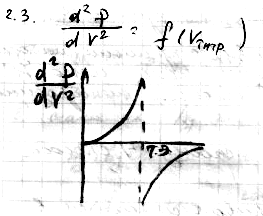
Общая характеристика метода:
+ высокая чувствительность; высокая точность; возможность титрования предельно разбавленных растворов; возможность одновременного определения нескольких веществ; можно проводить титрование в мутных и окрашенных растворах; титрование неводных растворов а также титрование малорастворимых соединений и растворимых в воде; возможность автоматизации процесса;
‒ большое число отсчетов; небыстрая установка ЭДС.
Потенциометрическое титрование проводят по реакциям:
- нейтрализации,
- окисления-восстановления,
- осаждения,
- комплексообразования.
В качестве электрода сравнения применяется хлорсеребрянный электрод.
Кислотно-основное титрование.
Кривые титрования по реакции нейтрализации являются изображением зависимости величины рН или Е от объема прилитого титранта. Вид кривой зависит от природы титруемого вещества и титранта.
Четкость определения Т.Э. зависит от силы электролита. Расчет кривых титрования по методу нейтрализации проводится по соответствующим формулам до Т.Э, в Т.Э. и после Т.Э.
В кислотно-основном титровании в качестве индикаторного обычно используют стеклянный электрод, как правило, входящий в комплект серийно выпускаемых промышленностью рН-метров. Потенциометрический метод позволяет провести количественное определение компонентов в смеси кислот, если константы диссоциации различаются не менее чем на три порядка, при этом будет наблюдаться несколько скачков титрования.
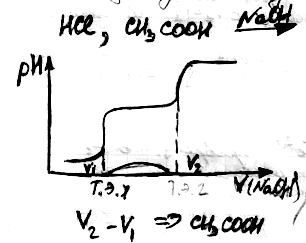
Например, при титровании смеси, содержащей хлорводородную и уксусную кислоты, на кривой титрования обнаруживается два скачка. Первый скачок свидетельствует об окончании титрования HCl, второй скачок наблюдается при оттитровывании уксусной кислоты.
Окислительно-восстановительное титрование.
В окислительно- восстановительных реакциях потенциал платинового индикаторного электрода зависит от соотношения концентрации окисленной и восстановленной формы.
Изменение потенциала платинового электрода можно проследить на примере титрования соли железа II бихроматом калия в кислой среде:
6FeSO4 + K2Cr2O7 + 7H2O ® 3Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 +7H2O
- до Т.Э. по мере прибавления раствора K2Cr2O7 будет уменьшаться концентрация [Fe2+] и увеличиваться [Fe3+]
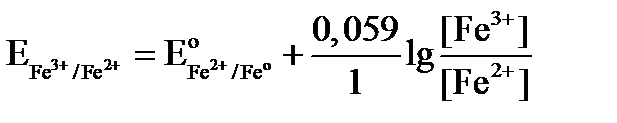 (потенциал возрастает)
(потенциал возрастает)
- после Т.Э. все Fe2+ превращаются Fe3+ и сопряженная пара исчезает и пояпляется вторая сопряженная пара Cr3+ и Cr2O72-
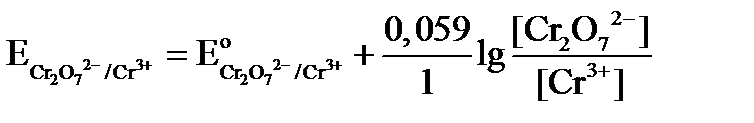 (потенциал возрастает)
(потенциал возрастает)
- в Т.Э
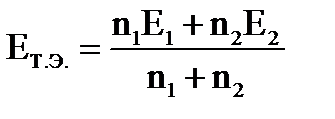
где n – число перенесенных электронов
Титрование по методу осаждения.
Индикаторными электродами в методах потенциометрического титрования, использующих реакции осаждения, служат металлические или мембранные электроды, чувствительные к определяемому иону или иону-осадителю.
Потенциометрические кривые в этих случаях будут выглядеть:

Практически по методу осаждения могут быть определены катионы серебра, ртути, цинка, свинца, анионы хлора, брома, йода и некоторые другие.
Смесь галогенидов при их совместном присутствии может быть оттитрована без разделения нитратом серебра на серебряном электроде. В это случае, на кривой титрования будет столько скачков, сколько анионов содержится в растворе. Порядок расположения скачков зависит от величины ПР галогенидов серебра. Так, например, если в растворе содержится хлор и бром, то оттитровываться сначала будет бром, т.к. ПР(AgBr)=5,3*10-7, а затем хлор, т.к. ПР(AgCl)=1,8*10-10
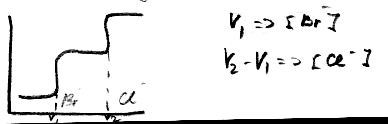
Расчет кривых титрования по реакции осаждения производится следующим образом
Рассмотрим случаи титрования AgNO3 раствором хлорида.
- До Т.Э. в растворе присутствует Ag+ в паре с серебряным электродом, образуется электрод первого рода, тогда:
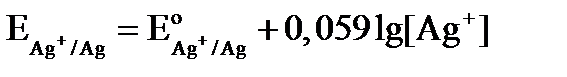
- В Т.Э. все ионы серебра оказываются оттитрованными:
Ag+ + Cl- = AgCl↓
ПР = [Ag+] [Cl-] отсюда следует 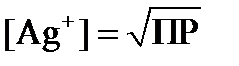
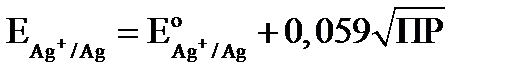
- После Т.Э. реакции начинает накапливаться кроме уже имеющегося AgCl анионы хлора:
Ag│AgCl, Cl-
Т. е. образуется электрод второго рода
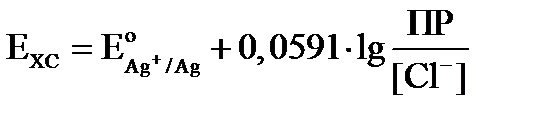
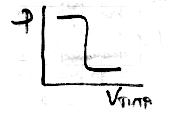
При обратном титровании расчет будет обратный и кривая титрования будет иметь вид:
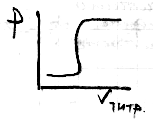
Комплексонометрическое титрование.
Потенциометрическое титрование катионов комплексоном III (ЭДТА) можно проводить с использованием в качестве индикаторного электрода соответствующего металла: титрование солей меди с медным электродом, солей цинка – с цинковым и т.д. или подходящего ионоселективного электрода.
Определение ионов серебра, например, можно производить используя реакцию комплексообразования еребра с цианид ионами:
CN- + Ag+ Û[Ag(CN)2]-
Процесс комплексообразования обратим, константа нестойкости этого комплекса равна:
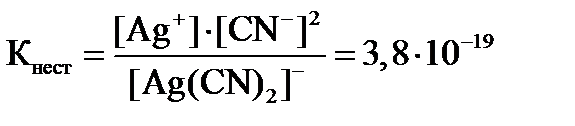
При титровании цианида калия нитратом серебра ионы серебра расходуются на образование комплексного иона Û[Ag(CN)2]- и их концентрацию, их можно определить по формуле:
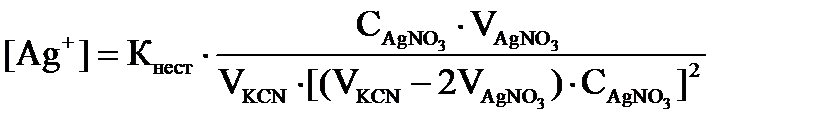
где 2 – число лигандов.
Потенциал определяется по уравнению:
Е = 0,80 + 0,058× lg[Ag+]. (28)
В точке эквивалентности цианид-ионы будут связаны в комплексе. Учитывая, что при диссоциации комплекса существует соотношение 2[Ag+] = [CN-].
Подставляя это значение в уравнение константы равновесия получаем:
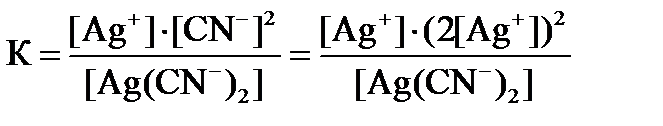 .
.
Откуда:
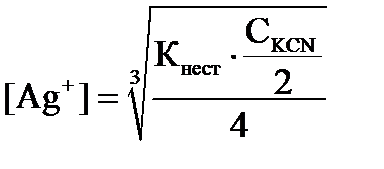
Далее потенциал определяется по формуле (28).
Характерно, что после прохождения точки эквивалентности наблюдается образование малорастворимого осадка и потенциал определяется произведением растворимости образующейся соли, но, как правило, он остается постоянным до тех пор, пока весь комплекс не превратится в осадок.
