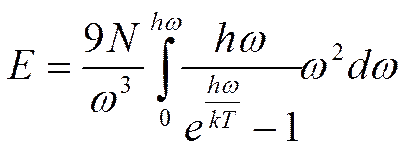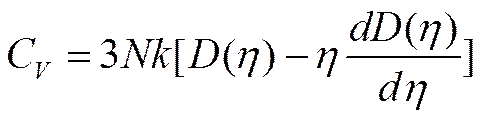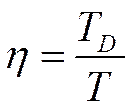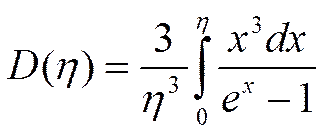Физический признак кристаллов.
В зависимости от рода частиц, расположенных в узлах кристаллической решетки, и характера сил взаимодействия между ними кристаллы разделяются на четыре типа: ионные, атомные, металлические, молекулярные.
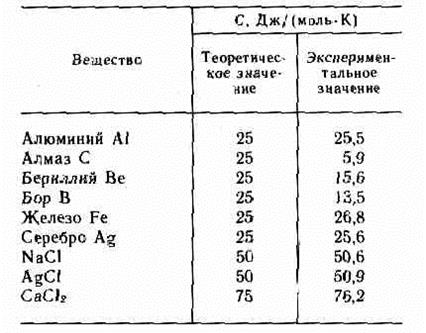
Ионные кристаллы.В узлах кристаллической решетки располагаются поочередно ионы противоположного знака. Типичными ионными кристаллами являются большинство галоидных соединений щелочных металлов (NaCl, CsCl, KBr и т.д.), а также оксидов различных элементов (MgO, CaO и т.д.). Силы взаимодействия между ионами являются в основном электростатическими (кулоновскими). Связь,обусловленная кулоновскими силами притяжения между разноименно заряженными ионами, называется ионной.
Атомные кристаллы.В узлах кристаллической решетки располагаются нейтральные атомы, удерживающиеся в узлах решетки ковалентными, связямиквантово-механического происхождения (у соседних атомов обобществлены валентные электроны, наименее связанные с атомом). Атомными кристаллами являются алмаз и графит (два различных состояния углерода), некоторые неорганические соединения (ZnS, BeO и т.д.), а также типичные полупроводники — германий Ge и кремний Si.
Валентные связи осуществляются парами электронов, движущихся по орбитам, охватывающим оба атома, и носят направленный характер: ковалентные силы направлены от центрального атома к вершинам тетраэдра. В отличие от графита решетка алмаза не содержит плоских слоев, что не позволяет сдвигать отдельные участки кристалла, поэтому алмаз является прочным соединением.
Металлические кристаллы.В узлах кристаллической решетки располагаются положительные ионы металла. При образовании кристаллической решетки валентные электроны, сравнительно слабо связанные с атомами, отделяются от атомов и коллективизируются: они уже принадлежат не одному атому, как в случае ионной связи, и не паре соседних атомов, как в случае гомеополярной связи, а всему • кристаллу в целом. Действительно, большинство металлов имеют кубическую объемно центрированную (Li, Na, К, Rb, Cs) и кубическую гранецентрированную (Cu, Ag, Pt, Au) решетки. Чаще всего металлы встречаются в виде поликристаллов.
Молекулярные кристаллы.В узлах кристаллической решетки располагаются нейтральные молекулы вещества, силы взаимодействия между которыми обусловлены незначительным взаимным смещением электронов в электронных оболочках атомов. Эти силы называются ван-дер-ваальсовыми, так как они имеют ту же природу, что и силы притяжения между молекулами, приводящими к отклонению газов от идеальности. Молекулярными кристаллами являются, например, большинство органических соединений (парафин, спирт, резина и т. д.), инертные газы (Ne, Ar, Kr, Хе) и газы СО2, О2, N2 в твердом состоянии, лед.
Теплоемкость твердых тел
В качестве модели твердого тела рассмотрим правильно построенную кристаллическую решетку, в узлах которой частицы (атомы, ионы, молекулы), принимаемые за материальные точки, колеблются около своих положений равновесия — узлов решетки — в трех взаимно перпендикулярных направлениях. Таким образом, каждой составляющей кристаллическую решетку частице приписывается три колебательных степени свободы, каждая из которых, согласно закону равнораспределения энергии по степеням свободы (см. § 50), обладает энергией kT.
Внутренняя энергия моля твердого тела
Um = 3NАkT = 3RT,
где NА — постоянная Авогадро; NAk=R (R — молярная газовая постоянная).
Молярная теплоемкость твердого тела
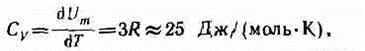
т. е. молярная (атомная) теплоемкость химически простых тел в кристаллическом состоянии одинакова (равна 3R) и не зависит от температуры. Этот закон был эмпирически получен французскими учеными П. Дюлонгом (1785—1838) и Л. Пти (1791 —1820) и носит название закона Дюлонга и Пти.
Если твердое тело является химическим соединением (например, NaCl), то число частиц в моле не равно постоянной Авогадро, а равно nNA, где n — число атомов в молекуле (для NaCl число частиц в моле равно 2Nа, так, в одном моле NaCl содержится NA атомов Na и NA атомов Cl). Таким образом, молярная теплоемкость твердых химических соединений
CV = 3pR»25n Дж/(моль•К),
т. е. равна сумме атомных теплоемкостей элементов, составляющих это соединение.
По Эйнштейну:
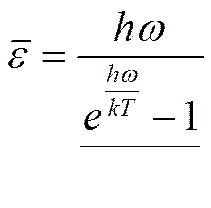
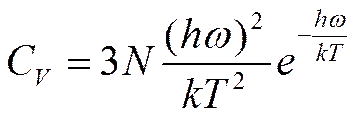
По Дебаю: