Растворы неэлектролитов и электролитов
МУРМАНСКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ
Кафедра химии
Контрольная работа №2
РАСТВОРЫ НЕЭЛЕКТРОЛИТОВ И ЭЛЕКТРОЛИТОВ
по курсу «Химия»
Мурманск
Контрольная работа 2
Растворы неэлектролитов и электролитов
Вариант 1
1. Определите молярную концентрацию раствора, полученного при смешивании 200 мл 8М и 300 мл 2М растворов серной кислоты.
2. К водному раствору слабого электролита ЭCl2 добавили сильного электролита BaCl2. Как это влияет на значение константы и степени электролитической диссоциации ЭCl2. Дайте аргументированные ответы.
3. Определите значение рОН и рН водного раствора электролита, если концентрация ионов гидроксида 10-2 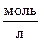 .
.
4. В каком из растворов концентрация ионов Pb2+ наименьшая: Pb(OH)2, PbCl2 или PbI2? Почему?
5. Закончите составление уравнений реакций:
SnSO4 + K2CO3 + H2O ®
FeCl3 + CH3COOK + H2O ®
6. Какова реакция водного раствора нитрата меди (II): слабокислая, нейтральная, слабощелочная, сильнощелочная? Составьте ионно-молекулярное и молекулярное уравнения гидролиза Cu(NO3)2.
Контрольная работа 2
Растворы неэлектролитов и электролитов
Вариант 2
1. В растворе объёмом 250 мл содержится сульфат алюминия массой 7,5 г. Чему равна молярная концентрация и молярная концентрация эквивалента этого раствора?
2. Можно ли осуществить следующие реакции:
BaCO3¯ + CaCl2 ® CaCO3¯ + BaCl2
AgI¯ + KBr ® AgBr¯ + KI
3. Раствор циановодорода HCN имеет рН < 7. Постепенно в него добавляют цианид калия и констатируют, что среда становится менее кислой, затем нейтральной и, наконец, щелочной (рН < 7). Объясните результаты опыта.
4. Раствор, содержащий 2,1 г КОН в 250 мл воды, замерзает при –0,519°С. Найдите для этого раствора изотонический коэффициент. Криоскопическая постоянная воды К=1,86.
5. Какая из солей в большей степени подвергается гидролизу (при одинаковой концентрации растворов): NH4Cl; СH3COONa; K2S; Rb2CO3? Почему? Напишите молекулярное и ионные уравнения гидролиза Rb2CO3 по первой ступени.
6. Вычислите рН раствора 0,1М уксусной кислоты, если степень диссоциации составляет 1%.
Контрольная работа 2
Растворы неэлектролитов и электролитов
Вариант 3
1. Какой объём 10% – ного раствора гидроксида калия (r = 1,08 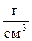 ) можно приготовить из 15 г КОН?
) можно приготовить из 15 г КОН?
2. Определите рОН и рН раствора, в котором концентрация гидроксид-ионов равна 1,5×10-9 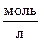 .
.
3. К насыщенному раствору AgBr, находящемуся в равновесии с осадком, добавили раствор NaCl. Какие явления будут наблюдаться? Почему?
4. При какой концентрации раствора степень диссоциации азотистой кислоты HNO2 будет равна 0,2?
5. В растворе каких солей краснеет лакмусовая бумажка: KCl; ZnSO4; Cu(NO3)2; K2CO3? Напишете молекулярное и ионно-молекулярное уравнения гидролиза соли Cu(NO3)2.
6. Температура кристаллизации одномолярных растворов циановодорода HCN и глюкозы C6H12O6 близки. Какой вывод можно сделать относительно степени диссоциации HCN: а) a близка к 1; б) a близка к 0? Почему?
Контрольная работа 2
Растворы неэлектролитов и электролитов
Вариант 4
1. Какой объём 30% - ного раствора гидроксида калия (r = 1,286 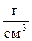 ) нужно взять, чтобы приготовить 2 л 10% - ного раствора КОН (r = 1,082
) нужно взять, чтобы приготовить 2 л 10% - ного раствора КОН (r = 1,082 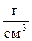 ).
).
2. В 0,05 кг воды растворено 0,006 кг неэлектролита. Определите молярную массу ( 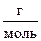 ) неэлектролита, если раствор замерзает при – 3,72°С. Криоскопическая постоянная воды К = 1,86.
) неэлектролита, если раствор замерзает при – 3,72°С. Криоскопическая постоянная воды К = 1,86.
3. Определите концентрацию катионов водорода ( 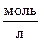 ), если рН раствора 10.
), если рН раствора 10.
4. Не проводя вычислений, расположите вещества в порядке увеличения их растворимости в воде: Ag2CO3; Ag2SO4; Ag2CrO4. Ответ аргументируйте справочными данными.
5. Вычислите константу диссоциации циановодородной кислоты HCN, если степень диссоциации её в 0,01М растворе равна 2,83×10-4.
6. При гидролизе каких солей образуется H2S и HCN? Приведите уравнения гидролиза этих солей.
Контрольная работа 2
