Занятие № 6 Тема: «Растворы. Законы растворимости. Растворы электролитов. Теории кислот и оснований. Коллигативные свойства растворов. Диффузия. Осмос».
1. Вопросы для обсуждения:
1. Растворы. Вода как растворитель. Аномальные свойства воды.
2. Растворимость. Факторы, влияющие на растворимость. Термодинамические процессы при растворении.
3. Механизм растворения ионных и молекулярных веществ. Сольватация. Гидратация.
4. Растворимость газов в жидкостях. Законы Генри, Сеченова, Дальтона, их биологическое значение.
5. Понятие об электролитах. Электролитный баланс в организме человека. Основные положения теории электролитической диссоциации.
6. Теории кислот и оснований (Аррениуса, Брёнстеда-Лоури, Льюиса).
7. Коллигативные свойства разбавленных растворов. Диффузия.
8. Осмос, осмотическое давление. Закон Вант-Гоффа для разбавленных растворов электролитов и неэлектролитов. Изотонический коэффициент.
9. Поведение живой клетки в гипо-, гипер-, изотонических растворах (плазмолиз, гемолиз). Осмотическое давление крови, онкотическое давление.
10. Относительное понижение давления насыщенного пара растворителя над раствором. Первый закон Рауля.
11. Понижение температуры замерзания и повышение температуры кипения растворов по сравнению с растворителем. Второй закон Рауля.
12. Криометрия, эбулиометрия, их применение в медико-биологических исследованиях.
2. Ситуационные задачи:
Задача №1. Для промывания гнойных ран используется гипертонический раствор хлорида натрия. В 500 мл такого раствора содержится 9 г хлорида натрия. Рассчитать осмотическое давление раствора. Сделать вывод о процессе, происходящем с живой клеткой в данном растворе.
Решение:
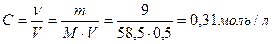
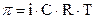
NаСl ↔ Na+ + Cl- 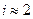
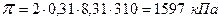 .
.
В гипертоническом растворе живая клетка подвергается плазмолизу.
Задача № 2. Рассчитать температуру кристаллизации (замерзания) 40% (по массе) раствора этилового спирта в воде? К(H2O) = 1,86 оС/m.
Решение
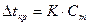 , где Сm - моляльная концентрация раствора.
, где Сm - моляльная концентрация раствора.
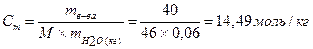 Þ
Þ 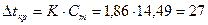 °С
°С
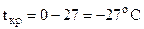
3. Решить самостоятельно:
1. Вычислить осмотическое давление 0,2 М растворов калий хлорида, кальций хлорида, мочевины. (t=250C)
2. Вычислить осмотическое давление 0,9% раствора NaCl и 5% раствора глюкозы. (t=370C)
3. Рассчитать осмотическое давление водного раствора фенола (используется для лечения воспаления среднего уха), в 100 мл которого, содержится 3 г. фенола.
4. При какой температуре замерзает 40% раствор этанола в воде?
5. При какой температуре нужно хранить 1% водный раствор новокаина, чтобы он не замерз? Мновокаина = 272,8 г\моль
6. Температура кипения 20% водного раствора дисахарида = 100,380С. Определить молекулярную массу растворённого вещества.
7. Определить температуру кипения раствора глюкозы, содержащего в 200 г. воды 50 г. глюкозы.
3. Тематика рефератов по учебно-исследовательской работе студентов (УИРС).
| 1. | Биологические жидкости организма человека. |
| 2. | Роль электролитов в физиологических процессах. |
| 3. | Медицинские аспекты процессов образования осадков. |
| 4. | Роль диффузии в процессах переноса веществ в биологических системах. |
| 5. | Роль осмоса и осмотического давления в биологических системах. Изотонические, гипотонические, гипертонические растворы. |
