Методы определения порядка реакции. 1) Реакцию димеризации 2А(г) ® В(г) контролировали измерением общего давления в зависимости от времени
(Домашнее задание №2)
Вариант 20.
1) Реакцию димеризации 2А(г) ® В(г) контролировали измерением общего давления в зависимости от времени. Были получены следующие результаты:
| t ,с | |||||
| Р, мм рт. ст. |
Определите порядок реакции (n) и вычислите k.
2) Для необратимой реакции А(г) ® В(г) была получена следующая зависимость времени превращения А на 30% от начального давления вещества:
| Р0, Па | ||||
| t30% , мин | 10,8 | 7,5 | 5,3 | 3,7 |
Определите по этим данным порядок реакции и размерность константы этой реакции?
3) Для реакции 2NO + Cl2 ® 2NOCl при Т = 400 К были получены следующие данные:
| № опыта | Давление в мм рт. ст. | Скорость w=-d[NOCl]/dt, моль/см3×с | |
| NO | Cl2 | ||
| 1,0 | 2,0 | 3,8·10-14 | |
| 3,0 | 1,0 | 3,96·10-13 | |
| 2,0 | 2,0 | 3,52·10-13 |
Найдите k и порядок по NO и Cl2.
4) Реакция первого порядка проходит на 30% за 30 мин. Какова скорость реакции (моль/л×час) при концентрации реагирующего вещества 0,01 моль/л?
Методы определения порядка реакции
(Домашнее задание №2)
Вариант 21.
1) Реакцию сульфирования бензола оксидом серы (VI) С6Н6 + SO3 ® C6H5-SO3H изучали следующим образом. Вначале концентрация SO3 поддерживалась постоянной и определялось изменение со временем содержание бензола в смеси (табл.1):
| t ,с | ||||||
| С (С6Р6), усл.ед. | 24,5 | 17,2 |
Затем поддерживалась постоянной концентрация бензола и оценивалось уменьшение в 3 раза концентрация SO3. Полученные результаты представлены в табл.2:
| С (SO3), усл.ед. | ||||||
| t1/2, мин | 75,5 |
Каким кинетическим уравнением описывается реакция сульфирования бензола?
2) Реакция первого порядка проходит на 20,5% за 46 мин. Сколько моль исходного вещества вступит в реакцию по прошествии двух часов, если начальная концентрация С0 = 0,5 моль/л, а объем раствора 15 л?
3) Для реакции газофазного гидрирования ацетилена при 788 К получены данные, сведенные в таблицу:
| № опыта | Давление в мм рт. ст. | Скорость w = dР/dt×103, мм рт.ст./с | |
| С2Н2 | Н2 | ||
| 0,887 | |||
| 1,850 | |||
| 2,590 |
Вычислите k и порядок реакции по С2Н2 и Н2.
Методы определения порядка реакции
(Домашнее задание №2)
Вариант 22.
1) Определите порядок реакции: 2А(г) ® 2В(г) + С(г) и вычислите константу скорости, если общее давление реакционной смеси изменилось следующим образом:
| t, мин | |||||
| P, Па |
2) При взаимодействии эквивалентных количеств брома с этиленом, протекающей в тетрахлорметане по реакции С2Н4 + Br2 ® C2H2Br2 ,была установлена следующая зависимость времени уменьшения концентрации брома в 2 раза от исходной (С0).
| С0, Br2, моль/л | 0,05 | 0,03 | 0,02 | 0,01 |
| t1/2 , мин | 32,50 | 54,44 | 81,94 | 163,89 |
Определить n и k. Какова будет концентрация этилена через 3 час от начала реакции?
3) При дегидрировании н-бутилена до дивинила при Т = 873 К и различных начальных давлениях бутилена (P0) были получены следующие значения начальной скорости (w0):
| w0, моль/ч | 0,0262 | 0,0210 | 0,0175 |
| Р×10-2, Па | 88,25 | 46,25 | 31,60 |
Определите порядок реакции.
4) Разложение оксида азота (V) в газовой фазе протекает по уравнению реакции 2N2О5 ® 2N2О4 + О2 и описывается кинетическим уравнением 1-го порядка. Константа скорости этой реакции при 273 К равна 7,9×10-7 с-1. Исходное давление N2О5 равно 3333 Па. Вычислите, за какое время давление в смеси газообразных веществ достигнет 3733 Па?
Методы определения порядка реакции
(Домашнее задание №2)
Вариант 23.
1) Определите порядок реакции: 3А(г) ® А3(тв). Давление исходного вещества в одном опыте упало с 0,252×105 Па до 0,205×105 за 30 часов, а в другом опыте, который проводился в том же сосуде и при той же температуре, с 0,105×105 до 0,102×105 Па за 21 час.
2) Для реакции разложения этиленоксида при 687 К по уравнению: С2Н4О ® CH4 + СО, были получены следующие результаты:
| t, мин | |||||
| Общ. давление P×10-2, Па | 155,33 | 163,46 | 167,59 | 171,59 | 177,59 |
Определить n и k. Какое давление будет в реакционной смеси через 1 час от начала реакции?
3) Используя следующие данные, определите порядок реакции разложения оксида азота (I):
| Р0×10-2, Па | 57,60 | 105,33 | 193,00 |
| t1/2 , с |
4) Реакция в смеси двух газов А и В при 2300 С протекает по закону порядка 3/2 для А и нулевого порядка для В. Начальные давления газа А 15,7 мм рт.ст. За 1 час после начала опыта в сосуде осталось 30% газа А. Определите константу скорости этой реакции.
Методы определения порядка реакции
(Домашнее задание №2)
Варианты 24.
1) Реакция термического разложения n-диоксана при 777 К протекает по уравнению:
(С2Н4)2О2 ® 2СО + Н2 + С2Н6
Изменение парциального давления диоксана со временем представлено в таблице:
| t ,мин | ||||||
| Р×10-3, Па | 106,64 | 95,98 | 89,31 | 81,31 | 65,32 | 42,66 |
Определите по этим данным порядок реакции графическим и аналитическим способами. Каково будет парциальное давление диоксана и общее давление в реакционной смеси через 15 мин после начала реакции?
2) При взаимодействии эквивалентных количеств брома и этилена наблюдалась следующая зависимость времени полупревращения этилена от его исходной концентрации (с0).
| с0, моль/л | 0,05 | 0,03 | 0,02 | 0,01 |
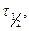 мин мин | 3266,7 | 4916,7 | 9833,3 |
3) Определите порядок реакции NO с водородом 2NO + 2H2 ® N2 + 2H2O, если начальная скорость реакции зависит от состава смеси следующим образом:
| w0 ×106, моль/л×с | 1,2 | 4,8 | 2,4263 |
| Р(О2), мм рт.ст. | |||
| Р(NО), мм рт.ст. |
4) Константа скорости реакции омыления уксусно-этилового эфира щелочью при 283 К равна 2,38 л×моль-1×мин-1. Рассчитайте время половинного разложения эфира, если 1 л 0,05 н раствора эфира смешать с 1 л 0,1 н раствора щелочи. (Реакция подчиняется кинетическому уравнению 2-го порядка).
