Пример 2. Вычислите молярную концентрацию раствора сульфата калия, 20 мл которого содержат 1,74 г этой соли
Вычислите молярную концентрацию раствора сульфата калия,
20 мл которого содержат 1,74 г этой соли.
Решение.
Молярная концентрация указывает на количество молей вещества в 1000 мл раствора. Ее вычисляют по формуле, (моль/л):
См = 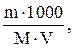 моль/л,
моль/л,
где m - масса растворенного вещества, г; М - молярная масса растворенного вещества, г; V - объем раствора, мл.
Молярная масса сульфата калия (К2SO4) равна:
39,10 + 32,06 + 4 · 16 = 174 г/моль.
Рассчитаем массу сульфата калия, содержащегося в 1 литре раствора, из соотношения:
в 20 мл раствора К2SO4 содержится 1,74 г К2SO4;
в 1000 мл - Х г К2SO4.
Тогда Х = 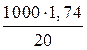 = 87 г.
= 87 г.
Молярная масса сульфата калия 174,26 г/моль, а 87 г этой соли составят
87 : 174,26 = 0,5 молей.
Итак, в 1 литре раствора сульфата калия содержится 0,5 молей этой соли. Следовательно, раствор 0,5 молярный (0,5 М). Эту же задачу можно решить по формуле
См = 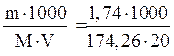 = 0,5моль/л.
= 0,5моль/л.
