Физиология поджелудочной железы.
ОСТРЫЙ ПАНКРЕАТИТ.
ОСТРЫЙ ПАНКРЕАТИТ – это воспалительно-дегенеративное поражение поджелудочной железы.
Актуальность проблемы.Самой сложной проблемой в неотложной хирургии органов брюшной полости является острый панкреатит ( ОП ). Отмечается неуклонный рост числа больных острым панкреатитом.
Они составляют 5-10% от общего числа пациентов хирургического профиля. В 15-20% наблюдений патологический процесс при остром панкреатите носит деструктивный характер. При панкреонекрозе у 40-70% больных происходит инфицирование очагов некротической деструкции. На инфекционные осложнения приходится до 80% причин смерти больных с деструктивным панкреатитом (В.С.Савельев и соавт. 2000).
Анатомия поджелудочной железы. Pancreas происходит от греческого слова pan – весь, creas – мясо. Это название железа получила за однородность по виду, цвету, консистенции. Эмбрионально железа развивается из эндодермальных выпячиваний первичной кишечной трубки, из которой образуется позже 12-перстная кишка, внепеченочные желчные пути.
Таким образом, эмбриональная общность кровообращения, лимфообращения, иннервации, а также особенности соединения протоковых систем печени и поджелудочной железы создают условия для распространения патологического процесса из одного органа на другой, что имеет чрезвычайно важное значение в понимании болезней гепатопанератодуоденльной зоны.
Поджелудочная железа располагается в собственно надчревной области и в левом подреберье. Различают головку, тело, хвост поджелудочной железы. Железа лежит в забрюшинном пространстве (рис. ) и окружена парапанкреатической клетчаткой, выраженность которой напрямую связана с питанием больного. Парапанкреатическая клетчатка является частью обширной забрюшинной клетчатки, которая состоит из параколярной, паранефральной, тазовой, поддиафрагмальной. Эти клетчаточные пространства рыхлые, отделены друг от друга непрочными соединительно-тканными перемычками, обильно пронизаны лимфатическими и кровеносными сосудами. Это способствует быстрому распространению процесса по забрюшинной клетчатке при ОП.
Одним из факторов, способствующих высокой летальности при панкреонекрозе является развивающаяся флегмона забрюшинной клетчатки.
На уровне переднего края тела поджелудочной железы находится корень брыжейки ободочной кишки. В связи с этим при панкреонекрозе в некротический процесс всегда вовлекается корень брыжейки, который у тучных больных представлен большим массивом жировой ткани. Эта омертвевающая ткань является источником эндогенной интоксикации, одним из компонентов развития и поддержания синдрома системного воспалительного ответа. Вовлечение в процесс сосудов и нервов, проходящих в корне брыжейки, приводит к парезу поперечно- ободочной кишки, что клинически проявляется её вздутием , а в случае развития тромбоза сосудов наступает некроз кишки. В силу своего анатомического положения ободочная кишка и её корень втягиваются в воспалительный инфильтрат при ОП.
Спереди от железы находится задняя стенка желудка, которая также, в силу своей анатомической близости, сразу вовлекается в воспалительный процесс. Она оносительно быстро (естетсвенная биологическая реакция) спаивается с жизнеспособными участками железы и отграничивает участки некроза от свободной брюшной полости. Таким образом, при инфицированном панкреонекрозе в поджелудочной железе образуется множество изолированных друг от друга гнойников. При доступе к ним с целью дренирования и некрсекветрэктомии всегда возникают значительные технические трудности и есть опасность ранения этих полых органов с последующим формированием желудочного и толстокишечного свищей. Участки желудка в воспалительном процессе клинически проявляется гастростазом. Вследствие микроциркуляторных расстройств, метаболических нарушений в стенке желудка, на его слизистой могут развиваться эрозии, острые язвы. ?????????
Головку поджелудочной железы подковообразно окружает 12- п.кишка которая также сразу же вовлекается в воспалительный процесс при остром панкреатите. Здесь возможно формирование дуоденальной непроходимости вследствие сужения её просвета, давящей увеличенной головкой поджелудочной железы и воспалительным инфильтратом. Возможно образование дуоденальных свищей при расплавлении стенки кишки гноем и активными ферментами ПЖ. Дуоденальный свищ представляет прямую угрозу жизни больного, вследствие возможного возникновения распространенного перитонита, а также в результате быстро развивающегося истощения и электролитных расстройств.
Поджелудочная железа обильно кровоснабжается. Головка - передневерхней, передненижней, задневерхней и задненижней поджелудочно- 12-перстными артериями; тело и хвост в основном селезеночной артерией. Отток венозной крови осуществляется по одноименным притокам воротной вены. Железа окружена большим количеством крупных артериальных и венозных сосудов.
К области головки прилежит нижняя полая вена, начальный отдел воротной вены. К области тела – верхние брыжеечные сосуды, аорта. По верхнему краю железы проходит селезеночная артерия, по нижнему – одноименная вена.
При инфицированном панкреонекрозе длительный гнойный процесс может разъесть крупные сосуды и тогда развивается жизненно опасное аррозивное кровотечение, от которого многие больные погибают, так как надежно остановить кровотечение в гнойной полости крайне затруднительно. Кроме того, часто заболевание осложняется тромбофлебитом селезеночной вены с последующим формированием селективной портальной гипертензии, проявляющейся спленомегалией, варикозным расширением вен пищевода с возможным кровотечением из них. У части больных развивается тромбоз воротной вены с формитрованием допеченочной портальной гипертензии.
Поджелудочная железа иннервируются из солнечного сплетения и большей частью располагается на нем. Это обстоятельство позволяет объяснить причину выраженного болевого синдрома при её заболевании.
Интерес представляет взаимоотношение между панкреатической частью общего желчного протока (ОЖП) и головкой поджелудочной железы. В половине случаев эта часть ОЖП располагается между головкой поджелудочной железы (ПЖ) и нисходящим отделом 12- п. кишки, а в половине наблюдений он бывает окружен тканью железы. Такое положение ОЖП создает условия для сдавления извне при заболеваниях ПЖ, нарушению оттока желчи, развитию механической желтухи.
Основной проток поджелудочной железы (ОППЖ) проходит в толще железы и открывается в нисходящем отделе 12-п. кишки, чаще в ампулу большого сосочка 12-ти перстной кишки (БСДК), который представлен возвышением слизистой 12-ти п.кишки на заднемедиальной полуокружности нисходящего отдела, связанным с проходящим в подслизистом слое терминальной части ОЖП (рис.16). Длина интрамуральной части ОЖП колебалась от 10 до 33 мм и была длиннее БСДК на 1-5мм (рис.30). Следовательно, папиллотомию у больных ОБП следует выполнять на длину несколько меньшую БСДК, что позволяет избежать сквозного ранения стенки 12-ти п.кишки.
Рис.16, рис.30.
По нашим данным ОППЖ в общую ампулу открывался в 8,6% случаев (рис.), а в 114% - он впадал отдельно на вершине сосочка .

Рисунок28 Взаимоотношение между общим желчным и основным протоком поджелудочной железы, (фотография препарата) Обозначения:1 - стенка двенадцатиперстной кишки, 2 - общий желчный проток, 3 - межпротоковая перегородка, 4 - основной проток поджелудочной железы.

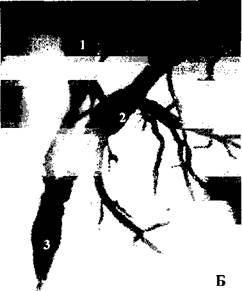
Рисунок 29 А,Б.Взаимоотношение между общим желчным и основным протоком поджелудочной железы, (фоторентгенограмма).
Обозначения:1 - общий желчный проток, 2 - основной проток поджелудочной железы, 3 - ампула БСДК.
В 4% наблюдений имеется хорошо функционирующий дополнительный проток поджелудочной железы .
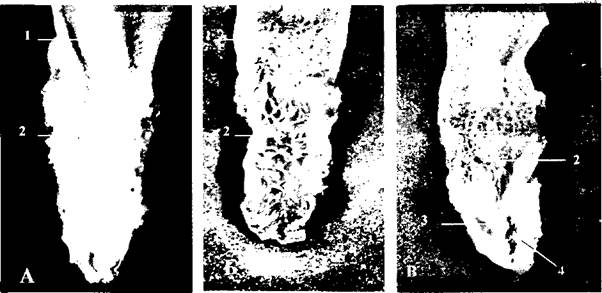
Рисунок 31А, Б, В.Рельеф ампулы БСДК. (фотография препарата): А - слизистая ампулы БСДК с хорошо развитыми продольными складками. Б - слизистая ампулы БСДК с хорошо развитыми поперечными складками.
Обозначения:1 - общий желчный проток, 2 - ампула БСДК, 3 - хорошо выраженная продольная складка слизистой ампулы БСДК, 4 - устье основного протока поджелудочной железы.
Ампула БСДК была обнаружена во всех случаях, независимо от формы соединения протоков. Основным признаком, позволяющим судить о наличии ампулы, является характерный рельеф слизистой оболочки интрамуральной части общего желчного протока. Слизистая этой части протока характеризуется в различной степени развитыми поперечными, продольными и косыми складками. Направлены складки всегда были к отверстию БСДК (рисунок 31 а,б,в). Форма и размеры ампулы БСДК весьма вариабельны. гана ампулы БСДК колебалась в довольно широких пределах - от 7 до 30 мм, диаметр составлял в среднем 3,5 мм.
На всех препаратах при слиянии протоков в общую ампулу хорошо развитая продольная или поперечная складка ампулы сосочка прикрывала в виде клапана отверствие ОППЖ.
Совокупность складок клапанов и сфинктеров была охарактеризована как сфинктерно-клапанный аппарат БСДК, препятствующий возникновению дуоденобилиопанкреатического рефлюкса (А.А.Должиков и соавт., 2002), но, вместе с тем, это может создать знчительное препятствие при выполнении ретроградной панкреато холангиографии (РПХГ), эндоскопической папиллотомии (ЭПГ), что чревато развитием острого панкреатита (ОП), утяжелением имеющегося ОП.
Устье основного протока поджелудочной железы на стенке ампулы занимает различное положение по отношению к общему желчному протоку. При совместном впадении протоков в 89,6% оно располагалось на медиальной стенке ампулы. БСДК, в 6,1% - на задней и в 4,6% - на задне-латеральной полуокружности её.

Рисунок32 А, Б, В.Взаимоотношение между общим желчным и основным потоком поджелудочной железы, (фотография препарата)
Обозначения:1 - общий желчный проток, 2 - ампула БСДК, 3 - устье основного протока поджелудочной железы, 4 - циркулярный мышечный слой кишки.
При раздельном впадении протоков, в устье основного протока поджелудочной железы во всех случаях располагалось ниже и медиальнее устья общего желчного протока. Поэтому при папиллосфинктеротомии рассечение передней стенки ампулы БСДК соответственно 11-12 часам по циферблату предупреждает возможность повреждения устья основного протока поджелудочной железы.
Расстояние от отверствия сосочка до междротоковой перегородки, разделяющей общий желчный проток и основной проток поджелудочной железы, колебалось в значительных пределах - от I до 19 мм.
Знания этого факта позволяет понимать, почему в одних случаях ОБП развивается при ущемлении желчного камня в устье БСДК, в других – он может возникнуть при ущемлении камня в ампуле сосочка на значительном расстоянии от отверствия БСДК.
Из этого следует, что в первом случае достаточно небольшой папиллотомии, чтобы камень встал в просвет 12-ти п. кишки и восстановился свободный отток панкреатического секрета, во втором – устранения блокады устья ОППЖ может понадобиться папиллотомия длиной до 20мм.
В области БСДК устья протоков окружены мышцей (рис. 20 ).

Рисунок 20.Интрамуральная часть общего желчного протока (слизистая и подслизистые оболочки двенадцатиперстной кишки удалены; фотографии препаратов; увеличение в 3,5 раза)
Обозначения:1 - циркулярный мышечный слой двенадцатиперстной кишки, 2 - нисходящие продольные мышечные волокна, 3 - циркулярный мышечный слой терминальной части протоков (сфинктер БСДК), 4 - устье ампулы БСДК.
Мышечный жом БСДК характеризуется рядом важных особенностей своего строения. Образующие его мышечные волокна начинаются в виде небольшой прослойки на 2-3 мм от отверствия соска; продолжаясь вверх, толщина мышечного слоя увеличивается. Наибольшая толщина отмечается
у места слияния общего желчного протока и основного протока поджелудочной железы, где она колебалась от 0,7 до 1 мм. Еще далее вверх толщина жома уменьшается, и на расстоянии 16-30 мм от отверствия соска ( в зависимости от формы и длины, его) мышечные волокна в стенке общего желчного протока обнаружить не удавалось. ( рис. 25,26)

Рисунок25 Стенка общего желчного протока на расстоянии 5 мм от наружной поверхности двенадцатиперстной кишки. Окраска по Ван-Гизон. (микрофотография препарата; увеличение в 120 раз) Обозначения:1 - ткань поджелудочной железы, 2 - стенка общего желчного протока (содержит только эластические и коллагеновые волокна).

Рисунок 26Стенка основного протока поджелудочной железы на расстоянии 3 мм от наружной поверхности двенадцатиперстной кишки. Окраска по Ван-Гизон. (микрофотография препарата; увеличение в 120 раз)
Обозначения:1 - ткань поджелудочной железы, 2 - стенка основного протока поджелудочной железы (содержит только эластические и коллагеновые волокна)
В состав сфинктера входят циркулярные мышечные волокна, не связанные с мышечными элементами 12-п. кишки. Имеются и продольно расположенные восходящие и нисходящие мышечные волокна, не образующие сплошного слоя, но связанные с мышечными элементами последней.
Между мышечными волокнами сфинктера всегда обнаруживаются прослойки соединительной ткани и дуоденальные железы, которые проникают в жом из подслизистой оболочки кишки. (рис. 21).
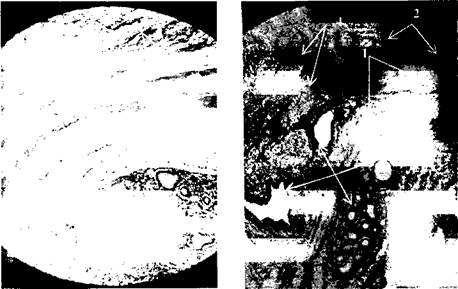
Рисунок 21.Мышечный жом БСДК. Окраска по Ван-Гизон. (микрофотография препарата; увеличение в 120 раз)
Обозначения:1 - циркулярный мышечный слой, 2 - прослойки соединительной ткани, 3 - железы БСДК, 4 - продольные мышечные пучки.
Весьма вероятно, что воспаление дуоденальных желез, может приводить к функциональным и морфологическим нарушениям сфинктера. Нашими исследованиями установлено, что более чем у 80% больных острым билиарным панкреатитом были выявлены как острые воспалительные изменения БСДК, так и в различной степени выраженные явления острого папиллита на фоне предшествующих хронических изменений сосочка.
С практической точки зрения целесообразно выделять ампулярную часть сфинктера, сфинктер общего желчного протока и сфинктер основного протока поджелудочной железы. (рис. 22 ).
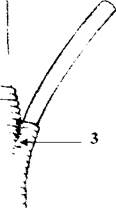
Рисунок22 Мышечный жом БСДК. (схема).
Обозначения:1 - сфинктер общего желчного протока, 2 - ампулярная часть сфинктера, 3 - сфинктер основного протока поджелудочной железы.
Ампулярная часть сфинктера - самая мощная, охватывает расширение общего желчного протока от места впадения в него основного протока поджелудочной железы и до отверствия сосочка. Длина этой части сфинкртера колебалась от 7 до 20 мм.
В большинстве случаев с увеличением длины терминальной части общего желчного протока увеличивается и длина ампулярной части сфинктера. Подобная зависимость наблюдалась и при определении расстояния от отверствия соска до межпротоковой перегородки. Нами было установлено, что при рассечении ампулярной части сфинктера образуется отверствие достаточное, для свободного оттока желчи, обнажается устье основного протока поджелудочной железы, не повреждается мышечная часть стенки 12-п.кишки. Сохраняется также хорошо развитый сфинктер общего желчного протока и менее развитый сфинктер основного протока поджелудочной железы, что может способствовать предупреждению послеоперационного рефлюкса дуоденального содержимого в желчные пути и в основной проток поджелудочной железы.
Сфинктер общего желчного протока во всех случаях был хорошо развит и располагался выше впадения в него основного протока поджелудочной железы. Длина его колебалась от 6 до 10 мм составляя в среднем 7 мм. При этом 1/3 этого жома расположена вне- и 2/3- внутристеночно. Наибольшая толщина сфинктера - у места впадения в общий желчный проток основного протока поджелудочной железы, где она колебалась от 0,6 до 0,8 мм (рисунок 23). По направлению к печени толщина мышечного жома уменьшалась и на расстоянии 1-2 мм от наружной стенки кишки сфинктер общего желчного протока был толщиной от 0,1 до 0,2 мм (рис.24)
На расстоянии 4-5 мм от наружной стенки 12-п.кишки циркулярных мышечных волокон в стенке общего желчного протока выявить не удалось (рис.25).
Сфинктер основного протока поджелудочной железы расположен внутристеночно и имеет длину в среднем 4 мм (измерение проводилось от места впадения его в ампулу БСДК). За наружной поверхностью двенадцатиперстной кишки мышечных волокон в стенке основного протока поджелудочной железы обнаружить не удалось (рисунок 26).
Структурной основой относительной автономности мышечных элементов БСДК является выраженный нервный аппарат.
Источниками внеорганных нервов БСДК, как показали наши исследования, являются переднее и заднее печеночные сплетения, нервные волокна которых широко анастомозируют между собой и образуют как бы сетчатый футляр, окружающий общий желчный проток (рисунок 27).

Рисунок27 Внеорганная иннервация общего желчного протока.
Обозначения:1 - желчный пузырь, 2 - печень, 3 -общий желчный проток, 4 - нервы общего желчного протока, 5 - двенадцатиперстная кишка, 6 - поджелудочная железа.
Помимо нервной, важное значение имеет гормональная регуляция функции сфинктера БСДК. Специфическим действующим агентом этого процесса является холецистокинин (221).
Кровоснабжение БСДК осуществляется ветвями панкреатодуоденальных артерий, из которых наиболее крупные располагались по боковым полуокружностям интрамуральной части ОЖП.

Рисунок23 Внутристеночная часть сфинктера общего желчного протока. Окраска по Ван-Гизон. (микрофотография препарата; увеличение в 120 раз) Обозначения:1 - участок подслизистой оболочки двенадцатиперстной кишки, 2 - мышечные волокна общего желчного протока, 3 - слизистая общего желчного протока.


Рисунок24 Внестеночная часть сфинктера общего желчного протока. Окраска по Ван-Гизон. (микрофотография препарата; увеличение в 120 раз) Обозначения:1 - ткань поджелудочной железы,
2 - мышечные волокна общего желчного протока,
3 - слизистая общего желчного протока.
Физиология поджелудочной железы.
Поджелудочная железа относится к железам внутренней секреции секреции, играет огромную роль в процессах пищеварения. Внешняя секреторная деятельность её состоит из выделения в просвет 12-перстной кишки ряда ферментов, участвующих в переваривании белков, жиров и углеводов.
Изучение механизма панкреатической секреции, состава панкреатического сока и влияния различных условий и свойств пищи на панкреатическую секрецию стало возможным только благодаря исследованиям выдающегося отечественного ученого, лауреата Нобелевской премии им.И.П.Павлова, который впервые разработал методику наложения фистулы поджелудочной железы у животного для получения чистого панкреатического сока. В дальнейшем изучение панкреатической секреции на человеке было проведено К.М. Быковым и Г.М. Давыдовым у больного с хронической панкреатической фистулой, а также в клинике путем применения двойного зонда, дающего возможность получить дуоденальное содержимое отдельно от желудочного.
Панкреатический сок, полученный в чистом виде, представляет собой бесцветную, прозрачную жидкость щелочной реакции (РН-7,8-8,4) благодаря наличию в нем двууглекислого натрия.
Количество панкреатического сока, выделяемого за сутки, составляет 1500-2000 мл. Главной составной частью панкреатического сока являются ферменты: трипсин, липаза, мальтаза, лактаза, инвертаза, нуклеаза, амилаза.
Трипсин - фермент, действующий на белки и расщепляющий их до стадии аминокислот.
Установлено, что трипсин представляет собой комплекс протеолетических ферментов: собственно трипсин, химотрипсин и карбоксипептидазу. В кишечник трипсин выделяется в неактивном состоянии в виде трипсиногена, который под влиянием кишечного фермента энтерокиназы и солей кальция переходит в активное состояние.
Липаза - фермент, расщепляющий жиры. Этот фермент также выделяется в кишечник в неактивном состоянии и активизируется в кишечнике желчью, главным образом, желчными кислотами. Панкреатический сок, совместно с желчью, способствует также эмульгированию жиров.
Амилазав отличие от трипсина и липазы выделяется поджелудочной железой в активном состоянии. Амилаза способствует расщеплению углеводов.
Инвертаза и лактаза расщепляют молочный сахар на декстрозу и фруктозу. Нуклеаза — расщепляет сложные белки-нуклеины.
Механизм панкреатической секреции двойной — нервный и гуморальный. И.П. Павловым впервые был доказан нервный механизм этой секреции. Это подтверждено опытами с мнимым кормлением. У людей с панкреатической фистулой разговор о вкусной пище вызывал обильное отделение панкреатического сока.
Гуморальный механизм секреции связан с выделением железами 12-перстной кишки гормона секретина, который образуется в результате воздействия на слизистую кишки соляной кислоты.
В дальнейшем было установлено, что секретин сложное вещество и в его состав входит пять отдельных компонентов: 1) собственно секретин, стимулирующий обильный ток панкреатического сока; 2) панкреозимин, который стимулирует выделение вязкой панкреатической секреции; 3) гепатокринин, стимулирующий выработку жидкой желчи с малым содержанием солей; 4) холицистокинин, вызывающий сокращение и опорожнение желчного пузыря; 5) энтерокинин, стимулирующий выделение кишечного сока.
Выделение панкреатического сока происходит периодически. После еды выделение панкреатического сока начинается через 2-5 мин. и продолжается в течение нескольких часов в зависимости от состава пищи.
Наиболее сильным возбудителем панкреатической секреции является соляная кислота, а также уксусная, молочная, лимонная и др.
Вторым по силе возбудителем является жир.
Щелочи угнетают панкреатическую секрецию.
Внутрисекреторная деятельность поджелудочной железы состоит в выработке гормонов: инсулина, липокаина и глюкагона. Благодаря этому поджелудочная железа играет большую роль в регулировании углеводного и ли-пидного обмена.
Впервые инкреторный аппарат поджелудочной железы описал Лангерганс в 1869 г. и было установлено, что описанные островки выделяют инсулин.
Глюкагон повышает содержание сахара в организме, т.е. действует противоположно инсулину. Таким образом, сохраняется равновесие сахара в организме.
Альфа-клетки островком Лангенганса вырабатывают липокаин, который предупреждает жировое перерождение печени.
Доказано участие поджелудочной железы в регуляции кроветворения и артериального давления.
Этиология и патогенез острого панкреатита. Предложено много теорий, объясняющих возникновение острого панкреатита, но независимо от этиологического фактора патогенетическая программа острого панкреатита реализуется в индивидуальной комбинации таких патологических синдромов, как панкреатическая гиперсекреция, протоковая гипертензия, ишемия поджелудочной железы и повреждение панкреатоцитов.
Теория общего канала - предложил Opil (1901 г.) Он, вскрывая труп больного, умершего от ОП, обнаружил в ампуле БСДК ущемившийся желчный камень и пришел к заключению, что наличие общей ампулы большого сосочка двенадцатиперстной кишки (БСДК) способствует забрасыванию желчи в панкреатический проток с последующей активацией ферментов поджелудочной железы.
Такое состояние может возникнуть при закупорке отверствия БСДК камнем, гнойно-некротической пробкой, при спазме БСДК, его рубцовом сужении. Эта теория наиболее жизненная, так как подтверждается частым сочетанием желчекаменной болезни и панкреатита. По данным отдельных авторов частота взаимосвязи острого панкреатита с заболеваниями желчных путей варьрует от 50 до 92%. Такой панкреатит называют билиарным.
Обтурацию протока поджелудочной железы с последующей гипертензией в нем , может вызвать метаплазия эпителия панкреатических протоков.
Исключительную роль повышения гидростатического давления в панкреатических протоках в происхождении острого панкреатита демонстрировали многие исследователи. В эксперименте доказано, что повышение давления в панкреатическом протоке до 300 мм вд.ст. вызывает острый отек железы, а давление, превышающее 500-700 мм вд.ст. , приводит к острому геморрагическому панкреатиту. Экспериментально установлено, что при превышении давления более 300 мм вд.ст. ацинусы, основная морфологическая единица железы разрывается.
Значение гипертензии в возникновении острого панкреатита подтверждается развитием ОП после ретроградной панкреатографии.
К возникновению гипертензии в панкреатическом протоке могут привести дуоденостаз, воспаление дуоденальных дивертикулов, дуоденит с папиллитом, гастродуоденальная язва (гастрогенныйпанкреатит), закупорка общего желчного протока аскаридами, обильная стимуляция поджелудочной железы, что наблюдается при переедании особенно жирной пищи (алиментарныйпанкреатит), употреблении алкоголя ( алкогольный панкреатит).
Об алкагольном панкреатите с уверенностью можно говорить при развитии панкреатита после запоя у больного с соматическими и психическими признаками хронического алкаголизма.
Алкагольныйпанкреатит - один из самых частых. Его патогенез реализуется при участии таких патологических синдромов, как панкреатическая гиперсекреция и повышение вязкости панкреатического сока, вызывающие гипертенезию на уровне ацинарных протоков.
Алиментарный панкреатит встречается значительно реже. Это весьма опасный вид острого деструктивного панкреатита. Ведущим фактором его развития является синдром панкреатической гиперсекреции в ответ на обилие острой, жирной пищи. Алкоголь при алиментарном панкреатите, в отличие от алкагольного, носит характер случайного эпизода.
Повреждение ацинусов может вызвать любая травма и тогда развивается травматическийпанкреатит ( тупая травма, интраоперационное повреждение, травмы БСДК при ЭПТ, РПХГ).
До настоящего времени всеобъемлющей теории, объясняющей патогенез ОП нет.
Длительное время патогенез острого панкреатита рассматривался с позиций ферментативной теории, согласно которой воздействие этиологического фактора приводит к повреждению панкреатоцитов и попаданию активированных ферментов поджелудочной железы в интерстиций, что сопровождается развитием феномена ''уклонения панкреатических ферментов" в кровь. Дальнейшие местные и экстрапанкреатические проявления заболевания объясняются в основном влиянием ферментной аутоагрессии .
На смену ферментативной пришла патобиохимическая теория, отводящая трипсину лишь начальную, пусковую роль в формировании патологического состояния, с дальнейшим вовлечением в патогенез липолитической и протеолитической систем ферментов поджелудочной железы, свертывающей и противосвертывающей систем крови, калликреин-кининовой, симпатико-адреналовой систем. Однако при таком подходе отсутствовало комплексное рассмотрение патологического процесса, учитывающее вовлечение всего организма, а не отдельных его систем. Поэтому в настоящее время патогенез острого панкреатита принято рассматривать в рамках формирующегося синдрома системного воспалительного ответа.
Термин "синдром системного воспалительного ответа" (SIRS или ССВО) был принят на совместной конференции американской коллегии пульмонологов и общества критической медицины США в 1991 г. с целью внесения терминологической ясности при характеристике больных в критическом состоянии, которое может развиваться вследствие различных причин.
SIRS – синдром характеризуется определенными клиническими критериями, которыми являются : температура тела больше 38.0С или менее 36.0С, частота сердечных сокращений более 90 в минуту, частота дыхания более 20 в минуту или артериальная гипокапния (СО2 менее 30 мм рт.ст.), лейкоцитоз более 12х10/л или лейкопения менее 4х10/л или наличие более 10% незрелых форм нейтрофилов, возникающими в ответ на массивный выброс медиаторов воспаления.
Выделяют три стадии развития ССВО:
1. Локальная продукция медиаторов воспаления в ответ на травму или инфекцию.
2. Выброс малого количества медиаторов воспаления в системный кровоток.
3. Генерализация воспалительной реакции.
Пусковым фактором в развитии ССВО при ОП является поступление в организм продуктов распада некротических тканей, образовавшихся вследствие самопереваривания железы собственными активированными ферментами. Всасывающиеся эндотоксины запускают выработку медиаторов воспаления, таких, как фактор некроза опухоли, интерлейкины, которые активизируют выброс как про-, так противовоспалительных агентов, значительную часть которых составляют эйкозаноиды - продукты ферментативного превращения арахидоновой кислоты. При остром деструктивном панкреатите наблюдается значительное увеличение уровня фактора некроза опухоли в крови, что подтверждает справедливость теории ССВО при панкреатите .
Немаловажную роль при ССВО играют лейкотриены (ЛТ), входящие в группу эйкозаноидов, что подтверждается повышением уровня Л Т в перитонеальном экссудате и лимфе при остром деструктивном панкретите
более чем в 12 раз. Ключевая роль липидных медиаторов в развитии ССВО подтверждается появлением в крови активной фракции фосфолипазы (сФЛА2П), основная масса которой является неактивной (сФЛА21). Данная фракция, как и цитозольная, принимает участие в синтезе простагландинов, ЛТ, тромбоксанов и др.
Другими медиаторами воспалительного ответа являются: компоненты копмлемента, фактор активации тромбоцитов, гистамин, межклеточные адгезивные молекулы, свободные радикалы кислорода, компоненты калликреин-кининовой системы, оксид азота.
Массивный выброс медиаторов воспаления сопровождается развитием эндотелиальной дисфункции, нарушением микроциркуляции, диссименированного внутрисосудистого свертывания крови, полиорганной недостаточности с поражением в первую очередь почек и легких.
Поражение легких характеризуется развитием острого респираторного дистресс синдрома взрослых, уменьшением легочной эластичности, артериовенозным шунтированием крови в малом круге кровообращения, рефрактерной гипоксемией.
Ведущее значение в повреждении легких при ОРДСВ отводится лейкотриенам. Из очага воспаления ЛТ с током крови поступают в печень, где основная масса их инактивируется. Однако при тяжелом течении острого панкреатита может происходить активация печеночных макрофагов с последующей выработкой ЛТ в печени, снижение её барьерной функции также приводит к массивному поступлению ЛТ в системный кровоток и, в частности, в легкие.
В результате дисфункции печени, почек, кишечника появляются новые факторы повреждающего воздействия. К ним относятся промежуточные и конечные продукты нормального обмена в концентрациях выше физиологических (лактат, мочевина, креатинин, билирубин) . Накопленные в патологических концентрациях компоненты и
эффекторы регуляторных систем (калликреин-кининовой, свертывающей, фибринолитической, нейромедиаторы), продукты патологического обмена (альдегиды, кетоны, высшие спирты), вещества кишечного происхождения типа индола, скатола замыкают порочный патологический круг при ОП.
Основной чертой всей совокупности изложенных изменений обмена веществ является сочетание гиперпотребности организма в различных субстратах для адаптации к повышенным затратам энергии с толерантностью тканей к этим же субстратам, т.е. формируюется синдром гиперметаболизма, представляющий собой метаболический ответ организма на генерализованную воспалительную реакцию, который характеризуется лихорадкой, лейкоцитозом, тахикардией и тахипноэ, появлением диффузных легочных инфильтратов на рентгенограммах, снижением легочного рисунка, прогрессирующей артериальной гипоксемией, увеличением минутного объема вентиляции. Показатели летальности при синдроме гиперметаболизма колеблются от 25 до 40 %. Гиперметаболизм может поддерживаться длительное время либо за счет недостаточной санации первоначального очага инфекта, либо из-за появления нового септикопиемического.
Критерием тяжести острого панкреатита является глубина воспалительно-дегенеративных изменений в поджелудочной железе, объем панкреонекроза, степень вовлечения в некротический процесс парапанкреатической и забрюшинной клетчатки. Это определяет клиническое проявление и течение заболевания.
Вначале ОП развивается отек железы. Железа становится бледной, стекловидной, отечной, твердой. Отек нередко распространяется на соседние ткани и органы - брюшину, брыжейку, кишечника, забрюшинную клетчатку. Если устранить причину ОП на этой стадии гистологических изменений, при хорошей активности противовоспалительных медиаторов можно добиться абортивного течения панкреатита.
При прогрессировании процесса нарастает стаз в сосудах, капиллярах, и в ткани железы появляются кровоизлияния. Железа становится красной. Гистологически определяется отек, лимфоидная инфильтрация, выход эритроцитов из сосудистого русла - наблюдается геморрагический отек железы. В дальнейшем , вследствие развивающегося тромбоза в сосудах, присоединяется вторичный некроз, увеличиваются масштабы поражения паренхимы. Железа становится дряблой. При алкагольной этиологии панкреатита, как правило, преобладает геморрагический некроз, который объясняют, прежде всего, активацией трипсина.
Некробиотические процессы приводят к активации липазы, вследствие чего присоединяется жировой некроз.
Большинство исследователей считают, что геморрагический и жировой некроз наступают практически одновременно. О форме панкреатита судят по преобладающим признакам. Следует подчеркнуть, что при ЖКБ преобладает жировой панкреонекроз. Поджелудочная железа при этом становится дряблой, мутной, покрытая сероватыми пятнами, имеющими вид капель сальной свечи. Эти специфические пятна жирового некроза определяются также на брюшине, брыжейке и в др. местах, куда лимфагенным путем проникает активированная липаза.
В.С.Савельев с соавт. считают, что во всех случаях вначале развивается липолитический некроз панкреоцитов. В них накапливаются жирные кислоты и сдвигают рН панкреацитов до 3,5-4,5 и это приводит к активации трипсиногена и переход его в трипсин.
Характерным является быстрое прогрессирование процесса с развитием перитонита, ретроперитонита.
Следует указать, что хотя ферментативная теория патогенеза ОП потеряла свое доминирующее значение, факт влияния активных ферментов ПЖ на течение заболевания отрицать не следует.
Вследствие уклонения активных ферментов поджелудочной железы в кровеносные сосуды и лимфатические пути наступают большие изменения и в других органах. В печени нередко определяются поражения, начиная от гнездного некроза до диффузной жировой дегенерации. Наблюдаются затеки активных ферментов в желчные протоки с образованием холангита, перихолангита, вплоть до некроза стенок и их прободения, а также в желчный пузырь с развитием ферментативного холецистита (Т.В.Шаак).
Присутствие ферментов в желчном пузыре вызывают аутолиз его стенки, что приводит к пропотеванию желчи в свободную брюшную полость и развитию перитонита. Для пропотных желчных перитонитов характерно осносительно быстрое ухудшение общего состояния больного, нарастание симптомов «острого живота».
Во время операции обращает на себя внимание студенистого характера, окрашенное желчью, пропитываение тканей. Со стенки желчного пузыря стекает желчь, хотя он и без видимых признаков гангренозного процесса, стенка рыхлая.
В почках нередко определяется тубулярный нефроз. В серозных оболочках - брюшине, перикарде, плевре встречаются участки жирового некроза. В своей практике мы наблюдали случаи летальных исходов, а на секции находили бляшки стеатонекроза на проводящих путях сердца.
Классификация острого панкреатитапринята на IХ Всероссийском съезде хирургов в 2000 г и создана на основе классификации, принятой в Атланте в 1992 г. (США).
Предложенная классификация соответствует современному уровню комплексной клинической, лабораторной и топической инструментальной диагностики острого панкреатита и его разнообразных осложнений. В её основу положено понимание стадийной трансформации зон некротической деструкции и развитии осложнений в зависимости от распространенности и характера поражения поджелудочной железы (ПЖ) и забрюшинной клетчатки под влиянием фактора эндогенного и экзогенного инфицирования.
Предложенная классификация выглядит следующим образом:
Формы острого панкреатита:
