Строение сердечных гликозидов
В основе строения агликонов сердечных гликозидов лежит циклопентанпергидрофенантреновая система, полностью или частично гидрированная.
Кольца А/В могут иметь как цис-, так и транс-сочленение.
Относительно кольца кольца В кольцо С всегда занимает транс-положение.
А кольца С/D в отличие от других природных стероидов имеют всегда цис-сочленение.
Молекулы сердечных гликозидов (СГ) состоит из агликона и углеводной части.
Специфическим действием на миокард обладает только агликон. Сахара на сердце не действуют, но, в сочетании с агликоном, обусловливают растворимость гликозидов в воде и их всасываемость.
В основе агликона СГ лежит стероидное ядро циклопентанпергидрофенантрена, в котором;
- кольца А/В могут иметь как цис-, так и транс-сочленение;
- кольца В/С имеют транс-положение (присуще всем природным стероидам);
- кольца С/D имеют цис-сочленение (в отличие от других природных стероидных соединений).
В стероидном ядре имеются постоянные заместители:
- в 17-м положении стероидного ядра у СГ всегда присоединяется 5 - членное или 6-членное ненасыщенное лактонное кольцо. Присутствие лактонного кольца отличает СГ от всех других природных стероидов. Именно наличие ненасыщенного лактонного кольца в молекуле обусловливает специфическое действие данных веществ на миокард.
Отсутствие, разрыв или изомеризация лактонного кольца приводит к полной потере активности СГ;
- в 3 и 14 положениях присутствуют гидроксильные (-ОН) группы;
- в 13 положении находится метильная (-СНз) группа.
Природные агликоны СГ могут иметь переменные заместители:
- в 10 положении могут быть метильная (-СНз), оксиметильная (-СНзОН), альдегидная (-СНО) или карбоксильная (-СООН) группа. Наличие у С10 альдегидной группы приводит к возрастанию гидрофильности и увеличению активности СГ при одновременном повышении токсичности;
- в 1, 2, 5, 11, 12, 15 и 16 положениях могут присутствовать гидроксильные (-ОН) группы. Наличие -ОН у С16 приводит к снижению активности СГ. Гидроксилы у С16 могут быть ацилированы муравьиной, уксусной, изовалериановой кислотами, что увеличивает токсичность СГ.
Важное значение имеет ориентация функциональных групп относительно плоскости молекулы. Наибольшей активностью обладают СГ, у которых имеется β-ориентапия лактонного кольца и других заместителей.
Свободные агликоны СГ плохо удерживаются миокардом. Поэтому действие проявляется очень короткое время и они более токсичны по сравнению с гликозидами.
Углеводная (гликозильная) часть молекулы содержит от 1 до 5 моносахаридов, всегда присоединющихся через кислород у С3. Все СГ являются О-гликозидами. Образование гликозидной связи происходит за счет атома кислорода полуацетального гидроксила сахара и атома водорода от гидроксила у Сз агликона СГ. Олигосахаридна часть, состоящая более чем из двух сахаров, построена линейно, в других случах может быть разветвленной.
Наиболее часто встречаются распространенные в растениях сахара (глюкоза, галактоза, ксилоза, арабиноза). Кроме того, в составе СГ присутствуют специфические обедненные кислородом - 6-дезоксисахара (рамноза) или 2,6-дезоксисахара (дигитоксоза) и их метиловые эфиры (цимароза) и другие.
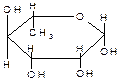
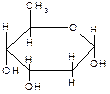
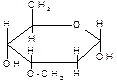
L-рамноза D-дигитоксоза D-цимароза
Дезоксисахара всегда присоединяются непосредственно к агликону. Если в состав углеводной части молекулы входит глюкоза, то она всегда находится в конце цепи.
Количество моносахаридных остатков имеет важное значение для силы, быстроты и продолжительности действия СГ. Монозиды, биозиды действуют сильно, но кратковременно. С возрастанием количества сахаров в углеводной части молекулы действие СГ становится более мягким и продолжительным.
СГ состоят из трех основных частей:
1. Стероидный цикл;
2. Лактонное кольцо;
3. Углеводная цепь.
 R1 = -CH3; -CH2OH; -CHO; -COOH
R1 = -CH3; -CH2OH; -CHO; -COOH
R2 = -H; -OH
