Групповой реагент, общие и фармакопейные реакции анионов II аналитической группы
Групповой реагент – раствор AgNO3
Реакция хлорид-иона Cl-
Нитрат серебра AgNO3 с ионом Cl- дает белый творожистый осадок хлорида серебра:
NaCl + AgNO3 = AgCl↓ + NaNO3
Cl- + Ag+ = AgCl↓
Осадок нерастворим в азотной кислоте, но легко растворяется в аммиаке с образованием комплексного соединения:
AgCl + 2NH3 = [Ag(NH3)2]Cl
При прибавлении к раствору хлорида диамин серебра концентрированной азотной кислоты осадок снова выделяется:
[Ag(NH3)2]Cl + 2HNO3 = 2NH4NO3 + AgCl↓
Реакция является фармакопейной.
Реакция бромид-иона Br –
Нитрат серебра AgNO3 с ионами Br – дает желтовато-белый осадок бромида серебра:
NaBr + AgNO3 = AgBr↓ + NaNO3
Ag+ + Br- = AgBr↓
Осадок не растворяется в азотной кислоте, плохо растворим в аммиаке, в отличие от хлорида серебра и хорошо растворяется в растворе тиосульфата натрия:
AgBr + Na2S2O3 = NaBr + Na[Ag(S2O3]
Реакция является фармакопейной.
Реакция иодид – иона J-
Нитрат серебра AgNO3 выделяет из иодидов светло-желтый творожистый осадок иодида серебра:
KJ + AgNO3 = AgJ↓ + KNO3
Ag+ + J- = AgJ↓
Осадок не растворяется в азотной кислоте и в растворе аммиака и плохо растворяется в растворе тиосульфата натрия. Реакция является фармакопейной.
4.К Образуйте заданную комплексную частицу в соединение и укажите для него:
- внешнюю координационную сферу;
- внутреннюю координационную сферу;
- комплексообразователь;
- лиганды;
- координационное число;
- назвать полученные соединения.
[Zn(OH)4]*, где Zn2+
-Внутренняя координационная сфера- [Zn(OH)4],
-Комплексообразователь-Zn2+
-Лиганды- OH-
-КЧ-4
-
5.Составьте уравнения гидролиза солей:
Al2S3, NH4Cl, Cu(NO3)2, FeCl3, Rb2SO3, Na2S,
Укажите рН раствора.
Al2S3+ 6 HOH= 2Al(OH)3+ 3H2S
2Al3++ 3S-+ HOH= 2Al(OH)3+ 3H2S
Среда нейтральная.
NH4Cl+ HOH=NH4OH+ HCl
NH4++ HOH= NH4OH + H+
Среда кислая, фиолетовый лакмус станет красным.
Сu(NO3)2+ HOH= CuOHNO3+ HNO3
Cu2++ HOH= CuOH++ H+
CuOHNO3+ HOH= Cu(OH)2+ HNO3
CuOH++HOH= Cu(OH)2+ H+
Среда кислая, фиолетовый лакмус станет красным.
FeCl3+ HOH=FeOHCl2+ HCl
Fe+3+ HOH= FeOH+2+ H+
FeOHCl2+HOH= Fe(OH)2Cl+ HCl
FeOH+2+HOH= Fe(OH)2++H+
Fe(OH)2Cl+HOH= Fe(OH)3+ HCl
Fe(OH)2++ HOH=Fe(OH)3+ H+
Среда кислая, фиолетовый лакмус станет красным.
Rb2SO3+HOH=RbHSO3+RbOH
SO2- +HOH= HSO3- + OH-
RbHSO3+HOH= RbOH+ H2SO3
HSO3-+HOH= H2SO3+ OH-
Среда щелочная, фиолетовый лакмус станет синим.
Na2S+ HOH= NaHS+ NaOH
S2-+HOH= HS-+ OH-
NaHS+ HOH=NaOH+ H2S
HS-+HOH= H2S+ OH-
Среда щелочная, фиолетовый лакмус станет синим.
| департамент здравоохранения Брянской области Государственное автономное образовательное учреждение среднего профессионального образования «Брянский базовый медицинский колледж» | 060301 «Фармация» (код и наименование специальности) базовый (профиль подготовки) «Фармация» (наименование ВМК) |
Учебная дисциплинаАналитическая химия
Коды проверяемых компетенций:
ОК: 2, 3
ПК: 1.1; 1.6; 2.1; 2.2; 2.3
БИЛЕТ №9
1.Реакция при температуре 60°С протекает за 1 мин.30сек. За сколько времени закончится эта реакция при температуре 80°С, если в данном интервале температурный коэффициент (у) равен 3?
Решение: в соответствии с правилом Вант-Гоффа при увеличении температуры от 60°С до 80°С скорость реакции возрастает:
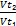 =
= 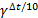 ,
, 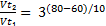 = 32=9
= 32=9
Увеличивается в 9 раз.
2) скорость реакции обратно пропорциональна времени реакции. Следовательно:
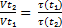 , или τ(t₂)= τ(t₁)*
, или τ(t₂)= τ(t₁)* 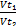
Где τ(t₁) и τ(t₂) – время реакции при температурах t1 и t2. Учитывая, что τ(t₁)= 90 сек. (1мин. 30 сек.), определяем время реакции при температуре t2: τ(t₁)= 90 сек* 1/9= 10 сек. Ответ: 10 сек.
2.Напишите характерные реакции на ион K+.
Реакция окрашивания пламени.
Летучие соли калия окрашивают бесцветное пламя горелки в фиолетовый цвет
Винная кислота Н2С4Н4О6 при достаточной концентрации ионов К+ в растворе дает белый кристаллический осадок гидротартрата калия
KCl + Н2С4Н4О6 = KHC4H4O6↓ + HCl
K+ + HC4H4O6- = KHC4H4O6↓
Гексанитритокобальтат (III) натрия Na3 [Co(NO2)6] осаждает из нейтрального или слабокислого раствора желтый кристаллический осадок гексанитритокобальтата (III) калия-натрия:
Na3 [Co(NO2)6] +2KCl = K2 Na [Co(NO2)6]↓ + 2NaCl
2K+ + Na+ + [Co(NO2)6]3- = K2Na[Co(NO2)6]↓
Микрокристаллоскопическая реакция – нитрит натрия – свинца (II) Na2PbCu (NO2)6, реагирует с солями калия в нейтральной среде, образуя характерные кубические кристаллы коричневого или черного цвета:
2KCl + Na2PbCu(NO2)6 = K2PbCu(NO2)6↓ + 2NaCl
