Опыт 2. Получение труднорастворимых соединений щелочных металлов
ОБЩАЯ и неорганическая ХИМИя
Свойства элементов главных подгрупп
Методические указания к лабораторным работам
для студентов, обучающихся по направлению подготовки бакалавриата 240100
САНКТ-ПЕТЕРБУРГ
УДК 546 (076.5)
ОБЩАЯ И НЕОРГАНИЧЕСКАЯ ХИМИЯ. СВОЙСТВА ЭЛЕМЕНТОВ ГЛАВНЫХ ПОДГРУПП:Методические указания к лабораторным работам / Национальный минерально-сырьевой университет «Горный». Сост.: Д.Э. Чиркст, Т.Е. Литвинова, И.В. Берлинский, Д.С. Луцкий.
Изложены методики проведения опытов по свойствам элементов периодической системы и обработки результатов экспериментальных работ. Лабораторные работы предназначены для студентов, обучающихся по направлению подготовки бакалавриата 240100 «Химическая технология».
Табл. 2. Библиогр. 8
Научный редактор: проф. Чиркст Д.Э.
© Национальный минерально-сырьевой
университет «Горный» , 2012 г.
Введение
Лабораторные работы по общей и неорганической химии проводятся с целью закрепления теоретического материала, который излагается на лекциях и самостоятельно прорабатывается студентами по учебникам и учебным пособиям. В ходе лабораторного практикума студенту ставится задача освоить приемы и методы ведения химического эксперимента, приобрести навыки работы с аппаратурой и реактивами, научится основным способам обработки экспериментальных данных и оценки погрешностей полученных результатов.
Методические указания в сжатой форме знакомят студентов с основными теоретическими положениями, относящимися к данной лабораторной работе или группе лабораторных работ со схожей тематикой, основным оборудованием и приемами работы на нем, правилами оформления лабораторных протоколов, обработкой результатов эксперимента.
Лабораторная работа № 1. Свойства элементов I А группы
Цель работы: изучение химических свойств элементов I А .группы.
Водород
Общие сведения
Электронное строение атома водорода описывается формулой 1s1. По своему электронному строению водород располагают в I А подгруппе таблицы Менделеева. По химическим свойствам водород является типичным неметаллом. В виде простого вещества – газ. Катион водорода обладает окислительными свойствами по отношению к металлам, стоящим в ряду напряжений до водорода.
Выполнение работы
Опыт 1. Кислотно-основные взаимодействия.
А. С помощью индикаторной бумаги определить рН нескольких растворов HCl, HF, NH4ОН, NaOH.
Б. В разных пробирках смешать по одинаковому числу капель a) HCl и NH4OH; b) HCl и NaOH; c) HF и NaOH. Определить рН каждой смеси. Какая кислота является более сильной: плавиковая или соляная? Написать уравнения реакции диссоциации. Для более слабой кислоты составить уравнение константы диссоциации. Какое основание будет более сильным: гидроксид аммония или гидроксид натрия? Написать уравнения реакций диссоциации. Вычислить рН растворов, считая, что концентрация каждого электролита 0,1 моль/л. Kd(HF) = 6,2·10–4. Написать реакции, перечисленные в п. Б, в молекулярной и ионной формах. Объяснить значение рН растворов после смешения кислот и оснований с позиций гидролиза. Составить уравнения реакций гидролиза в молекулярной и ионной формах.
Опыт 2. Реакция осаждения протона.К нескольким каплям разбавленной соляной кислоты добавить 1,5 % раствор бензоата натрия до образования осадка трудно растворимой бензойной кислоты. Составить уравнение реакции в молекулярной и ионной форме. Показать вытеснение более слабой кислоты.
Опыт 3. Окислительные свойства катиона водорода.
А. В три пробирки налить по нескольку капель раствор соляной кислоты концентрацией 15 % и поместить кусочки металлических цинка, железа, меди. Наблюдать выделение газа. В каком случае водород не выделяется и реакция не идет. Почему? В каком случае реакция протекает наиболее интенсивно?
Б. Кусочек ленты или стружки магния поместить в раствор хлорида аммония. Наблюдать выделение газа. Объяснить реакцию растворения магния в растворе хлористого аммония. При составлении уравнения реакции учесть, что растворение магния в растворе хлористого аммония – окислительно-восстановительный процесс.
Щелочные металлы
Общие сведения
К щелочным металлам традиционно относят литий, натрий, калий, рубидий цезий и франций. В своих соединениях (в большинстве случаев ионных) они проявляют всегда степень окисления +1. Эти элементы относятся к числу самых «неблагородных». Резкое изменение радиуса атома при переходе то лития к натрию и, далее, к тройке калий-рубидий-цезий является причиной отличия свойств лития и натрия от их более тяжелых аналогов. Особо следует подчеркнуть небольшой размер атома и иона лития, что приводит к аналогии свойств соединений этого элемента с магнием (т.н. диагональное сходство).
Характерным свойством щелочных металлов является легкость, с которой возбуждается световое излечение их атомов. Соли щелочных металлов способны окрашивать пламя горелки в различные цвета.
В химическом отношении все щелочные металлы крайне реакционноспособны. Они разлагают воду, реагируют со всеми неметаллами с образованием бинарных соединений.
Соли щелочных металлов, как правило бесцветны, если только не содержат окрашенных анионов и почти все легко растворимы. Исключение составляют отдельные соединения и некоторые соли лития. Образование труднорастворимых фосфатов, фторидов и карбонатов позволяет рассматривать литий как металл, свойства которого промежуточны между свойствами щелочных и щелочноземельных элементов.
Выполнение работы
Опыт 1. Окрашивание пламени. В пламя горелки последовательно внести по капле солей щелочных металлов (Li, Na, K, Cs). Отметить цвет пламени. Как цвет пламени связан с электронным строением атома?
Опыт 2. Получение труднорастворимых соединений щелочных металлов.
А. Получение осадка дигидроантимоната натрия:
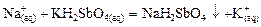 .
.
В пробирку внести 2–3 капли раствора соли натрия и прибавить равный объем дигидроантимоната калия. Для улучшения выпадения осадка можно потереть внутренние стенки пробирки стеклянной палочкой, охладить реакционную смесь.
Примечание: при рН < 7 выпадает белый аморфный осадок сурьмяной кислоты 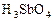 !
!
Б. Получение гексанитрокобальтата (III) натрия-калия. В пробирку внести 2-3 капли соли калия и прибавить значительный избыток раствора гексанитрокобальтата натрия, энергично перемешать. Осадок какого цвета образуется? Какой ион отвечает за образование окрашенного соединения калия?
В. Образование малорастворимых соединений лития. В 3 пробирки налить по 3–4 каплям соли лития и прибавить гидроксид натрия и гидрофосфат натрия (при нагревании); фторид натрия; карбонат натрия.
