ЛАБОРАТОРНАЯ РАБОТА № 6. "Определение общей жесткости воды"
"Определение общей жесткости воды".
В основе определения лежат следующие схемы реакций:
1. Me2+ + HInd2- → MeInd- + Н+
голубой винно-красный
2. MeInd- + Н2Edta2- → HInd2- + H+ + MeEdta2-
винно-красный Тр. Б голубой
Na2[Н2Edta] → 2Na+ + H2Edta2-
Трилон Б
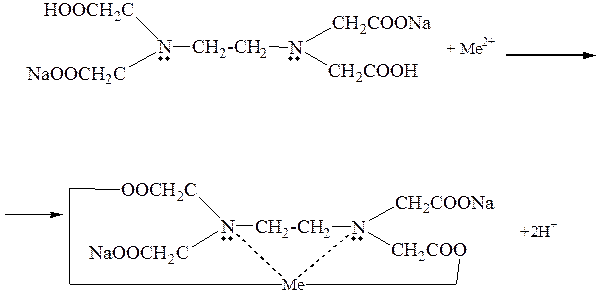
Методика определения
В колбу для титрования отбирают мерной колбой 50 мл анализируемой воды, прибавляют, если нужно, дистиллированную воду до объёма 100 мл, приливают мерной пробиркой 5 мл буферного раствора, 20-30 мг сухой смеси индикатора хром темно-синего, смесь тщательно перемешивают и, энергично встряхивая, медленно титруют раствором трилона Б, до перехода окраски раствора от винно-красной через лиловую и сине-фиолетовую к чисто голубой (синей).
При прибавлении избытка трилона Б окраска больше не меняется, поэтому в качестве эталона (свидетеля) может служить заведомо перетитрованный раствор пробы.
Точное титрование повторяют еще 2-3 раза. Из 3-х сходящихся результатов (разность не более 0,1 мл) берут среднее.
.
Данные эксперимента:
1. Водопроводная вода.
К Тр.Б =____
N Тр.Б =______моль/л
VН2О =______мл
V1 Тр.Б =______мл
V2 Тр.Б =______мл VСр. Тр.Б =______мл
V3 Тр.Б =______мл
Обработка результатов:
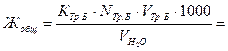
2. Кипяченая вода.
К Тр.Б =____
N Тр.Б =______моль/л
VН2О =______мл
V1 Тр.Б =______мл
V2 Тр.Б =______мл VСр. Тр.Б =______мл
V3 Тр.Б =______мл
Обработка результатов:
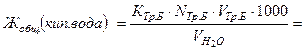
Воспользовавшись данными лабораторной работы №2, рассчитайте значение постоянной жесткости воды.
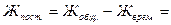 моль-экв/л Са2+ и Мg2+.
моль-экв/л Са2+ и Мg2+.
ОКСИДИМЕТРИЯ
Вопросы для самоподготовки.
1. Перечислите и охарактеризуйте окислительно-восстановительные методы объемного анализа.
2. Какие вещества применяются в качестве рабочих растворов в окислительно-восстановительных методах анализа?
3. Что представляют собой окислительно-восстановительные индикаторы? Что является причиной перемены их окраски?
4. Как рассчитывают молярные массы эквивалентов окислителей и восстановителей?
5. Расставить коэффициенты в уравнениях реакций методом полуреакций, рассчитать молярные массы эквивалента окислителя и восстановителя и указать в каком направлении могут самопроизвольно протекать следующие процессы:
1) K2Cr2O7 + H2SO4 + FеSO4 → Cr2(SO4)3 + Fе2(SO4)3 + K2SO4 + H2O
2) NaNO2 + КМnO4 + Н2SO4 → MnSO4 + NaNO3 + K2SO4 + H2O
3) МnO2 + HCl → MnCl2 + Cl2 + H2O
4) Zn+ HNO3 → NH4NO3 + Zn(NO3)2 + H2O
5) KMnO4 + Na2S + H2SO4 → MnSO4 + Na2SO4 + K2SO4 +S + H2O
6. От каких факторов зависит скорость окислительно-восстановительных реакций? Чему равен окислительный потенциал пары Sn4+/Sn2+, если молярная концентрация ионов Sn4+ равна 0,1 моль/л, а молярная концентрация ионов Sn2+ равна 0,001 моль/л.
7. Можно ли: а) действием С12 окислить SnCl2 в SnCl4: б) действием РbO2 в кислой среде окислить Сl- в Cl2 ?
8. Какой из ионов Sn2+ или Sn4+ проявляет большие окислительные свойства? Почему? Вычислить окислительный потенциал пары Sn4+/Sn2+ при молярной концентрации ионов Sn4+ равной 0,1моль/л, а ионов Sn2+ - 0,0001моль/л.
9. Указать в каком направлении могут самопроизвольно протекать следующие реакции:
1) 2NаСl + Fе2(SО4)3 ― 2FеSО4 + Сl2+ Nа2SО4
2) φº Сl2/2Сl¯ = +1,36В; φº Fе3+/Fе2+ = +0,77В;
3) НСlО + Н2О2 → О2+ НСl + Н2О
4) φº О2/Н2О2 = +0,68В; φº ClО¯/Cl¯ = +1,49В;
5) 2НIО3 + 5Н2О2 ― 5О2+ I2 + 6Н2О
6) φº 2IО3¯/I2 = +1,19В; φº О2/Н2О2 = +0,68В;
7) 5H2O2 + I2 → 2НIО3 + 4H2O
8) φº 2IО3¯/I2 = +1,19В; φº Н2О2 /Н2О = +1,77В;
ПЕРМАНГАНАТОМЕТРИЯ
Вопросы для самоподготовки.
1. В чем состоит сущность перманганатометрии?
2. Почему не нужен индикатор при перманганатометрических определениях?
3. Навеску технического железного купороса в 5,770 г растворили и довели объем раствора водой до 250мл. На титрование 25,0 мл полученного раствора пошло в среднем 19,5 мл раствора KMnO4 с титром 0,003100 г/мл. Вычислите массовую долю FеSO4 в техническом продукте.
4. Почему перманганатометрическое титрование целесообразно проводить в кислой среде? Вычислить окислительный потенциал перманганата при СMnO4‾ = СMn2+ и молярной концентрации ионов водорода равной 10-5 моль/л.
5. Сколько миллилитров раствора КМnО4 с молярной концентрацией эквивалентов 0,1054 моль/л израсходуется на титрование 0,1600 г (NН4)2С2О4·Н2О, растворенных в 25,00 мл воды? Изменится ли расход раствора КМnО4 для титрования навески, если растворить ее в другом объеме воды?
6. Найти ω% Fе (II) в растворе соли Мора, если на титрование 1г соли затрачивается 22 мл 0,1 н раствора КМnО4.
7. Найти ω% (Fе) в образце, если 0,9938г его растворено в кислоте и раствор доведен в мерной колбе до 200мл. На титрование Fе(II) из 50мл этого раствора затрачивается 20,5мл раствора перманганата калия с титром по железу 0,005851 г/мл.
8. Для анализа взята навеска породы массой 0,5 г с содержанием железа 69,96%. После растворения навески в кислотах, полученный раствор разбавлен в мерной колбе до 250 мл. Какой объем 0,1 н раствора перманганата калия требуется на титрование ионов железа, восстановленных до Fе(II) из 100 мл этого раствора?
9. Найти ω% железа в руде. Навеску массой 2г растворили в кислотах и раствор разбавили водой в мерной колбе до 200 мл. На титрование Fе(II) из 50 мл этого раствора затрачивается 22 мл 0,1 н раствора перманганата калия с поправочным коэффициентом К=1,022.
10. Найти ω% Н2С2О4∙2Н2О в образце, если его навеска массой 2 г растворена в воде и доведена в мерной колбе до 300мл. На титрование 25 мл этого раствора затрачено 24мл раствора перманганата калия с молярной концентрацией эквивалентов равной 0,1 моль/л.
