Энергия связи С—С, кДж/моль: 335; 322; 314; 310; 314; 322; 335
Энергия связи С—Н, кДж/моль: 394; 373; 364; 360; 360; 364; 373; 394
С повышением температуры различие в прочности связей С—С уменьшается. При умеренной температуре (400–500°С) разрыв углеводородной цепи происходит посередине, по наиболее слабым связям. С повышением температуры может происходить разрыв и других связей.
Связи С—С в циклоалканах несколько менее прочны, чем в нормальных алканах: в циклогексане — на 8 кДж/моль, в циклопентане — на 25 кДж/моль.
Связи С—С и С—Н в алкенах у атома углерода с двойной связью значительно прочнее, а в 5-положении — сильно ослаблены по сравнению с алканами (цифры означают энергию связи в кДж/моль):
H H
375 | | 321
R – CH2 – CH2 – C – C – CH = CH2
334 |259| 371
H H
Энергия раскрытия π-связи в алкене при сохранений σ-связи равна 239 кДж/моль:
• •
СН2=СН2 ® СН2СН2 — 239 кДж/моль
Если двойная связь является сопряженной, то энергия раскрытия π-связи примерно на 50 кДж/моль меньше:
• •
СН2=СН—СН=СН2 ® СН2=СН— СН—СН2 — 188 кДж/моль
В аренах связи С—Н и С—С прочнее, чем связи С—Н и С—С в алканах, а связи, сопряженные с ароматическим кольцом, ослаблены. Сопряжение с кольцом понижает прочность связи примерно в той же мере, как и сопряжение с двойной связью.
Реакции радикалов. Радикалы, являясь химически ненасыщенными частицами, обладают высокой реакционной способностью и вступают в различные реакции с очень большой скоростью. По активности радикалы можно расположить в ряд:
. . . . . . . .
C2H3>CH3=C3H7=втор-C4H9>C6H5 >C2H5>трет-C4H9>C6H5CH2>CH2=CHCH2>
.
(C6H5)2CH.
Различают следующие реакции радикалов:
1) моно- и бимолекулярную диссоциацию молекул на два свободных радикала (инициирование цепи)
• •
С2Н6 ® СН3 + СН3
•
C2H6 + C2H4 ® 2С2Н5
2) замещение
• •
CH3 + C2H6 ® CH4 + C2H5
3) распад радикалов с образованием ненасыщенных молекул
и новых свободных радикалов; распад протекает преимуществен-
но по β-связи по отношению к атому углерода с неспаренным
электроном (β -правило)
• •
СН3СН2СНСН3 —> СН2=СНСН3 + СН3
4) присоединение радикалов по кратной связи (реакция, обратная предыдущей)
• •
СН3 + С2Н4 ® С3Н7
5) изомеризация свободных радикалов. Предполагают, что
изомеризация протекает через циклическое переходное состояние
•
•
CH2CH2CH2CH2CH2CH2CH3 « 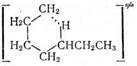 «CH3CH2CH2CH2CH2CHCH3
«CH3CH2CH2CH2CH2CHCH3
Легче образуются 6-членные циклы, труднее 5- и 7-членные, 3- и 4-членные циклы слишком напряжены, поэтому 1,2- и 1,3-изомеризация алкильных радикалов практически неосуществима.
Обрыв цепи. Осуществляется следующими реакциями:
6) рекомбинацией радикалов
• •
СН3 + СН3 ® С2Н6
7) диспропорционированием
• •
СН3 + С2Н5 ® СН4 + С2Н4
Как уже было отмечено выше, энергия активации реакции 1) —инициирования цепи — определяется энергией связи С—С в углеводороде. β-распад крупных радикалов (С3 и выше) — реакция 3) — протекает с энергией активации 110–170 кДж/моль. Взаимодействие относительно устойчивых метальных и этильных радикалов и атомов водорода с исходными молекулами-реакция 2) — требует энергии активации всего 25–37 кДж/моль. Энергия активации реакций обрыва цепи — рекомбинации 6) и диспропорционирования 7) — равна 0. Энергия активации суммарной цепной реакции для бутана составляет 245 кДж/моль.
Реакции термического разложения обычно описываются уравнениями первого порядка. Однако четкое математическое описание всего комплекса термических реакций не представляется пока возможным ввиду того, что крекинг и пиролиз даже простейших углеводородов включает множество элементарных актов. Кроме того, на кинетику цепной реакции крекинга оказывают влияние продукты реакции.
Термические превращения углеводородов в газовой фазе
Превращения алканов
Термодинамически возможны следующие реакции алканов:
| T, К | |
| Дегидрирование С2—С10 | ≥1000 |
| Циклизация С6 ® цикло-С6 + Н2 | ≥1100 |
| С10 ® цикло-С10 + Н2 | ≥800 |
| Ароматизация С6—С10 | ≥630 |
| Крекинг С3—С10 | ≥ 600—700 |
Экспериментальные данные по составу продуктов термического распада алканов хорошо объясняются радикально-цепным механиз-мом реакции. Крекинг бутана, например, можно представить следующей схемой.
Вначале за счет разрыва связи С—С в наиболее слабом месте образуются первичные свободные радикалы (инициирование цепи):
•

 2СН3СН2
2СН3СН2
 СН3СН2СН2СН3 • •
СН3СН2СН2СН3 • •
 СН3 + СН3СН2СН2
СН3 + СН3СН2СН2
Затем процесс развивается по двум возможным направлениям. Крупные, относительно неустойчивые радикалы (С3 и выше) самопроизвольно распадаются по β-правилу с образованием более устойчивых метильных и этильных радикалов или атомов водорода и соответствующих молекул алкенов:
• •
 (СН3СН=СН2) + Н
(СН3СН=СН2) + Н
 СН3СН2С·Н2
СН3СН2С·Н2
 •
•
(СН2=СН2) + СН3
(в скобках — конечные продукты).
Устойчивые в отношении распада, но чрезвычайно реакционноспособные метальные и этильные радикалы и атомы водорода вступают в реакцию с исходными молекулами, отрывая от них атом водорода:
• •
H + С4H10 ® (H2) + С4Н9
• •
CH3 + C4H10 ® (CH4) + C4H9
• •
СН3СН2+С4Н10 ® (СН3СН3) + C4H9
В результате образуются водород, метан, этан и вторичные бутильные радикалы. Образование первичных бутильных радикалов менее вероятно. Прочность С—Н-связи при первичном углеродном атоме выше, чем при вторичном. При 600°С вероятности отрыва радикалом от молекулы исходного вещества первичного, вторичного или третичного атомов водорода соотносятся как 1:2:10. В бутане шесть первичных атомов водорода и четыре вторичных; таким образом, вероятности образования первичных и вторичных бутильных радикалов относятся как (6 х 1) : (4 х 2) = 3 : 4.
Бутильные радикалы далее распадаются по β-правилу, а образующиеся при этом мелкие радикалы снова реагируют с исходными молекулами. Развивается цепной процесс. Обрыв цепи происходит в результате реакций рекомбинации и диспропорционирования.
