Константа скорости хим. реакции и ее зависимость от температуры. Правило Вант-Гоффа, уравнение Аррениуса
Константа скорости реакции (удельная скорость реакции) — коэффициент пропорциональности в кинетическом уравнении.
Скорость химической реакции зависит от температуры, причем при повышении температуры скорость реакции увеличивается. Голландский ученый Якоб Вант-Гофф показал, что при повышении температуры на десять градусов скорость большинства реакций увеличивается в 2—4 раза;

Где к – константа скорости реакции, к0 – предэкспоненциальный множитель, е – основание натурального логарифма, Еа – постоянная, называемая энергией активации, определяемая природой реакции. Значения Еа для химических реакций лежат в пределах от 40 до 400 кДж/моль. Уравнение Аррениуса позволяет проводить более точные расчеты изменения скорости реакции с увеличением температуры, чем уравнение Вант-Гоффа.
14.
Адсорбция физическая и химическая, изотерма адсорбции, константа адсорбционного равновесия.
Процесс поглощения одного вещества поверхностью другого называют адсорбцией. Вещество, частицы которого поглощаются, называется адсорбатом, поглотитель – адсорбентом. Взаимодействия между частицами адсорбата и адсорбента могут иметь различный характер. В зависимости от природы этого взаимодействия различают адсорбцию физическую и химическую.
физическая адсорбция – частицы адсорбата и адсорбента связываются прочными межмолекулярными силами взаимодействия (силами Ван-дер-Ваальса). (Адсорбция газов или растворенных веществ активированным углем)
хемосорбция – частицы адсорбата и адсорбента связаны более прочными силами сцепления за счет возникновения хим. взаимодействия, приводящего к образованию нового вещества. (адсорбция кислорода металлами).
Величина адсорбции зависит от природы адсорбента и адсорбата, температуры и концентрации (или давления) адсорбата. Кривую зависимости величины адсорбции от равновесных концентраций или давлений адсорбата при постоянной температуре называют изотермой адсорбции. Зависимость величины адсорбции от концентрации адсорбента выражается уравнением Лэнгмюра
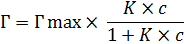
Где Г – величина адсорбции; Гmax – максимальная величина адсорбции, обусловленная поверхностью адсорбента; К – константа адсорбционного равновесия; с – равновесная концентрация адсорбента.
15.
Комплексные соединения
Сложные соединения, у которых имеются ковалентные связи, образованные по донорно-акцепторному механизму, получили название комплексных или координационных соединений. Эти соединения имеют в своем составе устойчивые группы, называемые комплексами, которые переходят без изменения из одного состояния в другое и сохраняются при растворении соединений. Комплексные соединения состоят из двух сфер: внешеней и внутренней. Внутренняя сфера, называемая также комплексом, включает центральный ион или атом, вокруг которого координируются отрицательно заряженные ионы или нейтральные молекулы. При записи копмлексного соединения внутреннюю сферу или комплекс заключают в квадратные скобки. Центральный ион или атом называется комплексообразователем, а координируемые им ионы или молекулы – лигандами. Число монодентантных лигандов, координируемых комплексообразователем, называется координационным числом. В зависимомти от заряда различают анионные, катионные и нейтральные комплексы. Нейтральные комплексы не имеют внешней сферы. Комплексообразователями служжат атомы или ионы, имеющие вакантные орбитали. К числу лигандов относятся простые и сложные анионы и некоторые молекулы. В зависимомти от числа вакантных орбиталей лиганды бывают монодентантными, бидентантными и поли дентантными.
