Эмпирическое правило Вант-Гоффа, уравнение Аррениуса. Энергия активации.
Скорость химических реакций сильно зависит от температуры. Согласно эмпирическому правилу Вант-Гоффа (1884) при повышении температуры на 10 градусов скорость большинства реакций возрастает в 2—4 раза. Число, показывающее, во сколько раз возрастает скорость реакции при повышении температуры на 10 градусов, называется температурным коэффициентом (γ) скорости данной реакции.
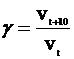
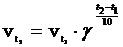
Шведский химик Сванте Аррениус в 1889 высказал мысль, что в реакцию вступают лишь те столкнувшиеся молекулы, у которых кинетическая энергия превышает некоторую минимальную величину, характерную для данной реакции, называемую энергией активации. Такие молекулы получили называние активных.
Молекулы обладают разной кинетической энергией и, следовательно, неодинаковой скоростью движения. Используя специальные методы математической статистики и теории вероятности, для каждой температуры можно получить количественное описание этого распределения (Максвелла).
Максимумы на кривых отвечают наиболее вероятной скорости при указанной температуре.
Например: при 20°С около 10% молекул кислорода обладают скоростями, превышающими 700 м/с. А при 100 градусов доля молекул со скоростями, превышающими 700 м/с, становится равной 17 %.
Та дополнительная энергия, которую надо придать молекулам реагирующих веществ для того, чтобы сделать их активными, называется энергией активации Еа. Она определяется природой реагирующих веществ и служит важной кинетической характеристикой любой химической реакции.
Уравнение Аррениуса связывает константу скорости реакции с ее энергией активации:
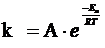
где: k - константа скорости реакции;
A —предэкспоненциальный множитель (множитель Аррениуса), постоянный для данной реакции;
e— основание натурального логарифма;
Ea- энергия активации, Дж/моль;
Т – температура, K;
R – универсальная газовая постоянная, 8,314 Дж/моль K.
Понятия о катализе, катализаторах и ингибиторах. Природа
Катализа.
Катализомназывается изменение скорости химической реакции под действием веществ, химический состав и количество которых в результате реакции остаются неизменными. Эти вещества получили название катализаторов.
Скорость химической реакции в присутствии катализаторов может увеличиваться или уменьшаться. В первом случае говорят о положительном, во втором — об отрицательном катализе. Отрицательный катализ часто называют ингибированием, а вещества, вызвавшие его, — ингибиторами.
7. Практическое использование гетерогенного катализа на примере производства аммиака или серной кислоты.
1. 4FeS2 + 11O2 = 2Fe2O3 + 8SO2
2. 2SO2 + O2 (V2O5) → 2SO3
3. SO3 + H2O → H2SO4
Известно сотни веществ, ускоряющих окисление SO2 до SO3, три лучших из них в порядке уменьшения активности: платина, пятиокись ванадия и окись железа. При этом платина отличается дороговизной и легко отравляется примесями, содержащимися в газе SO2, особенно мышьяком. Окись железа требует высоких температур для проявления каталитической активности (выше 625 гр. C). Таким образом, ванадиевый катализатор является наиболее рациональным, и только он применяется при производстве серной кислоты.
