Особенности физико-химических свойств воды
Организм взрослого человека на 65% состоит из воды, а новорождённого – на 75%. ⅔ от общего количества воды составляет внутриклеточная вода, ⅓ - внеклеточная.
Вода поступает в организм двумя путями: 1) алиментарным (еда, питьё) – 1,5-2,0 литра в сутки; 2) эндогенным (вода, образующаяся при метаболических превращениях) – 0,35-0,4 л в сутки.
Вода в организме участвует в:
- процессах метаболизма;
- терморегуляции как теплоноситель и хладагент;
- трансформации энергии (синтез и гидролиз макроэргических соединений);
- процессе диссоциации электролитов как полярный растворитель;
- растворении минеральных и органических веществ, газов, жидкостей.
Свойства воды объясняются строением её молекул и структурированностью.
Молекула воды имеет 2 ковалентные полярные связи – О-Н. Электронная плотность в них сдвинута в сторону более электроотрицательного кислорода, имеющего 2 неподелённые электронные пары. Вследствие этого, на обоих атомах водорода локализуются частичный положительный заряд – δ+, а на атомах кислорода – частичный отрицательный – δ-. Т.о., молекулы Н2О – биполярные, что определяет взаимодействие между ними. Благодаря такому распределению зарядов, соседние молекулы Н2О могут притягиваться друг к другу за счёт сил электростатического взаимодействия между атомом кислорода одной молекулы Н2О и атомом водорода другой (рис. 3.1).
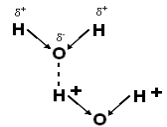
Рис. 3.1. Водородные связи между молекулами воды
Такой тип электростатического притяжения называют водородной связью. Молекулы воды находятся в непрерывном движении, поэтому водородные связи постоянно быстро разрушаются и вновь образуются. За счёт водородных связей между молекулами воды образуются тетраэдры или кластеры. Молекулы воды, которые не образуют тетраэдры, могут входить и выходить из кластеров (рис. 3.2).
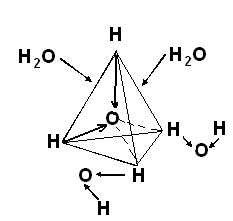
Рис. 3.2. Кластеры воды
Водородные связи слабее ковалентных. Однако, благодаря их многочисленности, они обеспечивают многие аномальные физические свойства воды:
- высокую удельную теплоёмкость;
- высокую температуру кипения;
- высокую температуру кристаллизации;
- высокую удельную теплоту испарения;
Вода, как полярный растворитель, имеет хорошую растворяющую и диссоциирующую способность. Водородные связи образуются при растворении в воде кристаллических солей, способных ионизироваться молекулами Н2О, и многих органических соединений (альдегиды, аминокислоты, спирты, кетоны, углеводы). Растворимость этих веществ обусловлена способностью молекул Н2О образовывать водородные связи с функциональными группами этих соединений.
В воде могут находиться в диспергированном (раздробленном состоянии) вещества, содержащие в своём составе одновременно гидрофобные и гидрофильные группы. Такие соединения называют амфипатическими. Примерами могут служить калиевые и натриевые соли высших жирных кислот (ВЖК) – мыла. Ионизированная в воде карбоксильная группа ВЖК или её соли образует полярную головку, а углеводородный радикал – гидрофобный хвост (рис.3.3).
 |
Рис. 3.3. Строение амфипатических веществ
Соль ВЖК легко диспергируется в воде, образуя агрегаты, называемые мицеллами. В них гидрофобные хвосты жирной кислоты скрыты от водной фазы внутри мицеллы, а полярные головки обращены к Н2О, образуя с ней водородные связи (рис. 3.4). На этом свойстве основана способность амфипатических веществ поддерживать в диспергированном в воде состоянии даже неполярные вещества. Именно так происходит эмульгирование пищевых жиров в двенадцатиперстной кишке под действием амфипатических веществ, содержащихся в жёлчи – жёлчных кислот и фосфолипидов.
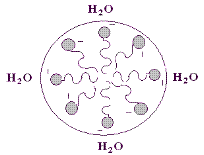 |
Рис. 3.4. Диспергирование в воде амфипатических веществ
Водородные связи характерны не только для воды, они широко распространены в биологических системах. Водородные связи легко образуются между любым электроотрицательным атомом (F, О или N) и атомом Н, ковалентно связанным с другим электроотрицательным атомом. Приведём несколько примеров возникновения водородных связей в биологических системах:
1. Между комплементарными азотистыми основаниями нуклеиновых кислот, стабилизируя их вторичную структуру. Водородные связи возможны между А и Т, а также между Г и Ц.
2. Водородные связи стабилизируют вторичную, третичную и четвертичную структуры белковых молекул.
