Реакция замещения между хлоридом меди (II) и железом
Реальный химический эксперимент
Первоначальные химические понятия
Цель работы________
Разложение основного карбоната меди
Оборудование и реактивы: штатив, пробирка, пробка с газоотводной трубкой, спиртовка, стакан или пробирка, малахит, известковая вода.
 Соберите прибор для разложения основного карбоната меди, для чего закройте пробирку пробкой с газоотводной трубкой и проверьте прибор на герметичность. Поместите в пробирку небольшое количество малахита. Закрепите пробирку в лапке штатива, как показано на рисунке. Конец газоотводной трубки опустите в стакан с известковой водой. Начинайте нагревать пробирку.
Соберите прибор для разложения основного карбоната меди, для чего закройте пробирку пробкой с газоотводной трубкой и проверьте прибор на герметичность. Поместите в пробирку небольшое количество малахита. Закрепите пробирку в лапке штатива, как показано на рисунке. Конец газоотводной трубки опустите в стакан с известковой водой. Начинайте нагревать пробирку.
Проверка прибора на герметичность
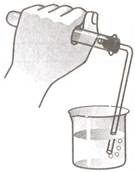 Перед использованием любого прибора для получения газов необходимо проверить герметичность соединения всех деталей. Если прибор окажется негерметичным, то собранный газ будет содержать примесь воздуха или его вообще не удастся собрать. Рассмотрите рисунок и составьте подробную инструкцию, как проверить прибор на герметичность.
Перед использованием любого прибора для получения газов необходимо проверить герметичность соединения всех деталей. Если прибор окажется негерметичным, то собранный газ будет содержать примесь воздуха или его вообще не удастся собрать. Рассмотрите рисунок и составьте подробную инструкцию, как проверить прибор на герметичность.
Инструкция по проверке прибора на герметичность
________________________________
Какое физическое явление лежит в основе этого способа проверки герметичности прибора?
________________________________
· Какие изменения происходят во время нагревания?
________________________________
· На какие вещества разлагается малахит? Запишите уравнение реакции.
________________________________
- Чем объясняется наклонное положение пробирки?
________________________________
- В раствор какого вещества помещается газоотводная трубка? Почему?
________________________________
- Сколько химических реакций вы наблюдаете во время данного опыта?
________________________________
Когда прекратится выделение газа, газоотводную трубку, не прекращая нагревания, необходимо обязательно вынуть из стакана. Почему?
______
Что произойдет при длительном пропускании углекислого газа через известковую воду? Почему? Составьте уравнение соответствующей реакции.
______
Реакция соединения серы с железом
Оборудование и реактивы: весы с разновесами, пробирка, держатель, магнит, фильтровальная бумага, асбестированная сетка, стеклянная палочка, спиртовка, сера, железо (порошок).
При выполнении опыта рассмотреть кислотно-основные и окислительно-восстановительные свойства простых веществ серы и железа на основании их положения в Периодической системе химических элементов Д.И. Менделеева.
Приготовьте смесь веществ в соотношении 7:4 (Ar (Fe):Ar(S)=56:32). Отвесьте необходимые количества серы и железа, перемешайте их и насыпьте на лист белой бумаги.
Какой цвет имеет смесь веществ?
__
Каким образом можно отделить серу и железо друг от друга?
____
Перенесите смесь в пробирку, закрепите ее в лапке штатива или держателе и нагревайте до тех пор, пока смесь не раскалится докрасна хотя бы в одном месте. Далее реакция продолжится сама собой. Для извлечения полученного вещества из пробирки, ее необходимо разбить.
Как доказать, что между серой и железом произошла химическая реакция? Приведите уравнение реакции.
____
Укажите окислитель и восстановитель в приведенной реакции
2-ой вариант: приготовленную смесь насыпьте на асбестированную сетку, сильно накалите конец стеклянной палочки и дотроньтесь им до смеси. Стеклянную палочку не выводите из смеси до окончания реакции.
Каковы преимущества и недостатки постановки данного опыта в каждом из вышеописанных вариантов?
______________
Возможные неполадки при проведении опыта
1. Для опыта надо брать восстановленное железо. При использовании обычных опилок реакция не идет. Почему?
________________________________
2. Реакция не пойдет или будут наблюдаться только отдельные вспышки, если смесь плохо перемешана. Почему?
________________________________3. Реакция не пойдет, если крупинки железа очень велики. Почему?
________________________________
Реакция замещения между хлоридом меди (II) и железом
Оборудование и реактивы:р-р хлорида меди или медного купороса, железные кнопки или скрепки.
В пробирку или в одно из гнезд пластины с углублениями налейте разбавленный раствор хлорида меди (II) голубого цвета и опустите обезжиренную канцелярскую кнопку или скрепку. В другое гнездо налейте раствор соли и оставьте без изменения.
Что происходит в пробирке?
______
По каким признакам мы можем судить о том, что произошла химическая реакция?
____
Какие вещества образовались в результате реакции? Приведите уравнение.
____
