Для опыта удобно воспользоваться реакцией
FeCl3 + 3KSCN 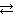 Fe(SCN)3 + 3KCl.
Fe(SCN)3 + 3KCl.
Из веществ этой системы только роданид железа (III) Fe(SCN)3 окрашен в красный цвет. Поэтому всякое изменение его концентрации можно легко заметить по изменению интенсивности окраски раствора, что позволяет сделать вывод о направлении смещения равновесия системы при изменении концентрации реагирующих веществ.
Смешать в пробирке равные объемы разбавленных растворов хлорида железа (III) и роданида калия. Полученный раствор разлить поровну в 4 пробирки. Оставить одну пробирку для сравнения, а в трех других изменить концентрации реагирующих веществ. Для этого добавить в первую пробирку несколько капель концентрированного раствора роданида калия, во вторую – несколько капель концентрированного раствора хлорида железа (III), в третью – кристаллического хлорида калия. Сравнить окраску в трех пробирках с контрольной.
Требования к результатам опыта
1. Сделать вывод о направлении смещения равновесия и изменении концентрации каждого из компонентов в каждой пробирке.
2. Сформулировать правило смещения равновесия при изменении концентрации реагирующих веществ.
3. Написать выражение константы равновесия для данной реакции.
Опыт 2. Влияние изменения температуры на смещение равновесия
Прибор, состоящий из двух шаров, заполнен смесью оксида азота (IV) и его димером. Чистый оксид азота (IV) существует при температуре выше 140 °С. Ниже этой температуры NO2 частично полимеризуется по уравнению
2NO2 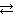 N2O4, ΔH° = –23 кДж.
N2O4, ΔH° = –23 кДж.
NO2 – газ бурого цвета, N2O4 – бесцветен. Изменение температуры позволяет судить о смещении равновесия в системе по изменению интенсивности окраски газов.
Один шар прибора опустить в стакан с холодной, а второй – в стакан с горячей водой. Наблюдать изменение интенсивности окраски газов в шарах.
Требования к результатам опыта
1. Сделать вывод о направлении смещения равновесия в данной реакции при нагревании и охлаждении.
2. Сформулировать правило смещения равновесия при изменении температуры.
3. Написать выражение константы равновесия для данной реакции.
Примеры решения задач
Пример 6.1. При некоторой температуре в системе N2 (г) + 3Н2 (г) 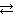 2NH3 (г) равновесные концентрации составляли (моль/л): [N2] = 1,5; [H2] = 1,7; [NH3] = 2,6. Вычислить константу равновесия этой реакции и исходные концентрации азота и водорода.
2NH3 (г) равновесные концентрации составляли (моль/л): [N2] = 1,5; [H2] = 1,7; [NH3] = 2,6. Вычислить константу равновесия этой реакции и исходные концентрации азота и водорода.
Решение.Константа равновесия данной реакции выражается уравнением
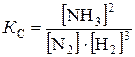 .
.
Подставляя данные задачи, получаем 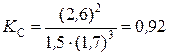 .
.
Исходные концентрации азота и водорода находим на основе уравнения реакции. Согласно уравнению реакции на образование 2 моль NH3 расходуется 1 моль N2. По условию задачи образовалось 2,6 моль NH3, на что израсходовалось 1,3 моль N2. Учитывая равновесную концентрацию азота, находим его исходную концентрацию: 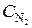 = 1,5 + 1,3 = 2,8 моль/л.
= 1,5 + 1,3 = 2,8 моль/л.
По уравнению реакции на образование 2 моль NH3 необходимо 3 моль H2, а для получения 2,6 моль NH3 требуется 3×2,6/2 = 3,9 моль H2. Исходная концентрация водорода 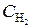 = 1,7 + 3,9 = 5,6 моль/л. Таким образом, КС = 0,92; исходные концентрации
= 1,7 + 3,9 = 5,6 моль/л. Таким образом, КС = 0,92; исходные концентрации 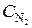 = 2,8,
= 2,8, 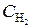 = 5,6 моль/л.
= 5,6 моль/л.
Пример 6.2. Реакция протекает по уравнению А + В 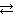 D + F. Определить равновесные концентрации реагирующих веществ, если исходные концентрации веществ А и В, соответственно, равны 2 и 1,2 моль/л, а константа равновесия реакции КС = 1.
D + F. Определить равновесные концентрации реагирующих веществ, если исходные концентрации веществ А и В, соответственно, равны 2 и 1,2 моль/л, а константа равновесия реакции КС = 1.
Решение. Так как все вещества в данной реакции реагируют в одинаковых соотношениях, обозначим изменение концентрации всех реагирующих веществ через x. К моменту установления равновесия образовалось х моль D и х моль F и соответственно [D] = x; [F] = x. По уравнению реакции на столько же уменьшились концентрации А и В, т. е. [A] = 2 – x; [B] = 1,2 – x. Подставим равновесные концентрации в выражение константы равновесия:
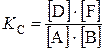 ;
; 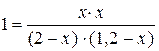 ; х = 0,75.
; х = 0,75.
Отсюда равновесные концентрации равны: [D] = 0,75 моль/л; [F] = 0,75 моль/л;
[A] = 2 – 0,75 = 1,25 моль/л; [B] = 1,2 – 0,75 = 0,45 моль/л.
Пример 6.3. Реакция протекает по уравнению 2SO2 + O2 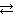 2SO3. В каком направлении сместится химическое равновесие, если объем системы уменьшить в 3 раза?
2SO3. В каком направлении сместится химическое равновесие, если объем системы уменьшить в 3 раза?
Решение. До изменения объема скорости прямой и обратной реакций выражались уравнениями:
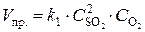 ;
; 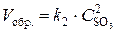 .
.
При уменьшении объема в 3 раза концентрация каждого из реагирующих веществ увеличится в 3 раза. После увеличения концентрации скорость прямой реакции стала 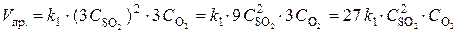 ,
,
т. е. возросла в 27 раз; а скорость обратной – 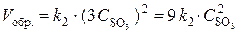 , т. е. возросла в 9 раз. Следовательно, равновесие сместится в сторону прямой реакции (вправо).
, т. е. возросла в 9 раз. Следовательно, равновесие сместится в сторону прямой реакции (вправо).
Пример 6.4. В какую сторону сместится химическое равновесие реакции А + В 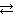 D, если повысить температуру на 30 °С? Температурные коэффициенты скорости прямой (γ1) и обратной (γ2) реакции равны соответственно 2 и 3.
D, если повысить температуру на 30 °С? Температурные коэффициенты скорости прямой (γ1) и обратной (γ2) реакции равны соответственно 2 и 3.
Решение. При повышении температуры на 30° скорость прямой реакции возрастет в 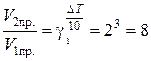 раз, а скорость обратной в
раз, а скорость обратной в 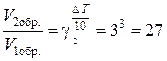 раз. Так как скорость обратной реакции возросла в 27 раз, а скорость прямой в 8 раз, то равновесие этой реакции при повышении температуры сместится в сторону обратной реакции (влево).
раз. Так как скорость обратной реакции возросла в 27 раз, а скорость прямой в 8 раз, то равновесие этой реакции при повышении температуры сместится в сторону обратной реакции (влево).
Пример 6.5. Как изменятся скорости прямой и обратной реакции, если в системе 2NO (г) + О2 (г) 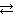 2NO2 (г) уменьшить давление в 2 раза? Произойдет ли при этом смещение равновесия? Если да, то в какую сторону?
2NO2 (г) уменьшить давление в 2 раза? Произойдет ли при этом смещение равновесия? Если да, то в какую сторону?
Решение. До уменьшения давления выражения для скорости прямой и обратной реакции имели вид 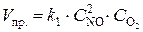 ;
; 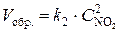 .
.
При уменьшении давления в 2 раза концентрации каждого из реагирующих веществ уменьшаются в 2 раза, так как общий объем системы увеличивается в 2 раза. Тогда 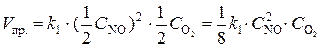 ;
;
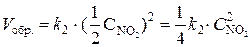 .
.
В результате уменьшения давления скорость прямой реакции уменьшилась в 8 раз, а скорость обратной – в 4 раза. Таким образом, скорость обратной реакции будет в 2 раза больше, чем прямой, и смещение равновесия произойдет в сторону обратной реакции, т. е. в сторону разложения NO2.
Пример 6.6. В каком направлении сместится равновесие реакции
COCl2 ↔ СО + Cl2, ∆H°х.р. = +112,5 кДж
а) при повышении давления; б) с понижением температуры; в) при уменьшении концентрации хлора?
Решение. а). При повышении давления равновесие смещается в сторону реакции, идущей с уменьшением числа молекул газа, при понижении давления – в сторону реакции, идущей с увеличением числа молекул газа. В левой части приведенной реакции 1 молекула (COCl2), а в правой – 2 (1 СО и 1 Cl2), поэтому при повышении давления равновесие смещается в сторону обратной реакции.
б). При понижении температуры равновесие смещается в сторону экзотермической реакции, при повышении температуры – в сторону эндотермической. В нашем примере прямая реакция эндотермическая (∆H°х.р. > 0), а обратная – экзотермическая, следовательно, при понижении температуры равновесие сместится в сторону обратной реакции. в). При увеличении концентрации исходных веществ и уменьшении концентрации продуктов реакции равновесие смещается в сторону продуктов реакции. При уменьшении концентрации хлора (продукта реакции) равновесие сместится в сторону прямой реакции, т.е. в сторону образования продуктов реакции.
