Теоретическое введение. Карбоновые кислоты – производные углеводородов, в молекулах которых один или
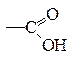 Карбоновые кислоты – производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на карбоксильную группу
Карбоновые кислоты – производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на карбоксильную группу
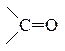 Особенности химических свойств карбоновых кислот обусловлены сильным взаимным влиянием карбонильной
Особенности химических свойств карбоновых кислот обусловлены сильным взаимным влиянием карбонильной
и гидроксильной О−Н групп.
Поэтому все химические реакции карбоновых кислот будут идти по следующим направлениям:
Замещение водорода в гидроксильной группе. Карбоновые кислоты – слабые электролиты и взаимодействуют с активными металлами, оксидами и гидроксидами металлов с образованием солей:
2CH3COOH + Mg → Mg(CH3COO)2 + H2;
уксусная кислота ацетат магния
C2H5COOH + NaOH → C2H5COONa + H2O.
пропионовая кислота пропионат натрия
Замещение всей гидроксильной группы. Карбоновые кислоты реагируют со спиртами в присутствии сильных неорганических кислот, в результате образуется сложный эфир:
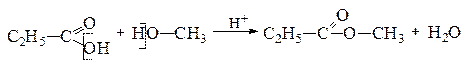 |
пропионовая метиловый метиловый эфир пропионовой кислоты
кислота спирт (метилпропионат)
Выполнение работы
Опыт 1. Свойства карбоновых кислот
· Налить в пробирку 2−3 мл раствора уксусной кислоты и внести туда немного стружек магния. Что наблюдается? Какое свойство карбоновых кислот характеризует этот опыт?
· В пробирку насыпать немного соды Na2CO3 и прилить раствор уксусной кислоты. Что наблюдается?
· В пробирку насыпать немного уксуснокислого натрия СН3СООNa и прилить 1−2 мл концентрированной серной кислоты. Слегка нагреть. Запах какого вещества обнаруживается?
Требование к результатам опыта
Записать наблюдения и составить уравнения реакций взаимодействия:
магния с уксусной кислотой; соды с уксусной кислотой; уксуснокислого натрия с серной кислотой.
Опыт 2. Получение уксусноэтилового эфира
Налить в пробирку по 2 мл: концентрированной уксусной кислоты, этилового спирта и концентрированной серной кислоты. Пробирку со смесью опустить на 1−2 мин в кипящую воду, после чего содержимое пробирки вылить в пробирку с раствором поваренной соли (NaCl уменьшает растворимость эфира). Через несколько минут на поверхность всплывет уксусноэтиловый эфир, который можно узнать по характерному запаху.
Требование к результатам опыта
Написать уравнение реакции получения уксусноэтилового эфира (Н2SO4 играет роль водоотнимающего вещества).
Опыт 3. Выделение карбоновых кислот из мыла
В стакан налить 20−30 мл воды, всыпать туда несколько ломтиков простого мыла. Для лучшего растворения нагреть, все время помешивая стеклянной палочкой.
К полученному раствору добавить 2−3 мл 10 %-го раствора серной кислоты и еще раз нагреть почти до кипения. На поверхности появляется слой кислот, выделенных из взятого мыла. При охлаждении эти кислоты затвердевают в твердый кружок.
Требование к результатам опыта
Написать уравнение реакции между натриевой солью стеариновой кислоты С17Н35СООNa и серной кислотой.
Примеры решения задач
Пример 30.1.Составить уравнения реакций, которые надо провести для осуществления следующих превращений: Метан → X → Y → уксусная кислота.
Назвать вещества X и Y.
Решение. При нагревании метана получают ацетилен – вещество Х:
2СН4 → С2Н2 + 3Н2.
Гидратацией ацетилена в присутствии солей ртути (II) синтезируют уксусный альдегид – вещество Y:
C2H2 + H2O → CH3COH.
Окислив уксусный альдегид кислородом воздуха в присутствии катализатора, получают уксусную кислоту:
2СН3СОН + О2 → 2СН3СООН.
Пример 30.2. В трех пробирках без надписей находятся следующие вещества: этанол, муравьиная кислота, уксусная кислота. Какие химические реакции следует провести, чтобы различить эти вещества?
Решение. Спирт (этанол) можно отличить по действию веществ на индикаторы. Например, кислоты окрашивают синий лакмус в красный цвет, спирт – нет.
Различить муравьиную и уксусную кислоту легко, так как муравьиная кислота проявляет некоторые свойства альдегидов. Например, она вступает в реакцию «серебряного зеркала» (уксусная – нет):
НСООН + Ag2O → CO2↑ + 2Ag + H2O.
Пример 30.3. Какой объем уксусной эссенции плотностью 1,07 г/мл надо взять для приготовления столового уксуса объмом 200 мл и плотностью 1,007 г/мл? Массовая доля уксусной кислоты в уксусной эссенции равна 80 %, в столовом уксусе – 6 %.
Решение. Определяем массу раствора уксуса, который надо приготовить:
m = V∙ ρ; m = 200 ∙ 1,007 = 201,4 г.
Рассчитаем массу уксусной кислоты, которая содержится в уксусе:
m (CH3COOH) = m ∙ ω (CH3COOH) = 201,4 ∙ 0,06 = 12,1 г.
Вычисляем массу уксусной эссенции m′, которая содержит уксусную кислоту массой 12,1 г:
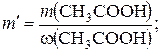
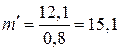 г.
г.
Находим объем уксусной эссенции:
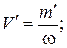
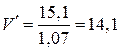 мл.
мл.
